447 - EFICACIA Y SEGURIDAD DE LOS BOLOS DE METILPREDNISOLONA EN EL TRATAMIENTO DE INDUCCIÓN DE LA ARTERITIS DE CÉLULAS GIGANTES
1Medicina Interna, Unidad de Enfermedades Autoinmunes Sistémicas y Minoritarias, Hospital Puerta de Hierro, Majadahonda, España. 2Medicina Interna, Hospital Fundación Jiménez-Díaz, Madrid, España. 3Medicina Interna, Hospital Ramón y Cajal, Madrid, España. 4Medicina Interna, Hospital Infanta Cristina, Parla, España. 5Medicina Interna, Hospital Gregorio Marañón, Madrid, España.
Objetivos: Comparar la eficacia y seguridad de los bolos de metilprednisolona (MP) con los glucocorticoides (GC) orales en el tratamiento de inducción de la arteritis de células gigantes (ACG).
Métodos: Estudio multicéntrico, observacional y retrospectivo, de pacientes diagnosticados de ACG según los criterios clasificatorios ACR/EULAR 2022. Se compararon las variables epidemiológicas, demográficas, clínicas, analíticas, el tratamiento de inducción y los desenlaces en los pacientes tratados con bolos de MP o con GC oral. Los objetivos primarios fueron el tiempo y la dosis acumulada de prednisona hasta la remisión, según la definición de las guías ACR/EULAR 2019. Los objetivos secundarios fueron la tasa de remisión, la dosis de prednisona basal, la dosis acumulada de prednisona, los efectos adversos de los esteroides, las complicaciones infecciosas y las complicaciones del tratamiento a los 3 meses del inicio de este. Se realizó un análisis multivariante incluyendo las variables basales, clínicas y tratamiento de inducción, con el objetivo de determinar en impacto de los bolos de MP en cada objetivo principal.
Resultados: Se analizaron 154 pacientes con ACG. El 63,6% eran mujeres con una edad media de 74,6 años. El 50% recibió bolos de MP y el 50% GC oral. En la tabla 1 se muestran las características basales y de la enfermedad al debut, sin diferencias en los dos grupos excepto por la mayor frecuencia de afectación vascular/isquémica en los pacientes que recibieron bolos de MP (31,2 vs. 15,6%, p = 0,022). Las diferencias en el tratamiento de inducción y objetivos del estudio se muestran en la tabla 2 y figura 1. La mediana de dosis de los bolos fue de 250 mg (RI: 125-500 mg), durante una media de 3,1 días (DE: 1,5). La mediana de la dosis posterior de prednisona tras los bolos fue de 38 mg, significativamente menor que la dosis de prednisona que recibe inicialmente el grupo control (50 mg, p = 0,01). Aunque no hubo diferencias en el tiempo hasta remisión, el grupo de MP recibió una menor dosis acumulada de prednisona en la remisión (mediana 870 vs. 1.450 mg, p < 0,001), y una dosis menor de GC a los 3 meses de inicio de tratamiento (mediana 10 vs. 15 mg, p = 0,02). En paralelo, el grupo de bolos de MP recibió con mayor frecuencia inmunosupresor asociado (57,1 vs. 19,5%, p < 0,001), a expensas del metotrexato (44,2 vs. 15,6%, p < 0,001) y tocilizumab (15,6 vs. 3,9%, p < 0,027). Tras el ajuste, los bolos de MP no se asociaron con el tiempo hasta remisión (coeficiente -1,39, p = 0,168) pero sí con la dosis acumulada hasta la remisión (coeficiente -3,87, p < 0,001).
|
Tabla 1. Características basales de la población |
||||
|
|
General (n = 154) |
Bolos MP (n = 77) |
No bolos (n = 77) |
p |
|
Características basales |
||||
|
Edad (años) (media, DE) |
74,6 (15,4) |
75,3 (12,4) |
73,9 (18) |
0,570 |
|
Sexo femenino (n, %) |
98 (63,6) |
44 (57,1) |
54 (70,1) |
0,094 |
|
Etnia caucásica (n, %) |
149 (96,8) |
75 (97,4) |
74 (96,1) |
0,367 |
|
HTA (n, %) |
99 (65,1) |
52 (68,4) |
47 (61,8) |
0,395 |
|
DM (n, %) |
36 (23,8) |
17 (22,1) |
19 (25,7) |
0,604 |
|
DL (n, %) |
69 (44,8) |
34 (44,2) |
35 (45,5) |
0,871 |
|
Obesidad (n, %) |
13 (8,9) |
8 (11) |
5 (6,8) |
0,83 |
|
Tabaco (n, %) |
15 (9,7) |
8 (10,4) |
7 (46,7) |
0,786 |
|
Osteoporosis previa (n, %) |
24 (16,6) |
9 (12,3) |
15 (20,8) |
0,168 |
|
Síntomas y signos de la enfermedad (n, %) |
||||
|
Cefalea |
88 (57,1) |
50 (64,9) |
38 (49,4) |
0,051 |
|
Claudicación mandibular |
41 (26,6) |
25 (32,5) |
16 (20,8) |
0,101 |
|
Constitucional |
82 (53,2) |
39 (50,6) |
43 (55,8) |
0,518 |
|
Fiebre |
51 (33,1) |
26 (33,8) |
25 (32,5) |
0,864 |
|
PMR |
53 (34,4) |
24 (31,2) |
29 (37,7) |
0,396 |
|
Hipersensibilidad cuero cabelludo |
25 (16,2) |
15 (19,5) |
10 (13,0) |
0,275 |
|
Vascular/isquémico |
36 (23,4) |
24 (31,2) |
12 (15,6) |
0,022 |
|
Examen temporal anómalo |
26 (16,9) |
11 (14,3) |
15 (19,5) |
0,390 |
|
Fenotipo (n, %) |
||||
|
Craneal |
94 (61) |
50 (64,9) |
44 (57,1%) |
0,321 |
|
Aortitis |
26 (16,9) |
12 (15,6) |
14 (18,2%) |
0,667 |
|
Sistémico |
51 (33,1) |
24 (31,2) |
27 (35,1) |
0,607 |
|
Territorio (n, %) |
||||
|
Craneal |
89 (57,8) |
46 (59,7) |
43 (55,8) |
0,625 |
|
Extracraneal |
28 (18,2) |
17 (22,1) |
11 (14,3) |
0,210 |
|
Aorta |
30 (19,5) |
16 (20,8) |
14 (18,2) |
0,684 |
|
Axilar bilateral |
9 (5,8) |
6 (7,8) |
3 (3,9) |
0,495 |
|
Marcadores analíticos (mediana, rango intercuartílico) |
||||
|
PCR (mg/L) |
52,1 (12,2-139,6) |
58,2 (20-108) |
44 (8,2-139,1) |
0,631 |
|
VSG (mm) |
74 (45-101,3) |
71 (45-108) |
75 (46-101) |
0,775 |
|
Ferritina (ng/ml) |
301 (149,5-512,5) |
283 (140,3-643,5) |
303 (175-491) |
0,080 |
|
Hemoglobina (g/dL) |
12,10 (10,8-13,1) |
12,2 (11,1-13,2) |
11,9 (10,8-13,1) |
0,222 |
|
Tabla 2. Tratamiento de inducción y objetivos del estudio en función de tratamiento con bolos de metilprednisolona o glucocorticoide oral |
||||
|
General (n = 154) |
Bolos MP (n = 77) |
No bolos (n = 77) |
p |
|
|
Tiempo inicio tratamiento (días), (mediana, RI) |
29 (7-74,5) |
28 (8-69) |
31 (1-89) |
0,249 |
|
Prednisona oral inducción (mg), (media, DE) |
42,6 (21,3) |
38 (49,4) |
50 (64,9) |
0,01 |
|
Inmunosupresor asociado (n, %) |
59 (38,3) |
44 (57,1) |
15 (19,5) |
< 0,001 |
|
Metotrexato (n, %) |
46 (29,9) |
34 (44,2) |
12 (15,6) |
< 0,001 |
|
Tocilizumab (n, %) |
15 (9,7) |
12 (15,6) |
3 (3,9) |
0,027 |
|
Hidroxicloroquina (n, %) |
2 (1,4) |
0 |
2 (3) |
0,227 |
|
Ácido acetilsalicílico (n, %) |
60 (42,3) |
33 (45,2) |
27 (39,1) |
0,500 |
|
Objetivos principales |
||||
|
Tiempo hasta remisión (días) (mediana, RI) |
41 (17,8-94) |
40,5 (20,5-93) |
41 (17-96) |
0,190 |
|
Dosis acumulada en remisión (mg) (mediana, RI) |
1.010 (445-1.868) |
870 (370-1.488,5) |
1.450 (607-2.437) |
< 0,001 |
|
Objetivos secundarios |
||||
|
Remisión a los 3 meses (n, %) |
84 (54,5) |
44 (57,1) |
33 (42,9) |
0,627 |
|
Dosis de prednisona a los 3 meses (mg) (media, DE) |
10 (7,5-20) |
10 (5-15) |
15 (10-20) |
0,02 |
|
Dosis acumulada a los 3 meses (mg) (media, DE) |
721,3 (303,8-1.279,8) |
979,67, 1.410,199 |
1.259,97, 1.016,401 |
0,129 |
|
Efectos adversos esteroides a los 3 meses (n, %) |
63 (40,9) |
33 (42,9) |
30 (39) |
0,743 |
|
Complicaciones infecciosas a los 3 meses (n, %) |
8 (6,2) |
5 (7,9) |
3 (4,5) |
0,486 |
|
Complicaciones de tratamiento a los 3 meses (n, %) |
8 (6,2) |
4 (6,3) |
4 (6,1) |
1 |
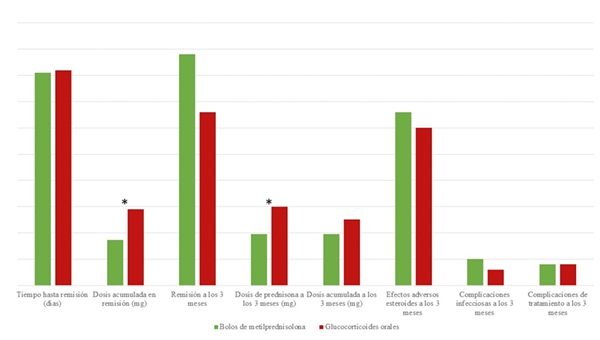
Conclusiones: Los bolos de MP suponen un ahorro significativo de esteroides en la inducción de la ACG, con una menor dosis de inicio, dosis acumulada y dosis a los 3 meses de GC oral, sin un peor perfil de seguridad. En base a estos resultados, deberían plantearse como tratamiento inicial no solo en pacientes con manifestaciones vasculares-isquémicas de la enfermedad.





