Los estudios en vida real que han evaluado el impacto de las guías de 2019 de la Sociedad Europea de Cardiología (ESC) y la Sociedad Europea de Aterosclerosis (EAS) sobre el uso de tratamientos hipolipemiantes (THL) son escasos. Este manuscrito presenta los datos basales y tras un año de seguimiento del uso de THL y la consecución de objetivos de colesterol de lipoproteínas de baja densidad (c-LDL) en la subpoblación española del estudio SANTORINI y los pone en perspectiva con la cohorte europea sin participantes españoles.
MétodosSANTORINI fue un estudio multinacional, prospectivo y observacional. La subpoblación española incluyó hasta 1018 pacientes con riesgo cardiovascular (CV) alto y muy alto.
ResultadosEn los 956 pacientes con datos de c-LDL, los niveles medios de c-LDL disminuyeron desde la visita basal (82,7±40,6mg/dl) hasta la de un año de seguimiento (72,3±32,6mg/dl) en pacientes con riesgo alto y muy alto. El porcentaje de pacientes que alcanzaron los objetivos de c-LDL, según las guías ESC/EAS de 2019, aumentó del 26,5% en la visita basal al 34,1% tras un año de seguimiento, tanto en pacientes de riesgo alto (23,1% versus 27,3%) como muy alto (27,9% versus 37,0%). La consecución de objetivos de c-LDL mejoró al iniciar tratamiento con un THL, en pacientes que no lo recibían en la visita basal, o al cambiar a una terapia combinada, en aquellos que ya lo estaban recibiendo. Durante el seguimiento, 7 pacientes fallecieron por causa CV y 46 y 24 experimentaron al menos uno de los eventos adversos CV mayores de 4 y 3 componentes, respectivamente.
ConclusionesLos datos de seguimiento de SANTORINI España muestran que el uso de THL aumentó desde la visita basal, tanto la monoterapia como la terapia combinada. A pesar de las recomendaciones, los pacientes con mayor riesgo CV siguen sin recibir el THL más adecuado para reducir sus niveles de c-LDL en la práctica clínica habitual.
Real-world studies evaluating the impact of 2019 European Societies of Cardiology (ESC) and Atherosclerosis (EAS) guidelines on the use of lipid-lowering treatments (LLTs) are scarce. This manuscript shows baseline and 1-year follow-up data on LLT usage and low-density lipoprotein cholesterol (LDL-C) goal attainment in the Spanish subpopulation from SANTORINI study and put them in perspective with the European cohort without Spanish participants.
MethodsSANTORINI was a multinational, prospective, non-interventional study. The Spanish subpopulation involved up to 1018 patients at high and very high cardiovascular (CV) risk.
ResultsOf 956 patients in LDL-C dataset, mean LDL-C levels decreased from baseline (82.7±40.6mg/dL) to 1-year follow-up (72.3±32.6mg/dL), in patients at high and very high risk. The percentage of patients who achieved 2019 ESC/EAS LDL-C goals increased from 26.5% at baseline to 34.1% at 1-year follow-up, in patients at high (23.1% versus 27.3%) and very high risk (27.9% versus 37.0%). Attainment to LDL-C targets improved while initiating treatment with a LLT in patients not receiving it at baseline or following change to a combination therapy in those who were receiving it. During the follow-up, seven patients died due to CV causes, and 46 and 24 had at least one four- or three-component major adverse CV events, respectively.
ConclusionsFollow-up data from SANTORINI Spain show that LLT usage increased from baseline, including monotherapy and combination therapy. Despite recommendations, patients at highest CV risk continue not receiving the most adequate LLT for reducing LDL-C levels in routine clinical practice.
Las enfermedades cardiovasculares (ECV) constituyen la principal causa de morbimortalidad en Europa, con 3,9 millones de muertes al año1. El colesterol unido a lipoproteínas de baja densidad (c-LDL) desempeña un papel fundamental en el desarrollo de la aterosclerosis y la formación de placas, lo que conlleva una alteración del flujo sanguíneo y un riesgo elevado de sufrir episodios cardiovasculares (CV)2. Por este motivo, la reducción de la concentración de c-LDL se ha convertido en una de las piedras angulares en la prevención de las ECV3. De hecho, la disminución en 1mmol/l del c-LDL se ha asociado a una reducción del riesgo relativo de episodios vasculares y coronarios importantes de hasta el 23%, así como a una reducción de la mortalidad total del 10% durante un período de 5años4,5. En consecuencia, en la actualización de 2019 de la guía de la Sociedad Europea de Cardiología (ESC) y de la Sociedad Europea de Aterosclerosis (EAS) se recomendaron unos objetivos más estrictos de c-LDL, es decir, por debajo de 70mg/dl (<1,8mmol/l) y 55mg/dl (<1,4mmol/l) en pacientes con riesgo CV alto y muy alto, respectivamente, junto con una reducción mínima del 50% de la concentración de c-LDL con respecto a la cifra basal5. Para poder alcanzar este objetivo, en estos pacientes se recomienda encarecidamente el uso de terapia combinada (con estatinas y tratamientos hipolipemiantes [THL] no estatínicos)6,7. En pacientes no tratados previamente con estatinas, la terapia combinada con ezetimiba y estatina ha logrado una reducción del c-LDL aproximadamente un 15% mayor que la observada con monoterapia con estatinas en las mismas dosis5,8. Además, esta combinación ha producido reducciones más significativas del c-LDL que la duplicación de la dosis de la estatina (13-20%) y el cambio de estatinas en monoterapia por terapia combinada con ezetimiba y estatina (11-15%). Durante la última década, estudios de práctica clínica con umbrales menos estrictos de c-LDL han demostrado consistentemente que muchos pacientes, incluidos los de riesgo alto y muy alto, no alcanzan las concentraciones recomendadas de c-LDL9–13. Estos estudios también han puesto de manifiesto que los THL consisten principalmente en estatinas en monoterapia y que la terapia combinada se emplea en una minoría de casos. Hasta la fecha, hay pocos estudios de práctica clínica en los que se haya evaluado el impacto de la guía ESC/EAS 2019 sobre el uso de THL14,15.
El estudio SANTORINI fue un estudio observacional, internacional y prospectivo cuyo objetivo fue evaluar la implementación de la actualización de 2019 de la guía ESC/EAS en pacientes adultos con riesgo CV alto y muy alto de 14 países europeos entre 2020 y 202116. Los resultados basales de 9136 pacientes revelaron que el 20,9% de ellos no estaba recibiendo THL, mientras que el 53,6% recibía THL en monoterapia y el 25,6%, terapia combinada. De los 7210 pacientes con datos basales y de seguimiento completos de c-LDL, la consecución de los objetivos aumentó del 21,2% en el momento basal al 30,9% en el seguimiento al cabo de un año16. En un tercio de los pacientes se realizó un aumento escalonado de los THL. También se incrementó el uso de monoterapia y terapia combinada (n=9136) (del 53,6% al 57,1% y del 25,6% al 37,9% respectivamente)16.
En este artículo se presentan los datos basales y de seguimiento al cabo de un año sobre el uso de THL y la consecución de los objetivos de c-LDL en la subpoblación española del estudio SANTORINI (denominado como SANTORINI España) y se ponen los resultados en perspectiva respecto a la cohorte europea sin participantes españoles (denominado como SANTORINI Europa sin España).
MétodosDiseño del estudio y pacientesEl estudio SANTORINI (NCT04271280) fue un estudio observacional no intervencionista en el que participaron pacientes adultos con riesgo alto o muy alto (según los médicos responsables de su atención), candidatos a recibir THL y con una esperanza de vida superior a un año en el momento de su inclusión en el estudio17. No se requirieron criterios de exclusión. La inclusión de pacientes se llevó a cabo entre marzo de 2020 y febrero de 2021 y, posteriormente, fueron seguidos durante 12±2 meses a partir del momento basal. Los pacientes reclutados podían encontrarse en situación de prevención primaria o secundaria. El estudio SANTORINI se llevó a cabo en conformidad con la Declaración de Helsinki. Todos los pacientes firmaron un consentimiento informado por escrito para participar en el estudio.
Objetivos y variablesEl objetivo principal del estudio SANTORINI consistió en describir los THL empleados en la práctica clínica habitual de ese momento en los pacientes de riesgo alto y muy alto, así como en determinar la proporción de los que cumplieron los objetivos de c-LDL recomendados por la guía ESC/EAS 20195. Los médicos responsables de la atención de los pacientes determinaron el riesgo CV de cada uno de ellos en el momento de su inclusión. Los umbrales correspondientes a los objetivos de c-LDL fueron <70mg/dl (<1,8mmol/l) en los pacientes de alto riesgo y <55mg/dl (<1,4mmol/l) en los de muy alto riesgo5. El riesgo CV durante el seguimiento se determinó como objetivo secundario y se midió por medio de la mortalidad de causa CV, los episodios CV adversos importantes (MACE, por sus siglas en inglés) de 4 componentes, los MACE de 3 componentes y la tasa de episodios por 100 años-paciente (AP). Los MACE de 4 componentes se definieron como la aparición de cualquiera de los episodios siguientes: muerte de causa CV, infarto de miocardio no mortal, ictus no mortal o revascularización coronaria (cirugía de derivación aortocoronaria o angioplastia coronaria transluminal percutánea). Los MACE de 3 componentes se definieron como la aparición de cualquiera de los episodios siguientes: muerte de origen CV, infarto de miocardio no mortal o ictus no mortal. La tasa de episodios por 100 AP se calculó como el número de pacientes con el episodio CV (basándose únicamente en el tiempo transcurrido hasta el primer episodio) dividido entre el tiempo total de exposición de todos los pacientes en riesgo (años) y multiplicado por 100.
En el presente artículo también se evalúan los objetivos utilizando los datos del estudio SANTORINI Europa sin España, es decir, SANTORINI Europa pero excluyendo los datos de España, para poner los resultados españoles en perspectiva respecto a Europa. La información sobre la intensidad de los THL aparece detallado en otra publicación18.
Análisis estadísticoEn el presente estudio observacional únicamente se han realizado análisis descriptivos. Las variables continuas se presentan en forma de media±desviación estándar (DE) y las categóricas en forma de frecuencias absolutas y relativas (%). Los resultados se presentan en la población total y en relación con el riesgo CV determinado por los médicos. Las concentraciones de c-LDL se presentan en mg/dl (para convertirlas a mmol/l, los valores deben multiplicarse por 0,02586). Las características de los pacientes, el uso de THL y el riesgo CV se evaluaron en los pacientes con cualquier dato de seguimiento disponible (es decir, población completa de análisis), mientras que las concentraciones de c-LDL y la consecución de los objetivos se evaluaron en aquellos con datos de c-LDL disponibles en el momento basal y en el seguimiento al cabo de un año (es decir, conjunto de datos de c-LDL). Los intervalos de confianza correspondientes a la consecución de los objetivos de c-LDL y las tasas de episodios CV se calcularon con la metodología de Clopper-Pearson. Todos los análisis se realizaron con el programa SAS, versión 9.4, SAS Institute Inc., Cary, NC, EE.UU.
ResultadosCaracterísticas basales de los pacientes de SANTORINI EspañaDe los 1043 pacientes reclutados en España, 1018 fueron incluidos en la población completa de análisis y 956 en el conjunto de datos de c-LDL. En la figura 1 suplementaria se muestra el diagrama de flujo de los pacientes (con los motivos de exclusión). En conjunto, los pacientes fueron predominantemente varones (72,9%), con una edad media de 63,3±11,3 años y un índice de masa corporal de 28,4±4,7kg/m2 (tabla 1). Un porcentaje elevado de pacientes presentaba enfermedad cardiovascular aterosclerótica (ECVA, 67,4%), hipertensión arterial (62,9%) y diabetes (41,4%). El 14,8% de los pacientes tenían hipercolesterolemia familiar heterocigótica. Según sus médicos, 295 pacientes (29,0%) tenían un riesgo alto y 723 (71,0%), un riesgo muy alto.
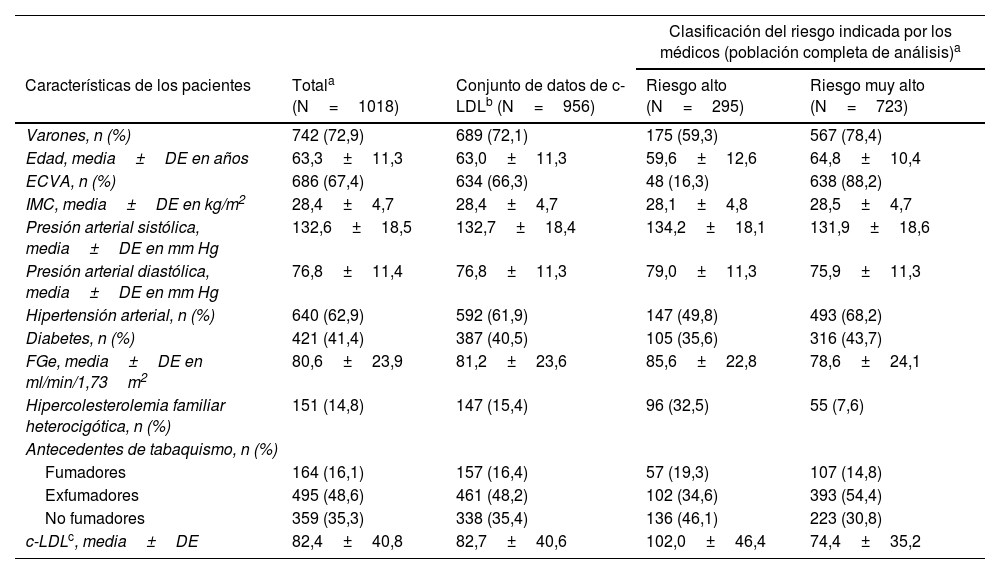
Características basales del estudio SANTORINI España en la población total, el conjunto de datos de c-LDL y en relación con la clasificación del riesgo indicada por los médicos (población completa de análisis)
| Clasificación del riesgo indicada por los médicos (población completa de análisis)a | ||||
|---|---|---|---|---|
| Características de los pacientes | Totala (N=1018) | Conjunto de datos de c-LDLb (N=956) | Riesgo alto (N=295) | Riesgo muy alto (N=723) |
| Varones, n (%) | 742 (72,9) | 689 (72,1) | 175 (59,3) | 567 (78,4) |
| Edad, media±DE en años | 63,3±11,3 | 63,0±11,3 | 59,6±12,6 | 64,8±10,4 |
| ECVA, n (%) | 686 (67,4) | 634 (66,3) | 48 (16,3) | 638 (88,2) |
| IMC, media±DE en kg/m2 | 28,4±4,7 | 28,4±4,7 | 28,1±4,8 | 28,5±4,7 |
| Presión arterial sistólica, media±DE en mm Hg | 132,6±18,5 | 132,7±18,4 | 134,2±18,1 | 131,9±18,6 |
| Presión arterial diastólica, media±DE en mm Hg | 76,8±11,4 | 76,8±11,3 | 79,0±11,3 | 75,9±11,3 |
| Hipertensión arterial, n (%) | 640 (62,9) | 592 (61,9) | 147 (49,8) | 493 (68,2) |
| Diabetes, n (%) | 421 (41,4) | 387 (40,5) | 105 (35,6) | 316 (43,7) |
| FGe, media±DE en ml/min/1,73m2 | 80,6±23,9 | 81,2±23,6 | 85,6±22,8 | 78,6±24,1 |
| Hipercolesterolemia familiar heterocigótica, n (%) | 151 (14,8) | 147 (15,4) | 96 (32,5) | 55 (7,6) |
| Antecedentes de tabaquismo, n (%) | ||||
| Fumadores | 164 (16,1) | 157 (16,4) | 57 (19,3) | 107 (14,8) |
| Exfumadores | 495 (48,6) | 461 (48,2) | 102 (34,6) | 393 (54,4) |
| No fumadores | 359 (35,3) | 338 (35,4) | 136 (46,1) | 223 (30,8) |
| c-LDLc, media±DE | 82,4±40,8 | 82,7±40,6 | 102,0±46,4 | 74,4±35,2 |
c-LDL: colesterol unido a lipoproteínas de baja densidad; DE: desviación estándar; ECVA: enfermedad cardiovascular aterosclerótica; FGe: filtración glomerular estimada; IMC: índice de masa corporal.
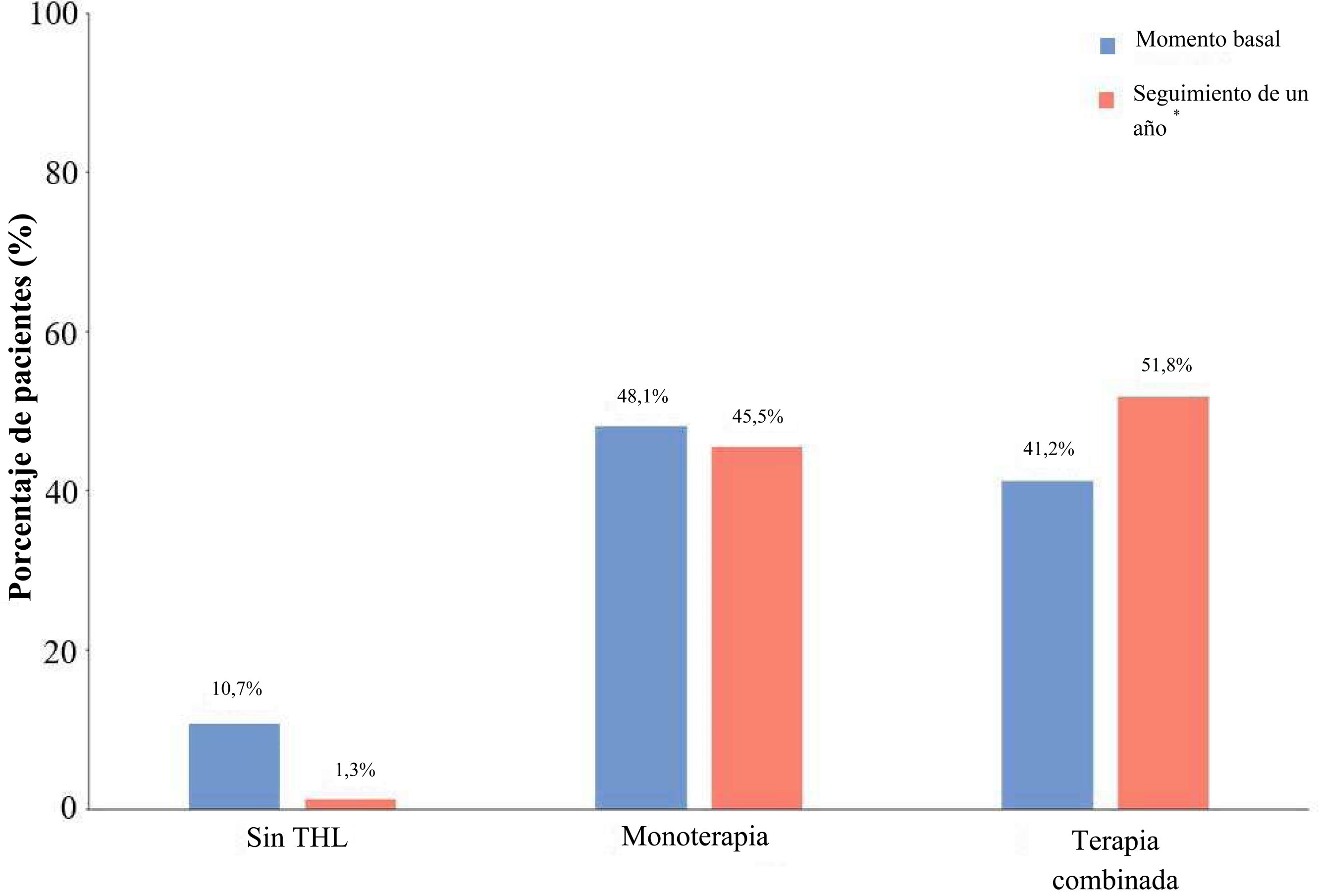
En total, el 48,1% y el 41,2% de los pacientes recibían THL en monoterapia y terapia combinada en el momento basal, respectivamente (fig. 1 y tabla 1 suplementaria). El uso de THL en monoterapia fue del 47,8% y 48,3% en los pacientes de riesgo alto y muy alto, respectivamente, mientras que el de terapia combinada fue del 40,3% y 41,5%, respectivamente. Al cabo de un año de seguimiento disminuyó ligeramente el porcentaje de uso total de THL en monoterapia (45,5%), mientras que aumentó el de terapia combinada (51,8%). En dicho momento, el uso de THL en monoterapia fue del 48,5% y 44,2% en los pacientes de riesgo alto y muy alto, respectivamente, y el de terapia combinada, del 49,5% y 52,7%, respectivamente. El incremento del uso de terapia combinada se observó principalmente en pacientes con ECVA (del 43,6% al 56,4%) y, en menor grado, en aquellos sin ECVA (del 36,1% al 42,2%; tabla 2 suplementaria). En conjunto, el 10,7% de los pacientes no recibían THL en el momento basal, porcentaje que disminuyó al 1,3% en el seguimiento al cabo de un año. Durante este período no se modificó el tratamiento en la mayoría de los pacientes (73,1%; tabla 3 suplementaria), mientras que se aumentó en el 22,4% y se redujo en el 3,1% de ellos.
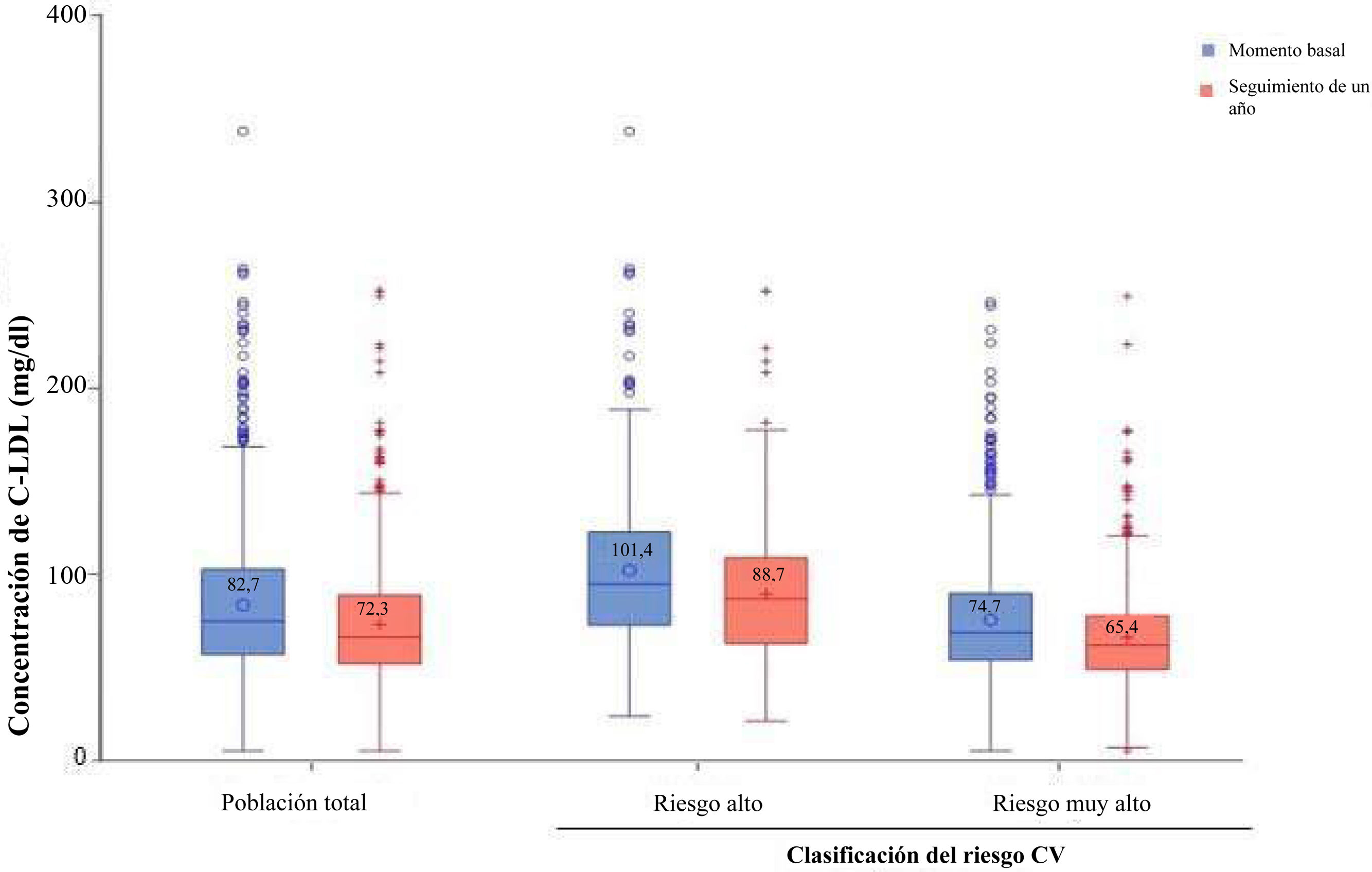
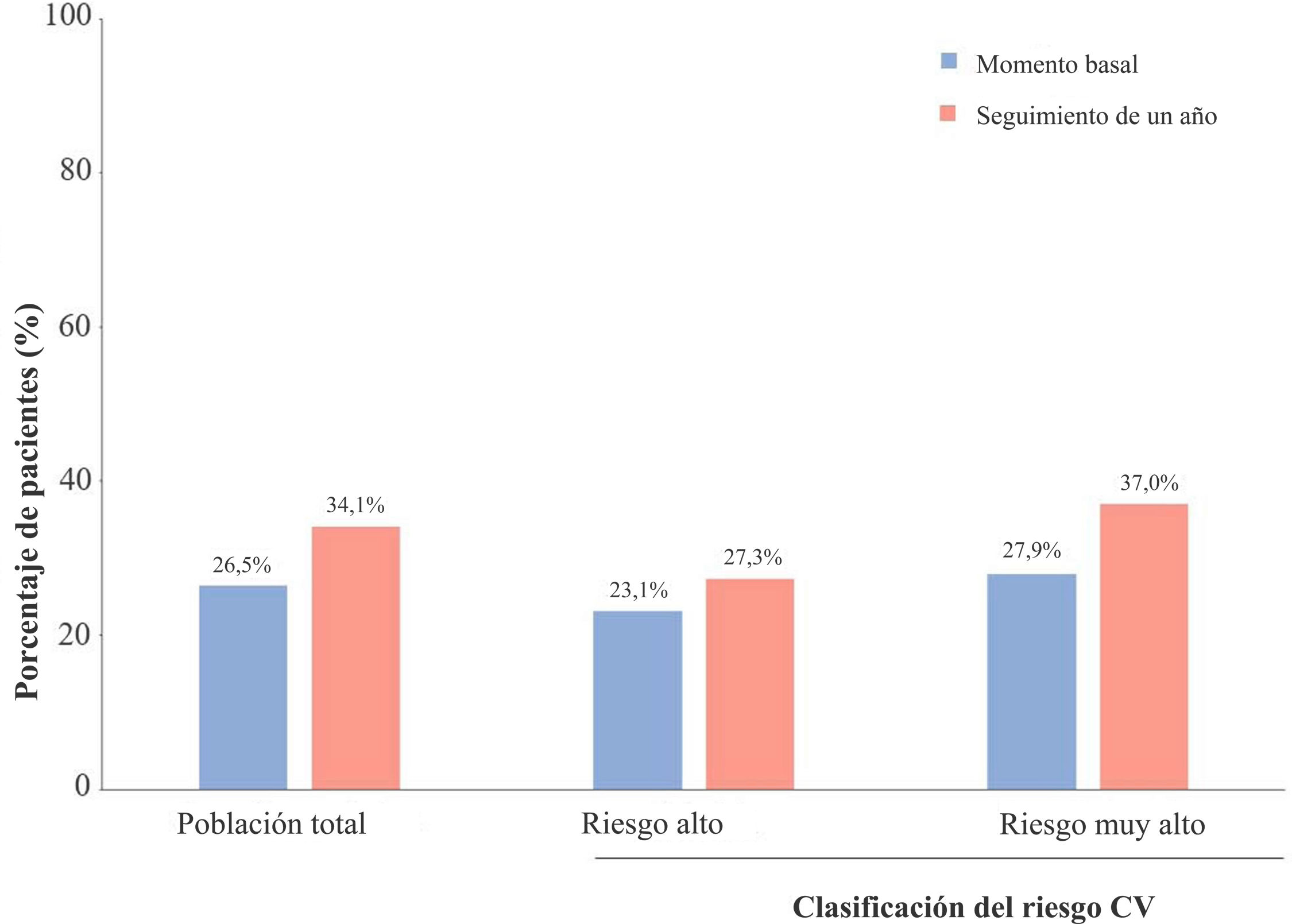
Concentraciones de c-LDL y consecución de los objetivos en SANTORINI EspañaEn general, la concentración media de c-LDL disminuyó entre el momento basal (82,7±40,6mg/dl) y al cabo de un año (72,3±32,6mg/dl), tanto en pacientes de riesgo alto (de 101,4±46,3 a 88,7±37,1mg/dl) como en los de riesgo muy alto (de 74,7±35,0 a 65,4±27,7mg/dl; fig. 2). El porcentaje de pacientes que lograron los objetivos de c-LDL según la guía ESC/EAS 2019 aumentó del 26,5% en el momento basal al 34,1% al cabo de un año, tanto en los pacientes de riesgo alto (23,1% frente al 27,3%) como en los de riesgo muy alto (27,9% frente al 37,0%; fig. 3). Este incremento fue especialmente notable en la población de pacientes que no recibían THL en el momento basal, en los que la consecución del objetivo aumentó del 8,6% en el momento basal al 32,4% al cabo de un año (fig. 2 suplementaria).
Concentración de c-LDL en SANTORINI España en el momento basal y al cabo de un año de seguimiento en la población total y en relación con la clasificación del riesgo CV indicada por los médicos (conjunto de datos de c-LDL, n=956).
c-LDL: colesterol unido a lipoproteínas de baja densidad; CV: cardiovascular.
Los valores dentro de los recuadros representan valores medios.
Consecución de los objetivos de c-LDL en SANTORINI España en el momento basal y en el seguimiento al cabo de un año en la población total y en relación con la clasificación del riesgo CV indicada por los médicos (conjunto de datos de c-LDL, n=956).
c-LDL: colesterol unido a lipoproteínas de baja densidad; CV: cardiovascular.
Durante el seguimiento fallecieron 7 pacientes por causas CV, todos ellos de muy alto riesgo (tabla 4 suplementaria). Cuarenta y seis y 24 de los pacientes presentaron al menos un MACE de 4 o 3 componentes, respectivamente. Por consiguiente, las tasas de episodios correspondieron a 0,7 (intervalo de confianza del 95% [IC del 95%]: 0,2-1,2) muertes de causa CV, 4,6 (IC del 95%: 3,3-5,9) MACE de 4 componentes y 2,4 (IC del 95%: 1,4-3,3) MACE de 3 componentes por 100 AP de seguimiento.
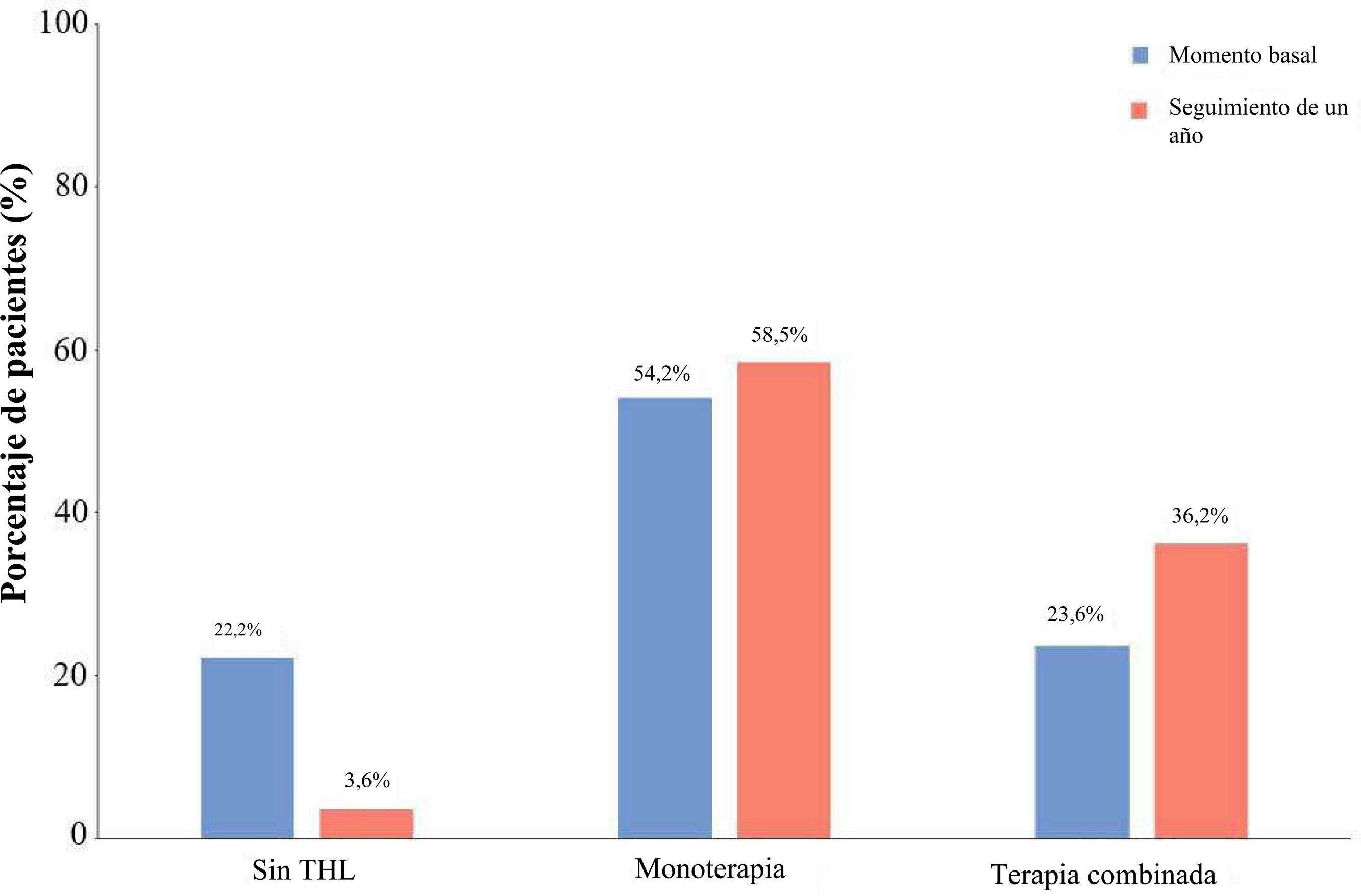
Perspectiva respecto a SANTORINI Europa sin EspañaAl presentar los datos en relación con el estudio SANTORINI Europa sin España, el uso de terapia combinada tras un año de seguimiento fue mayor en España que en Europa (51,8% frente al 36,2%; fig. 4). En los pacientes de alto riesgo, el uso de THL en monoterapia fue del 48,5% y 68,3% en España y Europa, respectivamente, mientras que el de terapia combinada fue del 49,5% y 24,1%, respectivamente (tabla 5 suplementaria). En los pacientes de muy alto riesgo, el uso de THL en monoterapia fue del 44,2% y 54,6% en España y Europa, respectivamente, mientras que el de terapia combinada fue del 52,7% y 41,1%, respectivamente.
En SANTORINI Europa sin España, la concentración media de c-LDL disminuyó de 95,2±47,8mg/dl en el momento basal a 77,4±37,1mg/dl después de un año de seguimiento (tabla 6 suplementaria). El porcentaje de pacientes que lograron sus objetivos de c-LDL aumentó del 20,4% al 30,4%. En SANTORINI Europa sin España, durante el seguimiento, 81 pacientes fallecieron por causas CV y 451 y 189 presentaron al menos un MACE de 4 o 3 componentes, respectivamente (tabla 7 suplementaria). Por tanto, las tasas de episodios correspondieron a 1,0 (IC del 95%: 0,8-1,2) muertes de causa CV, 5,7 (IC del 95%: 5,2-6,3) MACE de 4 componentes y 2,4 (IC del 95%: 2,0-2,7) MACE de 3 componentes por 100 AP de seguimiento.
DiscusiónLos presentes resultados de SANTORINI España revelan un aumento del uso de THL y del porcentaje de pacientes que lograron los objetivos recomendados de c-LDL según la guía ESC/EAS 2019 después de un año de seguimiento. Estudios de práctica clínica realizados antes de la publicación de la guía ESC/EAS 2019 ya revelaron una consecución subóptima de los objetivos de c-LDL en pacientes de riesgo alto y muy alto9–13. Al mismo tiempo, los estudios pusieron de relieve que estos pacientes no estaban recibiendo el THL más adecuado para reducir la concentración de c-LDL. En el estudio DA VINCI, llevado a cabo entre 2017 y 2018, el 63% y 39% de los pacientes de riesgo alto y muy alto, respectivamente, lograron los objetivos basados en el riesgo según la guía ESC/EAS 201612. Además, este estudio reveló que el 84% de los THL consistieron en estatinas en monoterapia, mientras que el 10% estuvo representado por la terapia combinada. Tras la actualización de 2019 de la guía ESC/EAS, muy pocos estudios han evaluado la aplicación de los umbrales más estrictos de c-LDL y el uso de THL en la práctica clínica habitual14,15. En Europa, el estudio SANTORINI mostró una variación de la consecución de los objetivos de c-LDL del 21,2% en el momento basal al 30,9% tras un año de seguimiento en los 7210 pacientes con datos completos de c-LDL16. El uso de THL en monoterapia aumentó del 53,6% al 57,1% y el de terapia combinada, del 25,6% al 37,9%. De hecho, reveló un mejor control del c-LDL en los pacientes que recibían terapia combinada. Numerosos estudios han puesto de manifiesto el uso de la terapia combinada, tanto oral (estatinas, ezetimiba y ácido bempedoico) como subcutánea (adición de inhibidores de PCSK9) para reducir sustancialmente el c-LDL, específicamente en los pacientes de máximo riesgo CV6,19–22. En los ensayos multicéntricos, aleatorizados, doble ciego y controlados con placebo FOURIER20 y ODYSSEY21, la adición de evolocumab o alirocumab al tratamiento estatínico de alta intensidad redujo el riesgo de episodios CV en un 15% durante aproximadamente 2 años. En el estudio Treat Stroke to Target se aleatorizó a 2860 pacientes con antecedentes de ictus isquémico o accidente isquémico transitorio a alcanzar una concentración de c-LDL por debajo de 70mg/dl (grupo con el objetivo más bajo) o de entre 90 y 110mg/dl (grupo con el objetivo más alto)22. El grupo con el objetivo más bajo de c-LDL tuvo un riesgo un 30% menor de sufrir un MACE posterior. Hay que destacar que el 40% de los pacientes del grupo con el objetivo más bajo de c-LDL recibieron terapia combinada con estatina más ezetimiba. Datos recientes indican además que la terapia combinada, especialmente las combinaciones en dosis fijas, logra los objetivos lipídicos y la prevención CV de manera más efectiva23,24. Además, se ha propuesto que el uso de terapia combinada desde etapas tempranas, o incluso desde el principio, aumenta el número de pacientes que logran los objetivos de c-LDL, previniendo así nuevos episodios CV y mejorando las lesiones ateroscleróticas existentes6.
Basándose en datos científicos, en las guías internacionales se recomienda el uso de terapia combinada para lograr los ambiciosos objetivos de c-LDL. A pesar de ello, según se ha mencionado ya, existe una brecha considerable entre las recomendaciones y la práctica clínica habitual en el tratamiento de dislipidemias. Por ejemplo, un análisis retrospectivo del registro SwissPR (Registro Suizo de Prevención Secundaria) en el que participaron 875 pacientes con enfermedad coronaria reveló que, tras la publicación de la guía ESC/EAS 2019, tan solo el 18% de los pacientes recibían terapia combinada con ezetimiba en el momento de incorporarse a la rehabilitación cardíaca y que al 2% se les habían prescrito inhibidores de PCSK925. Entre los obstáculos que contribuyen a la brecha entre las recomendaciones de las guías y la práctica clínica habitual figuran algunos relacionados con el médico (es decir, inercia terapéutica o percepción errónea de que se han logrado los objetivos de c-LDL) o con el sistema sanitario (como el acceso restringido a terapias combinadas o complementarias)26,27. La selección del THL más adecuado y capaz de lograr los objetivos terapéuticos desde el principio suele suponer el uso de terapia combinada como primera línea, en lugar de basarse en la estrategia escalonada tradicional, que sigue contando con el respaldo de las guías actuales sobre el tratamiento de dislipidemias5,28. Es posible que el inicio de un tratamiento basado en objetivos terapéuticos no solo facilite una consecución más rápida de los objetivos lipídicos, sino que también reduzca al mínimo la inercia terapéutica.
En la cohorte SANTORINI España, el aumento del uso del THL conllevó una disminución de las concentraciones de c-LDL en pacientes de riesgo alto y muy alto. En consecuencia, también se incrementó el porcentaje de pacientes que lograron los objetivos de c-LDL en el mismo período. Lo que resulta más interesante es que el control del c-LDL mejoró especialmente en los pacientes que no recibían THL en el momento basal (del 8,6% al 32,4%). Por el contrario, los que recibían THL en el momento basal mostraron una mejoría más moderada del control del c-LDL, lo cual se observó únicamente en los que cambiaron a terapia combinada. A pesar de ello, en la mayoría de los pacientes (73,1%) de nuestro estudio no se modificó el THL durante el seguimiento. Esta observación concuerda con estudios previos y pone de manifiesto que la optimización del THL a menudo solamente supone un aumento de la dosis de estatinas6,7,16. Curiosamente, en un estudio checo en el que se evaluó la adherencia de los cardiólogos a las guías clínicas, los autores constataron que, hasta en el 61,5% de los pacientes de muy alto riesgo CV que no lograron sus objetivos de c-LDL, sus cardiólogos expresaron su satisfacción con los resultados terapéuticos y optaron por no modificar el tratamiento7.
En comparación con SANTORINI Europa16, el porcentaje global de pacientes que lograron los objetivos de c-LDL tras un año de seguimiento fue numéricamente mayor en España (34,1% frente al 30,4% en Europa). Sin embargo, en España fue menor en los pacientes de alto riesgo (27,3% frente al 31,6%), pero mayor en los de muy alto riesgo (37,0% frente al 30,0%). La menor consecución de los objetivos en pacientes de alto riesgo de España contrasta con el hecho de que un mayor porcentaje de dichos pacientes utilizaba terapia combinada. Esta observación podría atribuirse a un mayor porcentaje de pacientes incluidos con hipercolesterolemia familiar en España (15,4% frente al 10,4% en Europa) o deberse posiblemente a diferencias en la clasificación del riesgo CV entre España y Europa16.
Una limitación del estudio podría derivar del sesgo de selección potencial inherente a los estudios observacionales. Los centros participantes, frecuentemente más experimentados, podrían mostrar el mejor de los casos. Además, no se tuvo en cuenta la reducción del 50% del c-LDL con respecto al valor basal para evaluar la consecución de los objetivos de c-LDL. Dada la naturaleza no intervencionista del estudio, no se contrastaron hipótesis formales, por lo que las conclusiones deben ser consideras con cautela. A pesar de estas limitaciones, éste es el primer estudio prospectivo que proporciona un panorama actualizado del control de los lípidos y la consecución de los objetivos de c-LDL en los pacientes con el mayor riesgo CV en España tras la publicación de la guía ESC/EAS 2019. Además, presenta datos relativos a una amplia cohorte de pacientes con concentraciones de c-LDL disponibles tanto en el momento basal como al cabo de un año.
ConclusionesLos datos de un año de seguimiento de SANTORINI España muestran que el uso de THL aumentó con respecto al momento basal, tanto en monoterapia como en terapia combinada. A pesar de las recomendaciones, los pacientes con mayor riesgo CV siguen sin recibir el THL más adecuado para reducir la concentración de c-LDL en la práctica clínica habitual. En las futuras guías sobre el tratamiento de la dislipidemia debería recomendarse adaptar el THL inicial a la magnitud de la reducción del c-LDL necesaria para lograr antes los objetivos terapéuticos y reducir la inercia terapéutica.
FinanciaciónEste estudio fue financiado por Daiichi Sankyo Europe GmbH, Múnich, Alemania. La asistencia en la redacción médica ha sido proporcionada por Evidenze Health España S.L.U. y financiada por Daiichi Sankyo Europe.
Conflicto de interesesJMM declara que ha recibido honorarios por consultoría de Daiichi Sankyo, Novartis y Sanofi; pagos/honorarios de Daiichi Sankyo, Amgen, Novartis, Servier, Sanofi, Ferrer y Viatris; y apoyo para asistir a reuniones de Daiichi Sankyo. CL declara honorarios por consultoría de Daiichi-Sankyo, Amarin, Alter, Novartis y Sanofi. MGdYC ha desempeñado un rol de asesoría u orador para Daiichi Sankyo. NP declara honorarios por consultoría (orador) para Sanofi, Amgen y Ferrer. ALC declara que ha recibido becas/contratos de Amryt Pharma, Menarini, y Ultragenyx; y pagos/honorarios de Amarin Amgen Amryt Pharma, Astrazeneca, Daiichi Sankyo, Esperion Ionis Pharmaceutical Medscaper, Menarini, Merck, Novartis, NovoNordisk, Peervoice Pfizer Recordati Regeneron, Sandoz, Sanofi The Corpus, Ultragenyx, y Viatris. GDM es empleada de Daiichi Sankyo. KKR declara que ha recibido apoyo editorial de Springer financiada por Daiichi Sankyo Europe; consultoría de Daiichi para el desarrollo del plan del análisis estadístico, protocolo, supervisión como IP; becas/contratos de Amgen, Daiichi Sankyo, Sanofi, Regeneron y Ultragenyx; honorarios por consultoría de Abbott Laboratories, Amgen, AstraZeneca, Bayer Healthcare Pharmaceuticals, Boehringer Ingelheim, Cargene, CRISPR, Daiichi Sankyo, Eli Lilly Company, EmendoBio, Esperion, Kowa, New Amsterdam Pharma, Novartis Corporation, Nodthera, GSK, Novo Nordisk, Pfizer, Regeneron, Sanofi, SCRIBE, Silence Therapeutics y VAXXINITY; pagos/honorarios de Novartis, Daiichi Sankyo, Novo Nordisk, Amgen, Sanofi y Boehringer Ingelheim; y opciones sobre acciones de New Amsterdam Pharma, Scribe, Pemi31. También es presidente de EAS. JMRC, EV, AIG, JFD, NP, MR-M, JdDG-D, FMD e IPdP declaran no tener conflictos de interés.
El trabajo de ALC está apoyado por la subvención Ricerca Corrente del Ministerio de Salud a Multimedica IRCCS.