La osteoporosis es un trastorno de elevada prevalencia. La SEIOMM publicó en 2022 unas guías de manejo de estos pacientes. La reciente comercialización en Europa de un nuevo fármaco, la abaloparatida, hace aconsejable considerar su papel dentro de las opciones terapéuticas.
Objetivo y resultadosEn este artículo se resume la información existente sobre la eficacia y la seguridad de la abaloparatida y se actualizan los algoritmos terapéuticos propuestos en la guía.
ConclusiónLa abaloparatida es un fármaco osteoformador con eficacia y seguridad similares a la teriparatida. Representa una nueva opción en el tratamiento de la osteoporosis grave con muy alto riesgo de fractura.
Osteoporosis is a highly prevalent condition. SEIOMM has published guidelines for managing these patients in 2022. The recent introduction of a new drug in Europe, abaloparatide, makes it advisable to consider its role among therapeutic options.
Objective and resultsThis article summarizes the existing information on the efficacy and safety of abaloparatide and it updates the therapeutic algorithms proposed in the guidelines.
ConclusionAbaloparatide is an osteoanabolic drug with efficacy and safety similar to teriparatide. It represents a new option for treating patients with severe osteoporosis and a very high risk of fracture.
Después de la publicación de las guías de manejo de la osteoporosis de la Sociedad Española de Investigación Ósea y del Metabolismo Mineral (SEIOMM) en 20221, se ha aprobado la comercialización de la abaloparatida en España y otros países europeos. Esto aumenta el número de fármacos osteoformadores disponibles para el tratamiento de la osteoporosis y hace conveniente una actualización de dichas guías. A tal fin, el grupo de trabajo que elaboró las guías ha evaluado los estudios disponibles acerca de la eficacia y seguridad de la abaloparatida y su papel dentro de los esquemas de tratamiento propuestos. Para ello, el comité designado por la SEIOMM revisó la literatura existente sobre la abaloparatida y elaboró un borrador que fue después sometido a la discusión por el resto de la Comisión de redacción de las guías (Anexo). Se exponen aquí sus conclusiones de forma resumida.
La abaloparatida es un péptido sintético análogo de los 34 primeros aminoácidos del péptido humano relacionado con la hormona paratiroidea (PTHrP) que pertenece al grupo de agentes osteoanabólicos. Actúa a través de la activación del receptor1 de la PTH (PTH1R), favoreciendo la diferenciación de los precursores osteoblásticos e inhibiendo la apoptosis de los osteocitos. La activación del PTH1R en esas células también induce la expresión del ligando del receptor activador del factor nuclear kappa-B (RANKL), de modo que indirectamente estimula la osteoclastogénesis. Desde el punto de vista mecanístico, la abaloparatida se diferencia de la teriparatida en su mayor afinidad por la unión a la conformación RG del PTH1R, lo que hace que la respuesta intracelular sea menos duradera que cuando la activación se realiza a través de la conformación R0, que es la que utiliza la teriparatida. Se ha sugerido que ello se traduciría en una menor inducción de la producción de RANKL y resorción ósea por la abaloparatida2. Este fármaco se administra por vía subcutánea, a dosis de 80μg/día, durante un máximo de 18meses.
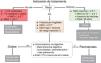
Efecto sobre la densidad mineral ósea (DMO) y las fracturasLa eficacia de la abaloparatida en mujeres posmenopáusicas con osteoporosis se evaluó en el ensayo ACTIVE, que comparó el tratamiento con abaloparatida frente a placebo3. Asimismo, se comparó con una rama abierta de mujeres tratadas con teriparatida. Después de 18meses de seguimiento, en comparación con el placebo, la abaloparatida redujo el riesgo de fracturas vertebrales (riesgo relativo [RR]: 0,14; IC95%: 0,05-0,39). También disminuyó el riesgo de fracturas osteoporóticas mayores (hazard ratio [HR]: 0,30; IC95%: 0,15-0,60), de fracturas clínicas (HR: 0,57; IC95%: 0,35-0,91) y de fracturas no vertebrales (HR: 0,57; IC95%: 0,32-1,0; p=0,049). Por tanto, se considera indicada para el tratamiento de la osteoporosis en mujeres posmenopáusicas que presentan un elevado riesgo de fractura (fig. 1).
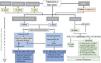
Asimismo, la abaloparatida aumentó la DMO en todas las localizaciones, en torno al 8-11% en la columna y el 3-4% en la cadera, en comparación con el placebo. El estudio ATOM mostró ganancias en DMO también en hombres4, pero no cuenta de momento con aprobación para la osteoporosis del varón en Europa. Al igual que con otros osteoformadores, tras finalizar el tratamiento con abaloparatida se aconseja administrar un antirresortivo (un bisfosfonato generalmente), lo que mantiene la reducción del riesgo de fractura5 (fig. 2).
Efectos adversosLa abaloparatida es un fármaco generalmente bien tolerado. Los efectos adversos señalados con mayor frecuencia son náuseas, cefalea, artralgias, cambios en la presión arterial (hipertensión y, especialmente, hipotensión ortostática), taquicardia, palpitaciones, hiperuricemia, hipercalcemia e hipercalciuria. No suelen obligar a suspender el tratamiento6. No obstante, dada la posibilidad de hipotensión ortostática, se recomienda en la ficha técnica que las primeras dosis se administren bajo la supervisión de un profesional sanitario. Por último, este fármaco se considera contraindicado en pacientes con riesgos conocidos de osteosarcoma, como los que han recibido radioterapia, y en los que tienen neoplasias con afectación esquelética.
Comparación de abaloparatida con otros anabólicosEn cuanto a la DMO, en el estudio ACTIVE la abaloparatida y la teriparatida tuvieron un efecto similar en la columna lumbar, pero a nivel de la cadera el incremento fue algo mayor con la abaloparatida (diferencia 0,8% a los 6meses, p<0,001), al parecer a expensas de un mayor efecto sobre el hueso cortical3.
Al igual que la teriparatida, la abaloparatida induce un aumento de los marcadores de formación ósea. Al cabo de 2-3meses se observa también un incremento de los marcadores de resorción. El incremento en ambos tipos de marcadores es menor con abaloparatida que con teriparatida.
Solo en el estudio ACTIVE se llevó a cabo una comparación directa de la abaloparatida con otro osteoformador. Cuando se compararon los efectos antifractura de la abaloparatida frente a la teriparatida, se observó que ambos tratamientos eran generalmente equiparables en la reducción de la incidencia de fracturas vertebrales, fracturas no vertebrales y fracturas clínicas, pero la abaloparatida resultó ser superior en la reducción de fracturas osteoporóticas mayores (1,5% vs 3,1%, p=0,03)3. En la misma línea, dos estudios «de vida real» realizados a partir de la misma base de datos americana han sugerido que la abaloparatida reduce el riesgo de fracturas periféricas algo más que la teriparatida. Aunque se hicieron ajustes por diversas características clínicas (propensity score), su carácter retrospectivo y no aleatorizado supone una importante limitación7,8.
Dado que los datos derivados de comparaciones directas son muy limitados, varios metaanálisis «en red» han tratado de comparar los efectos de diversos osteoformadores. Los resultados no revelan de manera consistente diferencias entre los efectos de teriparatida, abaloparatida y romosozumab sobre el riesgo de fractura9-13.
En cuanto a los efectos secundarios, en el estudio ACTIVE, abaloparatida y teriparatida mostraron un perfil similar. Si bien la frecuencia de hipercalcemia fue algo mayor con teriparatida (6,4% frente al 3,4%), la frecuencia de efectos adversos que llevaron a la suspensión del tratamiento fue algo mayor en el grupo tratado con abaloparatida (9,9 frente al 6,8%).
Por tanto, la abaloparatida y la teriparatida son fármacos con perfiles de eficacia antifractura y seguridades similares. Aunque pueden ocasionar cambios en la presión arterial en algunos pacientes, no se asocian a efectos graves y ambos se consideran seguros desde el punto de vista cardiovascular14. Además de las contraindicaciones específicas, debe valorarse cuidadosamente su empleo en pacientes con historia de tumores (como los de mama, pulmón o próstata), con elevada tendencia a metastatizar en hueso.
FinanciaciónEste trabajo no ha recibido financiación de ninguna entidad pública o privada.
Conflicto de interesesLos autores declaran haber recibido pagos por conferencias, bolsas de viaje o becas de investigación de: Amgen, UCB, Lilly, Merck, Gedeon Richter, Theramex, Stada y Angelini Pharma.
Los miembros de la Comisión de Redacción de las Guías de Osteoporosis de la SEIOMM se presentan en el Anexo.
Este artículo ha sido elaborado conjuntamente por Revista Clínica Española, Revista Clínica Española (edición en inglés), Revista de Osteoporosis y publicado conjuntamente por Elsevier España S.L.U.. Los artículos son idénticos salvo pequeñas diferencias de estilo y ortografía acordes con el estilo de cada revista. Se puede utilizar cualquiera de las dos referencias para citar este artículo.