Introducción
El manejo del paciente neutropénico es sumamente delicado y comporta tener resueltos dos tipos de problemas. El primero supone tener disponibles guías clínicas suficientemente claras para tratarles cuando se infectan, y el segundo procurar, dentro de lo posible, que no se infecten; esto es: hacer profilaxis antimicrobiana de sus potenciales infecciones. El primer objetivo, el de tratarles cuando acuden con fiebre, estuvo y está sometido a cambios tanto en el plano epidemiológico como puramente diagnóstico y terapéutico. Señalemos, sintéticamente, algunos de estos cambios.
Desde el punto de vista epidemiológico han cambiado notablemente las cosas respecto a décadas anteriores. En efecto, las infecciones por grampositivos se han incrementado mucho, siendo algunos de ellos resistentes a los glucopéptidos, tema altamente preocupante. Y no tiene menos importancia, por su gravedad, la bacteriemia producida por el estreptococo del grupo viridans. Tratando de sintetizar los cambios epidemiológicos, por lo que a las bacterias se refiere, podría decirse que desde la década de 1960 hasta la de 1980 los gramnegativos eran los responsables de la mayoría de las infecciones en pacientes neutropénicos, en particular los siguientes gérmenes: Pseudomonas aeruginosa, Escherichia coli, Klebsiella spp. y Proteus spp. Pero a mediados de la década de 1980 la flora infectante cambió, aumentando las infecciones por grampositivos hasta representar el 70% de las bacteriemias monomicrobianas, y no sólo esto, pues paralelamente al aumento de infecciones por grampositivos se ha constatado un descenso en el número de infecciones producidas por los gramnegativos señalados y han aparecido otros gramnegativos que plantean resistencia a antibióticos 1,2. Las razones que se han esgrimido para este cambio son las siguientes: uso generalizado de catéteres tanto a corto como a largo plazo, profilaxis antibacteriana inadecuada con escasa cobertura de grampositivos, mayor duración de la neutropenia, regímenes de quimioterapia agresivos que al margen de provocar prolongadas e intensas neutropenias causan mucositis graves y, finalmente, supresión frecuente de la acidez gástrica (tabla 1).
Pero los cambios epidemiológicos no sólo han afectado a las bacterias, sino a otros gérmenes como los hongos y los virus. Los hongos patógenos más comunes siguen siendo Candida spp. y Aspergillus spp., pero en los últimos años están emergiendo otros hongos filamentosos y levaduriformes 3, y si de nuevos hongos hablamos también hay que añadir a la vista de los virus nuevos agentes víricos causantes de cuadros clínicos variados, algunos de ellos de localización respiratoria y de extrema gravedad 5.
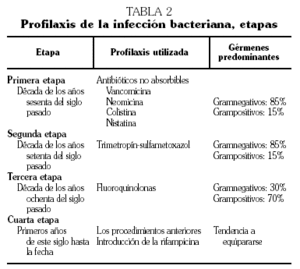
Pese a esta ampliación de los agentes antiinfecciosos y a los cambios cualitativos señalados, más del 50% de los cuadros infecciosos padecidos por los pacientes neutropénicos no llegan a aclararse etiológicamente. Ello quiere decir que en esa brecha existe un amplísimo camino abierto a la investigación microbiológica. Si bien todos estos cambios epidemiológicos son importantes, el más llamativo, cuando menos, es el incremento de las infecciones por grampositivos, ya comentado en líneas atrás (tabla 2).
El diagnóstico tanto clínico como intrumental y bacteriológico también ha sufrido notables cambios con el paso del tiempo. La tomografía axial computarizada (TAC), la resonancia magnética nuclear (RNM), la punción-aspiración con aguja fina (PAAF), la endoscopia y otras técnicas diagnósticas permiten explorar lugares de la economía a los que en el pasado reciente no se podía acceder.
Y en el ámbito del tratamiento propiamente dicho también se ha progresado notablemente en el caso de los pacientes neutropénicos. Por un lado, el desarrollo de nuevos antibacterianos, antifúngicos y antivíricos ha ampliado mucho la posible oferta terapéutica, y por otro, la masiva entrada en el mercado de los denominados «factores estimulantes de la hemopoyesis» permiten recuperar pacientes que en el pasado resultaba imposible. A ello deben añadirse las técnicas de «trasplante alogénico» y «autotrasplante» en sus diversas variedades.
Indudablemente, los avances no van a terminar aquí, y en ciernes están nuevos hitos en el manejo de estos pacientes, tales como la revitalización muy selectiva de la «transfusión de granulocitos», «el empleo de citocinas» y otros procederes 6,7.
Profilaxis antimicrobiana de la infección en el paciente neutropénico
La profilaxis antimicrobiana de la infección en el paciente neutropénico es una utopía deseada durante décadas y cuyos frutos maduros no ha sido posible aún conseguir porque, en efecto, la administración de quimioterápicos e inmunosupresores conduce a una neutropenia intensa y a efectos de la inmunidad celular con una morbimortalidad por infección más que notable y, lo que es importante, ningún método profiláctico con antimicrobianos ha conseguido mitigar el riesgo de infección de una manera radicalmente eficaz.
La historia de la profilaxis de la infección en pacientes neutropénicos ya es larga y está presidida por dos estrategias: por un lado, el aislamiento del paciente y la higiene del medio ambiental, y por otro, la administración de antibióticos o antimicrobianos con cáracter profiláctico, tema este controvertido aún hoy. Desde antiguo sabemos que los pacientes neutropénicos se autoinfectan con gérmenes de su flora endógena y gastrointestinal; flora endógena que puede ser síntesis de los propios gérmenes y de los que el paciente ha ido atrapando del ámbito hospitalario, de familiares, de otros pacientes, del personal sanitario, del agua y de los alimentos, y también sabemos desde antiguo que las posibilidades de infección de un neutropénico dependen además de otras variables, tales como la patología de base del paciente, la toxicidad intrínseca del tratamiento quimioterápico recibido y la duración de la neutropenia; del mismo modo también sabemos que la eficacia de las pautas de profilaxis antimicrobiana usadas históricamente depende, entre otras, de estas variables: el número de infecciones documentadas, el número de episodios febriles, el tiempo trascurrido entre la aparición de la neutropenia y el inicio de la fiebre 8,9; veamos qué se hizo y qué se está haciendo en la actualidad en la profilaxis antimicrobiana en este grupo de pacientes.
Profilaxis de la infección bacteriana
Cronológicamente los hechos se desenvolvieron de este modo. En la década de los años sesenta del siglo pasado se comenzaron a utilizar antibióticos orales no absorbibles para conseguir una descontaminación intestinal; los más utilizados eran éstos: vancomicina, neomicina, colistina, nistatina y otros. En la década de los setenta del siglo pasado se comenzó a utilizar el trimetopim-sulfametoxazol; este preparado eliminaba la flora intestinal, excepto los anaerobios. En la década de los ochenta/noventa del mismo siglo se utilizaron la fluoroquinolonas más que los preparados anteriores. Y, recientemente, por el incremento de las infecciones por grampositivos se ha comenzado a utilizar la rifampicina como antibiótico profiláctico.
No nos parece razonable incluir aquí un largo debate bibliográfico sobre todos los intentos de profilaxis antimicrobiana de la infección bacteriana en pacientes neutropénicos. A modo de resumen podríamos decir lo siguiente:
1) Los trabajos realizados son muy heterogéneos en sus líneas maestras, de ahí que al no ser comparables sea muy difícil extraer de ellos recomendaciones claras 10.
2) El uso de trimetropim-sulfametoxazol cada día es menor por dos razones: la falta de evidencia de un beneficio claro y su toxicidad tanto medular como cutánea. Sin embargo, hemos constatado que los hematólogos españoles siguen utilizando este fármaco con fines profilácticos con bastante profusión 11.
3) La utilización de fluoroquinolonas también está en entredicho. Por un lado, no está claro su beneficio, y por otro, los numerosos casos de resistencia que producen inducen a limitar o suspender su empleo 12.
Queda, por tanto, claro que la tendencia actual es la de suprimir la profilaxis antibiótica en los pacientes neutropénicos por su dudosa eficacia y por la creación de resistencias, así como por el incremento de las infecciones por grampositivos.
Profilaxis de las infecciones víricas
Prescindimos de nuevo de una larga confrontación bibliográfica para centrarnos en varias conclusiones prácticas extraídas de la literatua universal 13,14. Serían éstas:
1) Las infecciones víricas respiratorias tienen un patrón de infección igual que en sujetos sanos, pero en los pacientes neutropénicos pueden ser muy graves y de curso fatal. Por ello, ante un estado catarral de naturalez vírica debe demorarse el tratamiento citostático 15.
2) Existen situaciones en las que la profilaxis de la infección vírica es recomendable y hasta obligado. Destacamos éstas:
a) Virus del herpes simple. Las infecciones viricas tienen mucha importancia en los pacientes seriamente inmunocomprometidos. En este sentido, los pacientes sometidos a TPH quizás sean los más desamparados frente a este riesgo. Por ello aquellos que sean seropositivos para el virus del herpes simple deberán hacer profilaxis con aciclovir.
b) Citomegalovirus. En pacientes seronegativos pre-alotrasplante existen dos estrategias profilácticas; a saber: la primera es hacer profilaxis en todos los pacientes seropositivos con ganciclovir o foscarnet y la segunda es preventiva y consiste en dar sólo tratamiento con los agentes señalados a sólo a aquellos pacientes en quienes se demuestra una infección por citomegalovirus antes de que aparezca la enfermedad.
c) Virus sincitial respiratorio. También, como podrá observarse, son escasas las situaciones en las que se realiza profilaxis de la infección vírica.
Profilaxis de las infecciones fúngicas
Sobre este asunto suscitamos dos cuestiones puntuales: la profilaxis frente al género Candida y la profilaxis frente a Aspergillus.
1) Profilaxis frente a Candida. Otras cuestiones que se plantean son: a) no existe evidencia que la profilaxis con fluconazol aporte beneficio alguno fuera del alotrasplante; b) en el alotrasplante, sí se ha reconocido beneficio, siendo recomendables las siguientes dosis de fluconazol: 400 mg/día. La tendencia, sin embargo, es a dar 100-200 mg/día, y c) la instauración de una pauta de profilaxis en un paciente con neutropenia puede justificarse ante la existencia, fundamentalmente, de uno de estos factores: aislamiento de Candida spp. en dos o más mucosas; aislamiento de C. tropicalis en una mucosa; candiduria y antecedentes de candidiasis hepatoesplénica crónica 16.
2) Profilaxis frente al Aspergillus. Al respecto deben recordarse o suscitarse sustancialmente estas ideas: a) Riesgo. Los pacientes con antecedentes de infección por Aspergillus tienen un riesgo del 50% de que se reactive si reciben quimioterapia. Sin embargo, no empeora su pronóstico si la infección está controlada y bajo tratamiento durante todo el período en que el paciente esté neutropénico y, por tanto, con riesgo 12. b) Colonización. No existe un protocolo profiláctico establecido para la infección del Aspergillus. Sin embargo, si existe colonización por este hongo, el riesgo de enfermedad invasiva grave se incrementa en un 50%-80%. Por ello la colonización debe tratarse como factor de riesgo de enfermedad invasiva. El «itraconazol» oral es considerado el fármaco ideal para esta indicación y su nueva fórmulación oral con ciclodextrina puede resultar más eficaz 2.
c) Los factores de riesgo de infección por Aspergillus son la neutropenia prolongada, la enfermedad injerto contra húesped grave (grado >= 2) o crónica extensa y el tratamiento con dosis de corticosteroides superiores a 20 mg/día 17.
Profilaxis de Pneumocistitis carinii
Las cuestiones más claras en torno a este tema creemos que son las siguientes:
1) Paciente más expuesto. Los pacientes más expuestos al Pneumocystis carinii y en quienes debe hacerse profilaxis son los siguientes: pacientes sometidos a TPH, pacientes afectos de leucemia aguda linfoblástica a tratamiento quimioterápico que incluye dosis altas de corticoides y pacientes tratados con analógos de las purinas solas o en combinación 18.
2) Fármaco ideal. El fármaco ideal para hacer profilaxis es el trimetropim-sulfametoxazol cada 12 horas 2-3 días por semana.
3) Otros fármacos. Los pacientes que no toleran el fármaco anterior pueden beneficiarse de la toma de pentamidina inhalada o dapsona aunque su efectividad no esté suficientemente estudiada en estos pacientes 19.
Hemos desarrollado hasta aquí las cuestiones más importantes relacionadas con la profilaxis antimicrobiana de la infección en pacientes neutropénicos, bien producida por bacterias, virus, hongos o parásitos. Las conclusiones a las que puede llegarse tras este esquemático texto son las siguientes.
Conclusiones
1) No está demostrada la utilidad de la profilaxis antibacteriana. Los problemas asociados a ella hacen que se la cuestione seriamente.
2) La profilaxis de infección virica, fúngica y por P. carinii posee unas indicaciones muy precisas.
Resumen
En este breve trabajo de revisión se analiza, a la luz de la literatura actual, el papel que desempeña la profilaxis antimicrobiana en el paciente neutropénico. Se exponen sucesivamente estas cuestiones: la profilaxis de la infección bacteriana, la de las infecciones víricas, la de las infecciones fúngicas y, finalmente, la profilaxis del Pneumocystis carinii. La conclusión general más importante es que la profilaxis antimicrobiana en el paciente neutropénico tiene unas indicaciones muy limitadas, unas veces por no ser claro el beneficio que se desea obtener y otras por la alta probabilidad de crear resistencias bacterianas.