Introducción
Por quimioprevención del cáncer se entiende la intervención farmacológica orientada a impedir o enlentecer el proceso carcinogénico, con el objetivo de evitar o demorar la aparición del cáncer clínicamente detectable. El período de tiempo transcurrido entre la iniciación y la etapa en que un cáncer alcanza el volumen suficiente como para ser diagnosticado por medios clínicos se ha estimado en varias décadas, lo que permite tomar medidas quimiopreventivas. La investigación de laboratorio nos ha proporcionado una lista creciente de sustancias con potencial quimiopreventivo como vegetales, inhibidores de la síntesis de poliaminas, retinoides, antiinflamatorios no esteroideos (AINE) y sus más recientes sucesores, los inhibidores de la ciclooxigenasa (COX-2) denominados COXIB. En esta revisión tratamos sobre este grupo de fármacos, dado que la mejora de su índice terapéutico en comparación a los AINE ha incrementado notablemente el interés en el bloqueo de la COX-2 como estrategia farmacológica para la quimioprevención del cáncer humano 1-4. La necesidad de incluir la quimioprevención como estrategia para reducir la mortalidad por cáncer es patente cuando se consideran las limitaciones del diagnóstico precoz mediante cribado de la población y el tratamiento del cáncer con los medios actuales 5. Las consideraciones éticas que plantea la actividad preventiva han sido tratadas con la extensión y profundidad que la complejidad del tema merece en una revisión específica 6, por lo que nos centraremos en la vertiente biológica del tema.
Prostaglandinas, ciclooxigenasa-2 y proceso carcinogénico
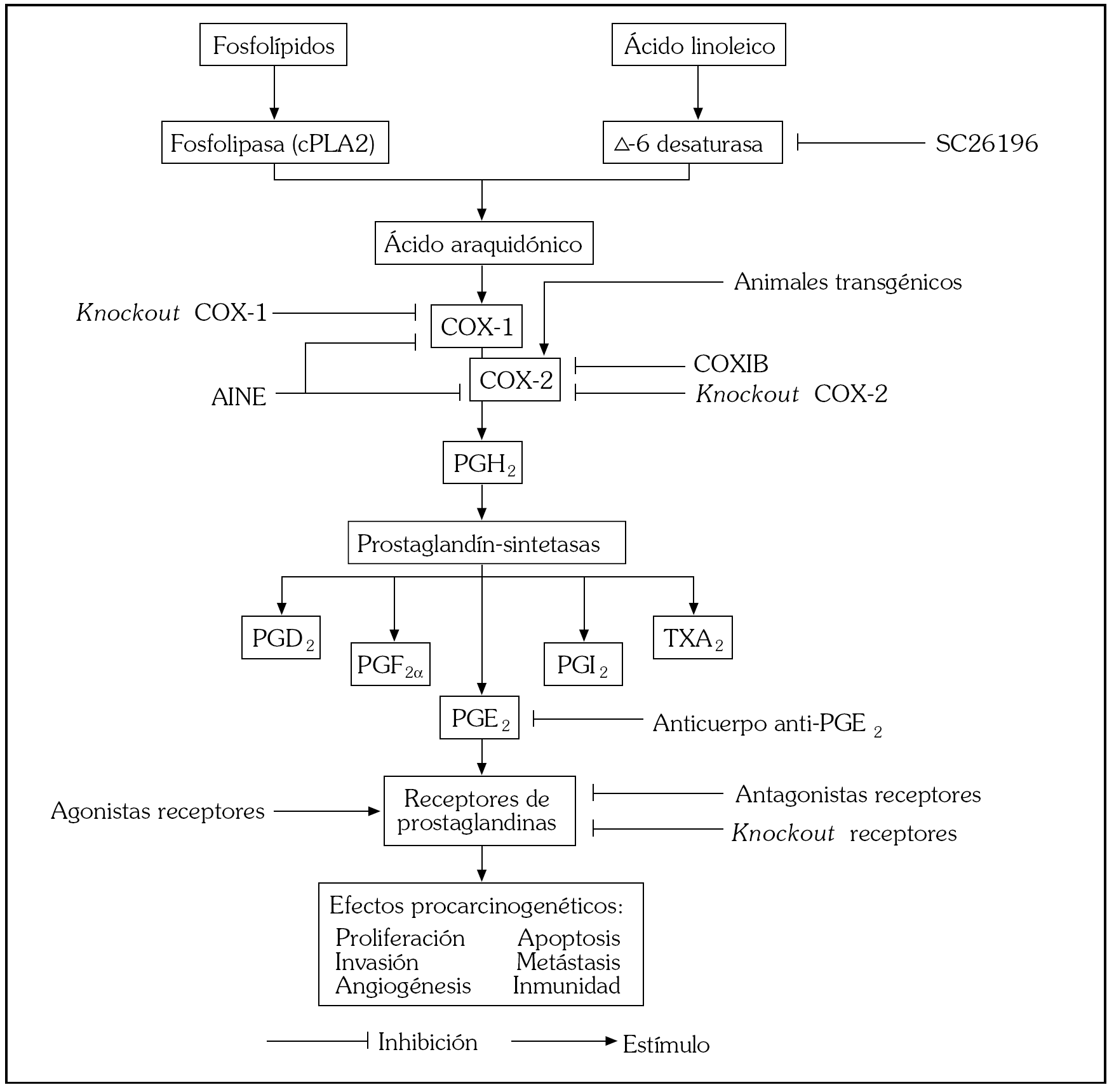
Las observaciones pioneras que relacionaron prostaglandinas (PG) y cáncer se basaron en el hallazgo de concentraciones intratumorales de estas sustancias mayores que en el tejido sano circundante 7. Las PG desempeñan en el proceso carcinogénico un papel promotor, ya que la reducción de sus niveles se asocia a una disminución de la carcinogénesis y por el contrario su incremento sostenido se asocia a un efecto facilitador de la aparición de tumores. En la figura 1 se muestra la vía metabólica de la síntesis de prostaglandinas y sus efectos sobre el proceso carcinogénico, con los diferentes pasos intermedios que pueden ser interferidos mediante manipulaciones genéticas o farmacológicas. El ácido linoleico es un precursor dietético del ácido araquidónico (AA), conversión que se realiza por la acción de la enzima -6-desaturasa. Cuando la acción de esta enzima es bloqueada por el inhibidor específico SC-26196, se produce una disminución de los niveles tisulares del AA y su correspondiente incremento en los niveles de ácido linoleico, lo que conlleva una reducción del orden del 35% de la incidencia de tumores intestinales en dos modelos murinos, y puede evitarse añadiento AA en la dieta 8. La actividad enzimática crucial para la vía metabólica de las PG es la COX, ya que su actividad resulta limitante para la tasa de síntesis de los productos finales. De las dos isoformas de la COX, la COX-2 es la que desempeña un papel más importante en la etiopatogenia del cáncer 1-4. La sobreexpresión de COX-2 es suficiente para inducir cáncer de mama en ratones transgénicos. La inclusión de un promotor vírico en el gen de la COX-2 en las glándulas mamarias murinas indujo una alta incidencia de hiperplasia, displasia y carcinomas infiltrantes y metastatizantes que junto a la sobreexpresión de COX-2 mostraban una disminución de las proteínas proapoptóticas Bax y Bcl-xL junto a un incremento de la proteína antiapoptótica Bcl-2 9.
Fig. 1. Prostaglandinas y carcinogénesis. La inhibición farmacológica o genética en diferentes localizaciones de la vía de señalización de las prostaglandinas se asocia a una disminución de la carcinogénesis mientras que el estímulo sostenido facilita el proceso.
Hay otros ejemplos en los que la COX-2 se ve activada por los diversos oncogenes: cáncer de mama HER-2 positivo y poliposis adenomatosa familiar (PAF) 10,11. Para investigar si en este caso la COX-2 era funcionalmente importante se confirmó su expresión en un modelo murino de cáncer de mama generado por la transfección del gen neu (equivalente murino del HER humano), y a continuación se exploró el posible valor quimiopreventivo del celecoxib administrado durante el proceso de la carcinogénesis mamaria. Se observó una reducción del 50% en los niveles mamarios de prostaglandina (PGE2) que correlacionaba con una disminución en la incidencia de tumores mamarios 12. Por otro lado, PAF representa un modelo acelerado de esta secuencia carcinogenética, ya que se nace con un alelo mutado del gen APC (Adenomatous Polyposis Coli), a diferencia de los casos esporádicos en los que dicha mutación se adquiere durante la vida adulta. Se observa que la COX-2 está sobreexpresada desde las etapas iniciales de los pólipos adenomatosos en seres humanos tanto en las formas hereditarias como en las esporádicas 13. Existen modelos murinos que desarrollan neoplasias intestinales múltiples (Min-mouse) como consecuencia de una mutación en el gen APC y han facilitado enormemente la investigación en este campo 14. En modelos murinos como en los humanos, se observa que la COX-2 induce neoangiogénesis, imprescindible para el crecimiento del adenoma, y que puede ser inhibida por JTE-522 y otros COXIB 15,16.
En un modelo de carcinogénesis cutánea 17 se ha logrado desarrollar ratones con mutaciones en los genes COX-1 y COX-2 mediante técnicas de Knockout (anulación funcional del gen), que son deficientes en estas enzimas, cuya epidermis muestra cambios derivados de una diferenciación queratinocítica prematura, y que son más resistentes al efecto de los carcinógenos químicos que los ratones genéticamente normales. La inhibición farmacológica de la COX-2 con celecoxib ha mostrado un efecto preventivo sobre la carcinogénesis cutánea inducida por rayos ultravioleta, con efecto dependiente de la dosis 18. La inhibición farmacológica de la COX-2, con COXIB a dos dosis distintas, produjo una disminución de la formación de pólipos del 62% y 50%, actividad claramente superior al efecto del sulindac (reducción del 26%), y que imita claramente el efecto del déficit genético 19,20.
Siguiendo en dirección corriente abajo de la vía biosintética de las PG, la prostaglandin-sintetasa E parece estar aumentada en adenomas y adenocarcinomas colorrectales humanos, aunque de forma no exactamente paralela a la COX-2, hecho que se interpreta como una evidencia adicional sobre la importancia de la PGE2 en el proceso carcinogénico 21. En los modelos de Min-mice si se administran AINE o anticuerpos neutralizantes de PGE2 se observa una reducción en el número y tamaño de las lesiones neoplásicas que tienden a ocurrir espontáneamente 22. Añadiendo análogos de la PGE2 se logra revertir el efecto preventivo de los AINE 23. El último paso en la vía de señalización de las PG es el estímulo de los receptores específicos de prostaglandinas, de la membrana celular y nuclear 24. La manipulación genética del receptor de la PGE2, EP2, también ha probado su influencia sobre la carcinogénesis.
Pero también se han observado en el laboratorio otros mecanismos de acción por los que los AINE resultan antineoplásicos. Empleando sulindac e indometacina se observó que la inhibición no selectiva de ambas isoformas de la COX conducía a una acumulación de ácido araquidónico, que a su vez activaba la esfingomielinasa, lo que incrementaba la síntesis de ceramida, sustancia que ejerce un potente efecto proapoptótico 25. Se han descrito otros mecanismos moleculares: activación de factor nuclear kappa-B (NF-κB) por algunos AINE 26, la inhibición de la IKKβ y en consecuencia la inhibición de la fosforilación de la IκBα por parte del ácido aceitlsalicílico, inhibición de la Bcl-XL por algunos AINE, etc. En las observaciones experimentales las concentraciones de fármacos que activan estos mecanismos son a menudo superiores a las que se pueden lograr en clínica, lo que ha motivado controversia sobre la importancia clínica de estos mecanismos.
Ciclooxigenasa-2: una conexión entre inflamación y carcinogénesis
La comprensión del papel de la COX-2 en la biología del proceso carcinogenético está permitiendo construir una visión unificadora de fenómenos que hasta hace poco creíamos dispersos. Recientemente ha quedado bien establecido que la infección por Helicobacter pylori es una causa de cáncer gástrico 27. Se propone el posible valor de las dos opciones quimiopreventivas: erradicación del H. pylori e inhibición de la COX. Pero la erradicación del H. pylori no siempre se sigue de una desaparición de la COX-2 elevada, lo que puede ser explicado por la hipótesis de que una vez iniciado el proceso carcinogénico existe un punto de no retorno, en el que adquiere autonomía y se mantiene o incluso se estimula por efecto de promotores no relacionados con la causa iniciadora del proceso 28,29. El estrés oxidativo es un potente inductor de la transcripción del factor de crecimiento del epitelio vascular (VEGF) 30, que interactúa estrechamente con la COX-2 en la neoangiogénesis que soporta la carcinogénesis. Es un mutágeno capaz de dañar el ADN celular al tiempo que las proteínas responsables de su reparación, y por tanto el propio proceso inflamatorio puede actuar como iniciador del cáncer a través de los radicales libres de oxígeno y de óxido nítrico que genera 31-33. Las células tumorales tienen la capacidad de aprovecharse de los factores tróficos secretados por las células inflamatorias, emplean las mismas moléculas de adhesión y utilizan las quimiocinas y sus receptores para emigrar y metastatizar, lo que presenta la visión del estroma tumoral «como una herida que no cura» 34.
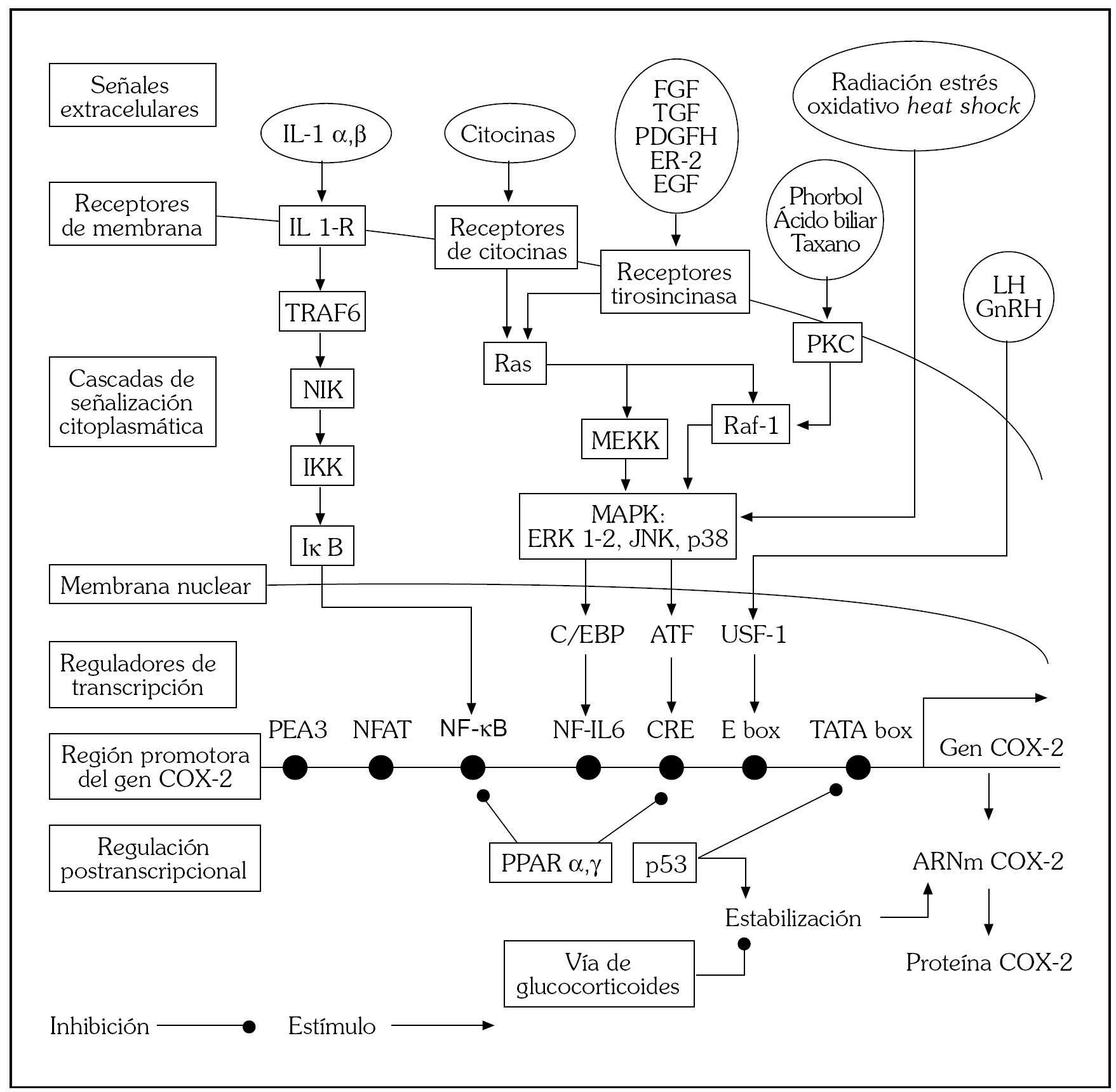
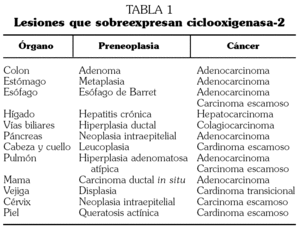
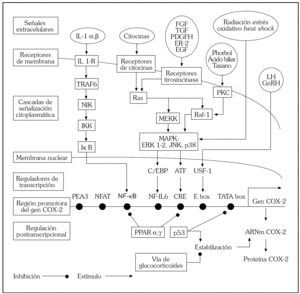
Pero también se detecta COX-2 expresada en otras lesiones preneoplásicas y cánceres (tabla 1) en los que la inflamación no parece desempeñar un papel etiopatogénico tan relevante. Ha sido descrito que la inflamación puede ser evocada por las propias células tumorales epiteliales 35, y en otros casos son las propias células epiteliales tumorales quienes expresan COX-2 en cantidades patológicas. En la figura 2 se esquematizan los mecanismos reguladores de la expresión de la COX-2, amalgamando procesos que en la realidad son específicos de tipo celular. La transcripción se produce como consecuencia de la activación de alguno de los sitios de la región promotora, o en algunos casos como resultado de la acción combinada de varios de estos sitios. Esta región puede activarse por estímulos tan diversos como interleucinas, citocinas, factores de crecimiento peptídicos, hormonas, radiaciones, carcinógenos químicos, oncogenes, etc. 36. La expresión de la COX-2 también está regulada a nivel postranscripcional a través de la estabilización del ARNm. Los corticoides parecen ser desestabilizadores del ARNm, con lo que se acelera su degradación, y en consecuencia se disminuye su función. El bloqueo de la COX-2 es un mecanismo de acción común a diversos agentes quimiopreventivos: retinoides como el ácido 9-cis-retinoico, antioxidantes como el pyrrolidinedithiocarbamato 37, talidomida 38, gefitinib 39, e incluso los aceites de oliva y de pescado 40. Parece claro que la COX-2 es inducible en respuesta a una gran variedad de estímulos implicados en la carcinogénesis, y esto explica la alta frecuencia con que se observa su expresión en un amplio abanico de lesiones preneoplásicas y cánceres.
Fig. 2. Elementos reguladores de la COX-2. La región promotora del gen de la COX-2 se regula por diversos factores de transcripción que a su vez son activados por las vías de señalización esquematizadas en la figura. IL: interleucina; FGF: factor de crecimiento de fibroblastos; TGF: factor de crecimiento transformante; PDGF: factor de crecimiento derivado de plaquetas; HER-2: oncogén de la familia de factor de crecimiento epidérmico; EFG: factor de crecimiento epidérmico; TNF: factor de necrosis tumoral; TRAF: factor asociado al receptor TNF; NF: factor nuclear; NIK: cinasa inductora de NF-kB; IKK: complejo cinasa-IkB; MAPK: cascada de proteincinasa activada; ERK: cinasa reguladora de señales extracelulares; JNK: cinasa aminoterminal de c-Jun; CRE: elemento de respuesta cAMP; TATA(AA) promotor hexa-nucleótico; C/EBP: proteína unida al potenciador de CCAAT; PPAR: receptor activado-proliferante de peroxidasa. Adaptada de Dvorak HF 34.
Efectos de las prostaglandinas derivadas de la COX-2 en la biología tumoral
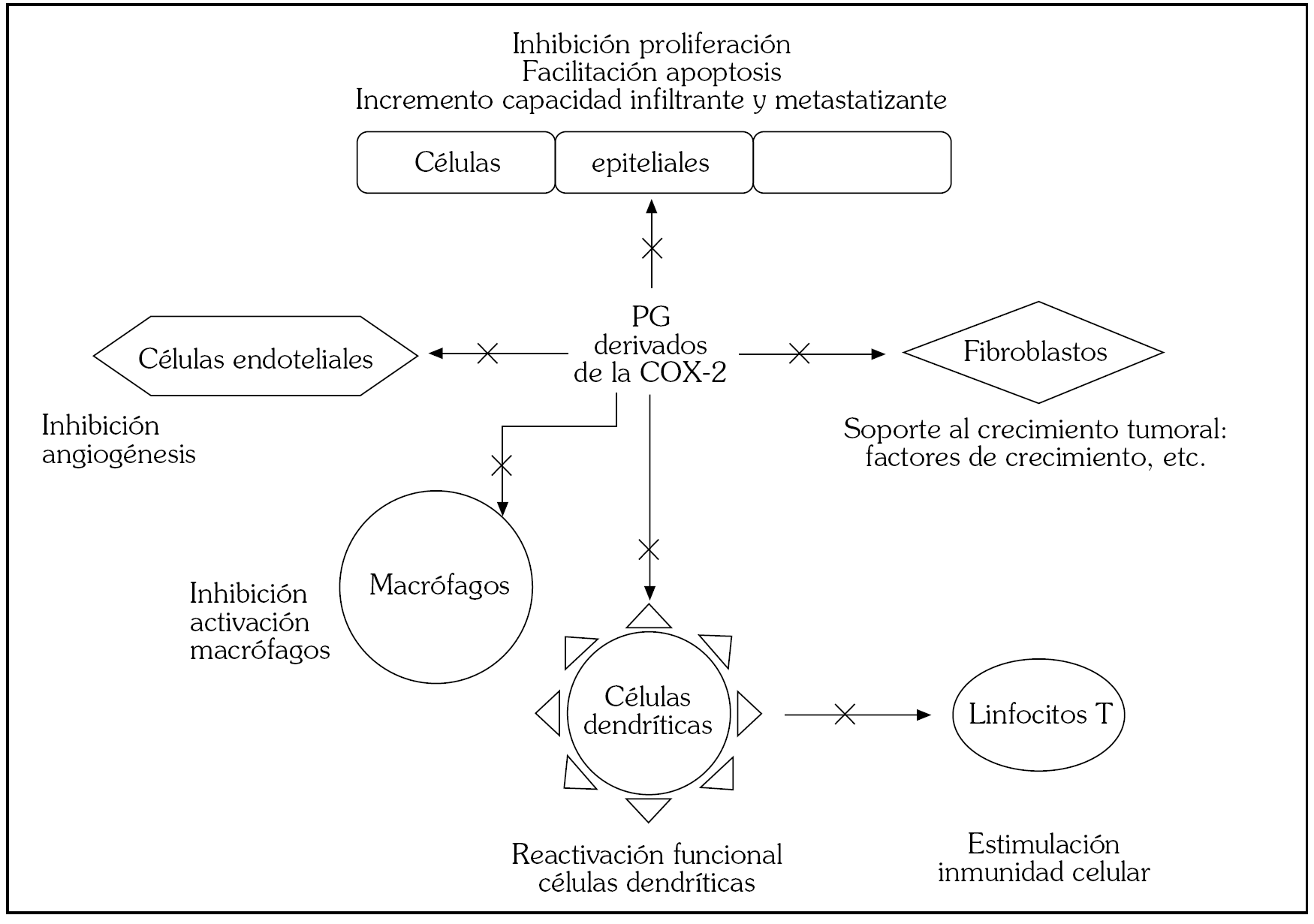
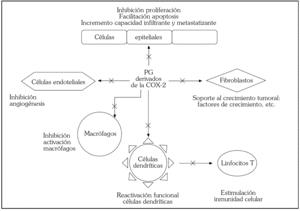
Las prostaglandinas ejercen efectos estimuladores de la proliferación celular, atenuadores de la apoptosis, moduladores de la expresión de moléculas de superficie que incrementan la capacidad de invasión y metástasis, estimulan la angiogénesis, atraen y activan a los macrófagos y producen inmunosupresión a través de su efecto sobre las distintas subpoblaciones linfocitarias 41. La formación de un cáncer es un proceso consistente en la adquisición de una serie de capacidades funcionales de la célula que le permitan su desarrollo autónomo 42: a) autosuficiencia en las señales de crecimiento; b) pérdida de la sensibilidad a las señales anti-proliferativas; c) evasión de la apoptosis, o muerte celular programada; d) potencial de replicación ilimitado, que parece relacionado con la actividad de la telomerasa; e) angiogénesis, imprescindible para el aumento de tamaño tumoral, ya que ninguna célula puede sobrevivir a una distancia superior a las 100 µm de algún capilar, y f) capacidad de invasión y metástasis, la capacidad que confiere letalidad a los tumores. El modelo teórico es posible por un fenómeno de inestabilización genética que favorece la adquisición del fenotipo canceroso gobernado por un limitado número de genes cruciales 43. Los prostanoides derivados de la COX parecen ser un componente importante de la maquinaria molecular que rige el proceso carcinogenético, como lo demuestra la evidencia disponible sobre los mecanismos de acción de los fármacos inhibidores de los COX (fig. 3).
Fig. 3. Efectos celulares y microambientales de los inhibidores de la COX-2. X: Inhibidor de los efectos de las prostaglandinas (PG) por inhibición de la COX-2. El grado de participación de cada tipo celular es específico de lesión preneoplásica, por lo que las redes de señalización intercelular en la que participan las PG presentan variabilidad dependiente de órgano y lesión neoplásica. Cualquier tipo celular puede ser fuente de PG bajo circunstancias microambientales apropiadas que activen la expresión y función de la COX-2.
Mecanismos de acción anticarcinogénica de los inhibidores de la ciclooxigenasa-2
Efectos antiproliferativo y proapoptótico
Existen pruebas experimentales que documentan el efecto inductor de la apoptosis 44-47. Es probable que este efecto sea incluso más importante que la inhibición de la proliferación 47. Una comparación directa del efecto de 6 COXIB (NS-398, nimesulida, meloxicam, etodolac, rofecoxib y celecoxib) sobre líneas celulares derivadas de cáncer de colon ha proporcionado los siguientes datos: todos ellos fueron capaces de suprimir la síntesis de PG, pero la capacidad de inhibir la proliferación e inducir apoptosis difería entre ellos 48. El efecto inhibidor de la fosforización de la quinasa antiapoptótica Akt puede ser la causa de esta diferencia. Esta fosforilación de la Akt fue descrita en las líneas celulares derivadas de cáncer de próstata LNCaP (andrógeno-dependientes) y PC-3 (andrógeno-independientes) 49,50. Las líneas celulares derivadas de tumores neuroectodérmicos primitivos resultaron más sensibles al efecto antitumoral del celecoxib que del rofecoxib, correlacionando este resultado con un efecto inhibidor de la fosforilazión de Akt y un efecto inductor de la caspasa-3 (promotora de la apoptosis) observables sólo en las células tratadas con celecoxib 51. Se ha llegado a la conclusión de que los requerimientos estructurales para inhibir la COX-2 difieren de los necesarios para inducir apoptosis 52.
Efecto antimetastásico
La relación entre las PG y la capacidad de adhesión celular a las proteínas de la matriz extracelular fue descrita a partir de experimentos de transfección de COX-2 a cultivos de células intestinales. Las células transfectadas expresaban COX-2 y cambios fenotípicos entre los que había una expresión disminuida de E-cadherina, molécula fundamental para la adhesión y comunicación intercelular, que le confería una capacidad incrementada de sobrevivir adherida al matrigel y que también ha sido relacionada con una mayor capacidad para metastatizar 53. La inhibición de la migración lograda a través de la inhibición de la COX-2 era reversible con la adición de PGE254. En otro modelo de células derivadas de cáncer de mama y otro de colon, se observó que indometacina, celecoxib, NS-398 y SC560 (inhibidor selectivo de COX-1) fueron capaces de reducir la capacidad metastásica de estos tumores 55,56.
Inhibición de la angiogénesis
La inhibición de la angiogénesis es otro mecanismo crucial de los AINE y COXIB 57-59. En modelos de neoangiogénesis in vivo la COX-2 parece ser la fuente principal de PG, mientras que la COX-1 no desempeña un papel destacado 60, hecho que contrasta con los modelos de cultivos celulares in vitro en los que se sugiere que sí puede resultar importante 61. El papel relativo de las isoenzimas de la COX fue evaluado con los inhibidores selectivos resultando que todos los fármacos capaces de inhibir la COX-2 produjeron una clara reducción de la neovascularización 62. Además proporcionaron evidencia experimental de que la PGE2 producida por el huésped, y actuando a través de los receptores tipo EP3, era esencial para este proceso 63. El papel de la COX-2 en la neoangiogénesis se debe a un efecto regulador directo sobre la proliferación y apoptosis de las células endoteliales 64, además de un efecto indirecto mediado por la inducción de factores proangiogénicos como el VEGF 65. Aún más importante para la quimioprevención es el hecho de que la neoangiogénesis tumoral anómala se inicia en las etapas preneoplásicas 66. Resulta interesante que las PG derivadas de la COX-2 son capaces de inducir la síntesis y secreción de VEGF por parte de fibroblastos y macrófagos, y a su vez, el VEGF tiene la capacidad de inducir la expresión de COX-2 en las células endoteliales humanas 67, con lo que constituyen un bucle de señalización molecular de importancia capital para la angiogénesis. Se ha propuesto el término de «angioprevención» como estrategia para prevenir el cáncer 68.
Papel de los fibroblastos
La expresión de COX-2 en lesiones preneoplásicas como los pólipos adenomatosos a menudo se localiza en el estroma, específicamente en fibroblastos, macrófagos y otras células inflamatorias 69. Los fibroblastos parecen desempeñar un papel en la carcinogénesis más importante de lo que hasta ahora se ha reconocido. Cultivos de fibroblastos humanos obtenidos mediante biopsias de colon normal, afecto por carcinoma, y áreas adyacentes al tumor han mostrado una capacidad de expresión de COX-2 y secreción de PG cuantitativamente bien diferenciadas en respuesta a interleucina-1B (IL-1β), lo que se interpreta como prueba de su papel como fuente de PG en el proceso carcinogenético 70. Pero esta capacidad de producir COX-2 se ve restringida cuando los fibroblastos entran en fase proliferativa 71. Investigando este fenómeno se ha descrito que también son capaces de producir y secretar un factor bautizado como cytoguardin, que inhibe la expresión de la COX-2 ante estímulos de tipo citocinas y factores de crecimiento, y que además induce una intensa inhibición de la angiogénesis 72. La función de los fibroblastos puede adoptar características específicas de órgano. Por ejemplo, en el estroma mamario la PGE2 estimula la síntesis de aromatasa, fuente principal de estrógenos en mujeres postmenopáusicas, y de este modo el estroma actúa como fuente microrregional del mitógeno más potente conocido para el tejido glandular mamario 73.
Inhibición de los macrófagos
La presencia de un infiltrado de células inflamatorias peritumorales se ha interpretado como prueba de que el sistema inmunitario ejerce algún tipo de acción antitumoral, aunque también se ha interpretado como cooperantes en la progresión tumoral. La activación de macrófagos implica la secreción de grandes cantidades de VEGF, entre otras citocinas y enzimas proteolíticas, y su presencia se correlaciona con la angiogénesis tumoral peri e intratumoral 74. La respuesta humoral contra antígenos solubles tumorales inducía un incremento de la proliferación tumoral, y los inmunocomplejos depositados en la matriz extracelular eran los responsables de la activación de los macrófagos. También, las mucinas producidas por las células de cáncer de colon son capaces de inducir de forma dosis-dependiente la expresión de ARNm y proteína de COX-2 en los macrófagos, produciéndose síntesis de PGE2 y la subsiguiente activación macrofágica, con la consiguiente secreción de VEGF y otras citocinas 74. La adición de un inhibidor selectivo de la COX-2 (SC236) antes de la activación de los macrófagos fue capaz de impedirla, y los efectos de dicha activación no se reproducen por la adición exclusiva de PGE275. La COX-2 desempeña un papel importante en la activación macrofágica, y los inhibidores de la COX-2 pueden antagonizarla, ejerciendo así, un efecto antitumoral.
Efecto inmunomodulador
La PGE2 desempeña un importante papel inmunomodulador que posibilita el escape de los tumores al sistema de inmunovigilancia al favorecer la respuesta humoral en detrimento de la respuesta celular. En cultivos de linfocitos T pudo comprobarse que la COX-2 formaba parte del conjunto de genes de reacción inmediata que mediaban la activación linfocitaria, y que los COXIB NS-398 y celecoxib eran capaces de interferir esta activación 76. Sin embargo, los estudios in vivo mostraron que la inhibición de la COX-2 era capaz de restaurar la inmunidad celular antitumoral a través de la disminución de IL-10 (inmunosupresora) y el incremento de la IL-12 (inmunoestimuladora) 77. Las investigaciones más recientes han identificado a las células dendríticas (CD) como las fundamentales en la regulación de este proceso. Son capaces de expresar COX-2 y sintetizar PGE2 que induce la producción de IL-10, que a su vez inhibe a la IL-12, y la subsiguiente inhibición funcional de la CD. La inhibición de la COX-2 produjo los efectos contrarios, inhibiendo la síntesis de PGE2, disminuyendo la IL-10, incrementando la cantidad de IL-12 y como resultado de todo ello restaurando la función de la CD 78. La inhibición de la COX-2 tumoral podría prevenir la anulación funcional de las CD inducida por los tumores 79.
Evidencias en seres humanos de la actividad quimiopreventiva de los inhibidores de la ciclooxigenasa
A finales de los años 70 y durante los años 80, los estudios epidemiológicos señalaban cierta asociación entre el consumo de AINE y la disminución en la incidencia de cáncer colorrectal. Durante la década de los 90 se publicaron numerosos estudios epidemiológicos que mostraban el efecto quimiopreventivo del ácido acetilsalicílico y otros AINE. Los resultados son consistentes en mostrar este efecto quimiopreventivo y de reducción de la incidencia de pólipos o de cáncer 80. Los primeros resultados comunicados de estos ensayos 80,81 han sido positivos: la administración de ácido acetilsalicílico a una población de alto riesgo reduce la incidencia de nuevos pólipos.
Era conocida la eficacia del sulindac y del piroxicam para reducir el número y tamaño de los pólipos de colon de pacientes con PAF. Un ensayo prospectivo, aleatorizado y doble ciego que incluyó 22 pacientes mostró que el sulindac era capaz de inducir una reducción estadísticamente significativa del número y tamaño de los pólipos en comparación al placebo 82. El efecto del celecoxib fue investigado más recientemente en un ensayo prospectivo que incluyó 77 pacientes y que comparó placebo con dos niveles de dosis: 200 mg y 800 mg al día. Los resultados mostraron que las dosis altas de celecoxib fueron capaces de reducir el número y tamaño de los pólipos en colon 83. También los pólipos duodenales mostraron reducción de tamaño con este COXIB 84.
La incidencia de cáncer de mama en relación con el consumo de AINE es el segundo tumor más investigado, tras el cáncer de colon. Aunque los estudios individuales no presentaron resultados tan consistentes como los de colon, un metaanálisis ha mostrado que el efecto conjunto de todos los estudios incluidos muestra una reducción de la incidencia estadísticamente significativa 85. Cabe citar estudios epidemiológicos que indican reducción de incidencia de cáncer de pulmón 86, vejiga urinaria 87, tracto aerodigestivo superior 88 y páncreas 89, entre otros 90-92.
En un estudio prospectivo se observó que los niveles de PGE2 de tejido tumoral elevados disminuían claramente en pacientes con cáncer de pulmón que se trataban con quimioterapia preoperatoria más celecoxib frente a los que se trataban con quimioterapia sólo, con una influencia positiva en la respuesta clínica 93.
Por último hay otro tipo de datos cuya relevancia para la quimioprevención, aunque sea indirecta, parece incuestionable: la detección de niveles elevados de COX-2 en tumores humanos, y el valor pronóstico negativo que dicha expresión conlleva 1-3. Un porcentaje que oscila entre el 40% y el 90% de los tumores humanos más frecuentes (colon, pulmón, mama, próstata, etc.) muestra expresión elevada de COX-2 94. Un creciente número de publicaciones está documentando que el incremento de función de la COX-2 conlleva un peor pronóstico 95,96. La interpretación de estas observaciones es que la COX-2 no sólo contribuye a la carcinogénesis, sino que tras el pleno desarrollo fenotípico del cáncer sigue actuando como un acelerador de la agresividad biológica.
Seguridad de los inhibidores de la ciclooxigenasa
Ya hemos señalado que la seguridad de la medicación es tan importante como su eficacia para que la quimioprevención sea viable. El ácido acetil salicílico usado en la prevención de accidentes cardiovasculares, conlleva riesgo de accidente cerebrovascular hemorrágico (odds ratio: 1,4; IC 95%: 0,9 a 2), y hemorragia gastrointestinal (odds ratio: 1,7; IC 95%: 1,4 a 2,1), que restan parte del beneficio logrado en población de alto riesgo, o incluso pueden resultar en un balance negativo en poblaciones de bajo riesgo 97. Los COXIB no afectan a las plaquetas porque éstas carecen de COX-2 98. La toxicidad gastrointestinal de los AINE alcanza proporciones que le proyectan como problema de salud pública, tanto por la morbimortalidad, como por el impacto económico sobre los sistemas de salud 99. La reducción de esta toxicidad fue una de las principales motivaciones para el desarrollo de los COXIB. Los ensayos conocidos como VIGOR 100 y CLASS 101 compararon con AINE el rofecoxib y el celecoxib respectivamente, administrados a dosis superiores a las recomendadas para su uso como antiinflamatorios. Ambos COXIB mostraron una menor incidencia de complicaciones gastrointestinales que los AINE elegidos como comparadores. El metaanálisis de los estudios aleatorizados que compararon celecoxib con otros AINE mostró una ventaja a favor del celecoxib en abandonos del tratamiento por efectos gastrointestinales, incidencia de úlceras detectables por endoscopia y úlceras sintomáticas, perforaciones, hemorragias y obstrucciones 102.
La función renal es el aspecto en el que los COXIB menos han reducido el bajo riesgo asociado a los AINE. Como advierten la fichas técnicas de los COXIB comercializados puede observarse deterioro de la función renal con una frecuencia similar a la conocida para los AINE.La alteración de la función renal y de la presión sanguínea fue inferior con celecoxib que con otros AINE. Las diferencias entre los dos COXIB ya se habían detectado por el sistema de farmacovigilancia de la Organización Mundial de la Salud (OMS) que registra los comunicados espontáneos de efectos farmacológicos adversos, y que había advertido diferencias significativas en las que el rofecoxib provoca mayor número de casos de edema, deterioro de la función renal, insuficiencia renal aguda, insuficiencia cardíaca e hipertensión que el celecoxib 103-105.
Perspectivas de futuro
El concepto de que la prevención del cáncer en seres humanos es posible mediante el empleo de AINE y COXIB ha recibido un fuerte apoyo de los ensayos clínicos prospectivos aleatorizados 80-82 que han mostrado que es posible modificar la historia natural de una patología preneoplásica como los pólipos del colon. La importancia de este hecho fue reconocida es EE.UU. al aprobarse la indicación del celecoxib para el tratamiento de la PAF. Las ventajas de los COXIB sobre otros AINE en cuanto a efectos secundarios les sitúan como candidatos ideales para la quimioprevención. Se están realizando ensayos de prevención de la recurrencia de pólipos adenomatosos esporádicos con celecoxib y con rofecoxib. También se está investigando el papel del celecoxib en otros procesos preneoplásicos como esófago de Barret, carcinoma in situ de vejiga urinaria, keratosis actínica, broncopatía por tabaco, mama de riesgo, etc. Recientemente se han comunicado algunos resultados preliminares de celecoxib en lesiones preneoplásicas de cérvix uterino, y resultan bastante esperanzadores, tanto en displasia como en carcinoma intraepitelial 106.
Además, existe otro argumento comparativo: el celecoxib y el piroxicam se encuentran entre los agentes más potentes en reducir la incidencia de tumores intestinales inducidos por las 186 sustancias evaluadas en un modelo de carcinogénesis experimental 107. El significado de esta evidencia es claro: no sólo hay buenas pruebas científicas que avalen el estudio en seres humanos del potencial quimiopreventivo de los COXIB, sino que el celecoxib es una de las opciones más atractivas del amplísimo panel de moléculas candidatas a evaluación clínica.
Los estudios más recientes están encaminados a explorar el potencial quimiopreventivo de celecoxib en otras neoplasias aparte del cáncer colorrectal, entre los que cabe destacar el cáncer de pulmón, próstata y de mama 108-112. En esta última neoplasia, llama la atención la correlación de la sobreexpresion de COX-2 y HER2 que confiere mayor agresividad biológica a la célula tumoral y que puede inhibirse con trastuzumab 113. Nosotros mismos estamos investigando el posible efecto de ese fármaco en la prevención de recidivas y de segundas neoplasias en pacientes con cáncer de cabeza y cuello 114, y su posible monitorización con mARN de COX-2 en sangre periférica 115. Además, se está observando que celecoxib también potencia el efecto de la radioterapia sin incrementar su toxicidad 116,117.
Recientemente se han publicado tres estudios randomizados que evidencian el riesgo cardiovascular de rofecoxib, celecoxib y valdecoxib 118-120. El estudio APPROVe para prevención de pólipos adenomatosos de colon con rofecoxib puso de manifiesto que doblaba el riesgo de accidentes cardiovasculares comparado con placebo. Como consecuencia, se paró el estudio y se retiró rofecoxib del mercado en septiembre de 2004. Un estudio similar para prevención de pólipos de colon (APC Study), con celecoxib 200 ó 400 mg dos veces al día, ha evidenciado un 2,3% y un 3,4% respectivamente más accidentes cardiovasculares que placebo 119. Además, el estudio de valdecoxib para dolor cardíaco tras by-pass coronario, evidenció el doble de efectos secundarios cardíacos que el placebo 120. Los inhibidores de COX-2 no sólo carecen del efecto antiplaquetario del ácido acetilsalicílico, sino que alteran las defensas del endotelio vascular contra la agregación plaquetaria, la hipertensión y la arterioesclerosis y además favorecen la vasoconstricción 121. La mejor relación riesgo-beneficio obtenida con celecoxib, que se muestra menos cardiotóxico que otros COXIB ha hecho que un comité de expertos reunido por la Food and Drug Administration de EE.UU. aconseje por el momento que continúe en el mercado y en los ensayos clínicos, aunque incluyendo en la ficha técnica y en la información para el paciente, la advertencia de la posible cardiotoxicidad en los pacientes con riesgo, especialmente en fumadores activos y pacientes con antecedentes recientes de cardiopatía isquémica 122.
Es oportuno mencionar que la reticencia que suscita la noción de prevenir el cáncer con fármacos deberá considerar cuidadosamente los resultados de los ensayos que se publicarán en los próximos años y que vendrán a sumarse a los ya publicados con antiestrógenos en la prevención del cáncer de mama, además de los mencionados con celecoxib y ácido acetilsalicílico. La opinión negativa sobre la medicalización progresiva de la vida, vigente en algunos sectores sociales, deberá contrastarse con la posibilidad de prolongar la vida media de la población a través de la reducción o retraso de la incidencia de los cánceres más frecuentes.