La neumonía adquirida en la comunidad (NAC) es una afección común y potencialmente grave. En los últimos años ha empezado a tenerse en cuenta el control de la respuesta inflamatoria como un nuevo objetivo terapéutico en esta enfermedad. El objetivo de este estudio fue analizar la influencia de la administración de corticoides sistémicos sobre la mortalidad de los pacientes ingresados con NAC en condiciones de práctica clínica habitual.
Pacientes y métodosEstudio prospectivo observacional en el que se recogieron casos de NAC en pacientes ingresados en los servicios de Medicina Interna y Neumología de un hospital terciario a lo largo del año 2007. Se registró el tratamiento administrado durante su ingreso y se determinó la mortalidad hospitalaria, así como a los 30 y 90 días del alta hospitalaria.
ResultadosSe analizaron 257 pacientes, 179 varones (69,6%) y 78 mujeres (30,4%). La edad media fue de 72±15 años. Tanto la mortalidad hospitalaria como a los 30 días del alta fue del 10,2%, mientras que la mortalidad global a los 90 días fue del 14,8%. No se encontró relación entre el empleo de corticoides y la mortalidad. El uso de corticoides tampoco modificó los días de estancia hospitalaria ni la tasa de reingresos.
ConclusionesEn este estudio se ha observado que el tratamiento con corticoides sistémicos en la NAC no se asocia con una menor mortalidad ni influye en la tasa de reingresos. Tampoco modifica la duración de la estancia hospitalaria.
Community-acquired pneumonia (CAP) is a common and potentially serious disease. In recent years, control of the inflammatory response has begun to be taken into account as a new therapeutic target. This study has aimed to analyze the influence of the administration of systemic corticosteroids on mortality of patients admitted with CAP in the common clinical practice.
Patients and methodsA prospective observational study was carried out. The study included patients with CAP admitted to Internal Medicine and Pulmonology services of a tertiary hospital in 2007. Treatment given during admission was recorded and mortality during hospitalization and at 30 and 90 days after discharge was determined.
ResultsA total of 257 patients, 179 men (69.6%) and 78 women (30.4%) were analyzed. Mean age was 72±15 years. Both in-hospital mortality as well as at 30 days of discharge was 10.2%, while overall mortality at 90 days was 14.8%. No relation was found between the use of corticosteroids and mortality. Use of corticosteroids also did not modify the length of hospital stay or readmission rate.
ConclusionsIt was observed in this study that treatment with corticosteroids in CAP is not associated with lower mortality and does not affect the rate of readmissions. It also does not change the length of hospital stay.
La neumonía adquirida en la comunidad (NAC) es frecuente, y conlleva una mortalidad global cercana al 14%, que se mantiene estable a pesar de los indudables avances en su diagnóstico y tratamiento. El control de la respuesta inflamatoria se perfila como un nuevo objetivo terapéutico. Este estudio pretende evaluar el papel del tratamiento con corticoides sistémicos sobre la mortalidad de los pacientes con NAC.
¿Qué aporta este artículo?La administración de corticoides sistémicos en la NAC no se asocia con una menor mortalidad. Tampoco reduce la tasa de reingresos ni la estancia hospitalaria.
Los Editores
La neumonía adquirida en la comunidad (NAC) es una afección común y potencialmente grave. Su incidencia en España es de alrededor de 20 casos/1.000 habitantes/año1. El porcentaje de pacientes con NAC que ingresa es muy variable, y depende de diversos factores2. Su mortalidad global es elevada, y en la actualidad en España es cercana al 14%3. A pesar del avance de las técnicas de diagnóstico, del desarrollo de nuevos antibióticos y, de la mayor sofisticación de las unidades de Cuidados Intensivos, dicha cifra se ha mantenido estable a lo largo de las últimas décadas, siendo similar a la descrita en artículos científicos de hace 70 años4–8. El tratamiento antimicrobiano de la NAC se establece de forma empírica, tras valorar la gravedad del cuadro y la etiología más probable9. No obstante, existen normativas que facilitan la toma de decisiones3.
En los últimos años, se ha comenzado a perfilar como un nuevo objetivo el control de la respuesta inflamatoria, dado que se ha demostrado que existe una relación directa entre la intensidad de dicha respuesta medida en sangre, y la gravedad de la neumonía10–14. En este sentido se considera que los glucocorticoides son potentes antiinflamatorios naturales. El hipotético papel de los corticoides en el tratamiento de la NAC comenzó a postularse hace más de 50 años. El objetivo de su administración radicaría en el control de una respuesta inflamatoria excesiva, tanto a nivel pulmonar como sistémico. Se dispone de varios estudios y ensayos clínicos acerca de sus beneficios al ser añadidos al tratamiento convencional de la neumonía, con resultados contradictorios15–23 entre ellos, por lo que su empleo sigue resultando controvertido.
El objetivo de este estudio fue analizar la influencia de la administración de corticoides sistémicos sobre la mortalidad hospitalaria de los pacientes ingresados con NAC en condiciones de práctica clínica habitual.
Pacientes y métodosSe realizó un estudio prospectivo observacional en el que se recogieron pacientes ingresados con el diagnóstico de NAC en los servicios de Medicina Interna y Neumología del Hospital General Universitario Gregorio Marañón desde enero a diciembre de 2007.
Los criterios de inclusión fueron los siguientes: a) pacientes hospitalizados en las plantas de Medicina Interna y Neumología durante el período de recogida de datos; b) sujetos ingresados con el diagnóstico principal de neumonía (definido como un cuadro clínico compatible y aparición de un nuevo infiltrado en la radiografía de tórax o en una TC torácica sugerente de dicho proceso) o bien neumonía como diagnóstico secundario, con un diagnóstico principal de insuficiencia respiratoria o sepsis; y c) pacientes adultos (edad igual o superior a 18 años).
Los criterios de exclusión fueron: a) alta hospitalaria en los 15 días previos al nuevo ingreso; b) neumonías de adquisición nosocomial; c) pacientes procedentes de la Unidad de Cuidados Intensivos; d) situaciones clínicas que implicaran inmunosupresión, ya fuera fisiológica o inducida farmacológicamente; e) éxitus en las primeras 48h del ingreso (con el objetivo de excluir a los pacientes agónicos en los que se limitó el esfuerzo terapéutico); y f) enfermos oncológicos en tratamiento paliativo.
Una vez que los pacientes se encontraban en la planta de hospitalización, y durante las primeras 48h de ingreso, se analizaba el caso a partir de la historia clínica realizada en el servicio de Urgencias y, si era necesario, mediante entrevista con el paciente y consulta de su historial médico previo. Se obtenían datos relativos a la comorbilidad del enfermo (factores de riesgo cardiovascular, existencia de afección cardíaca, pulmonar, renal o hepática significativa, antecedentes de enfermedad oncológica activa o en remisión, existencia de deterioro cognitivo –evaluado mediante el test Mini-Mental–), que posteriormente eran empleados para calcular el índice de Charlson24, valores analíticos (hemograma, coagulación, gasometría arterial, bioquímica sanguínea completa que incluía función renal hepática e, iones, además, de reactantes de fase aguda como la proteína C reactiva y el fibrinógeno), alteraciones radiológicas (visibles en la radiografía simple de tórax o TC torácica), estudios microbiológicos (hemocultivos extraídos en urgencias), tratamiento antibiótico empírico iniciado a su ingreso en el hospital (diferentes tipos de regímenes terapéuticos, en monoterapia o combinación), así como el empleo de corticoides (vía de administración y tipo de fármaco empleado). También se registraban datos demográficos significativos (edad, sexo y si estaba institucionalizado). La gravedad de la neumonía se determinaba mediante el PSI (Pneumonia Severity Index)25. Posteriormente se valoraba la evolución del enfermo y el manejo farmacológico durante su ingreso hospitalario mediante la revisión del informe de alta o éxitus. Una vez dado de alta se contactaba con el paciente o sus familiares por vía telefónica a los 30 y 90 días, para evaluar la mortalidad y el uso de recursos sanitarios en cada período.
Todos los pacientes dieron su consentimiento informado para su inclusión en el estudio, de acuerdo con las normas de la declaración de Helsinki de 1975, y el acceso posterior a los datos de las historias clínicas se llevó a cabo de acuerdo con los protocolos establecidos en el hospital.
El análisis estadístico fue realizado con el programa SPSS, versión 15.0. Las 2 principales variables a estudio fueron el uso de corticoides y la mortalidad. La relación entre las diferentes variables se analizó mediante la prueba de la t de Student para variables cuantitativas y la de Chi-cuadrado para las variables cualitativas. La prueba U de Mann-Whitney se empleó en aquellos casos en los que por sus características, no era posible usar pruebas paramétricas y en aquellas variables que siendo categóricas, tenían un carácter ordinal. Todas las variables estudiadas en las que se observó asociación estadísticamente significativa se evaluaron mediante regresión logística univariante con el fin de conocer la odds ratio para cada una de ellas. Posteriormente se realizó un análisis multivariante para detectar qué variables tenían más relación independiente con la mortalidad.
ResultadosSe incluyó a un total de 257 pacientes, 179 varones (69,6%) y 78 mujeres (30,4%). Su edad media fue de 72±15 años (rango: 17-101). La mayoría de los enfermos procedía de su domicilio (87,1%) y solo un pequeño porcentaje (12,9%) había sido enviado desde residencias de ancianos o centros de larga estancia.
La mortalidad global fue del 10,2%, tanto durante el ingreso hospitalario, como a los 30 días del alta. La mortalidad a 90 días fue del 14,8%. Por otra parte, 55 enfermos (21,4%) reingresaron durante los 3 meses de seguimiento.
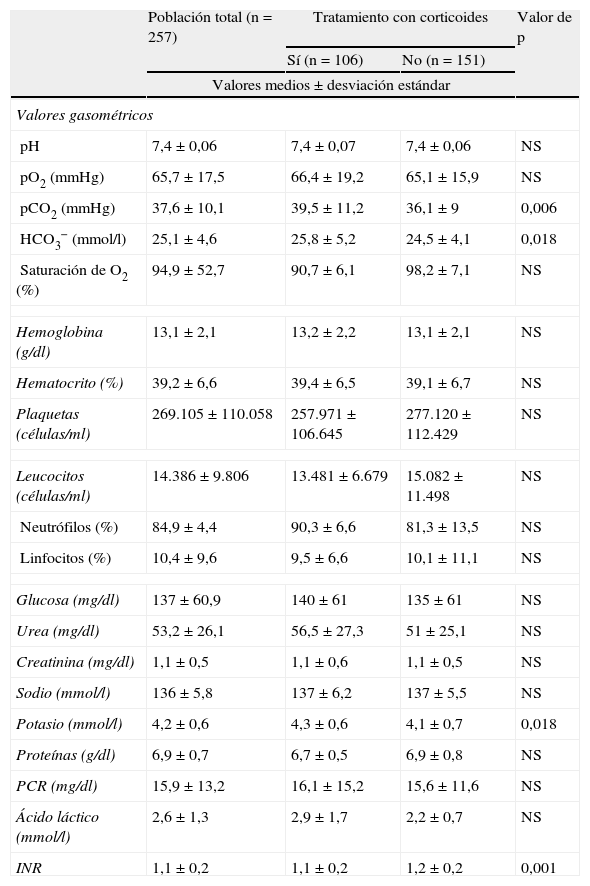
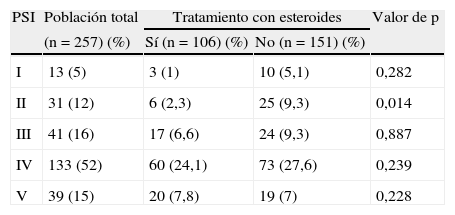
Las comorbilidades más frecuentes fueron la hipertensión arterial (53,5%), seguida de la enfermedad pulmonar obstructiva crónica (EPOC) (35,4%), y la dislipemia (23%). Un 19,5% de los pacientes eran fumadores activos en el momento del ingreso, y el 35,4% eran exfumadores. El 8,6% eran consumidores importantes de alcohol. Las características analíticas de los pacientes se detallan en la tabla 1. La distribución de la gravedad de la neumonía de los pacientes incluidos en el estudio, evaluada según la escala PSI25 se resume en la tabla 2; el 67% de los pacientes tenían estadio IV o V, sin diferencias apreciables en relación con el tratamiento esteroideo.
Parámetros analíticos más frecuentes en los pacientes del estudio
| Población total (n=257) | Tratamiento con corticoides | Valor de p | ||
| Sí (n=106) | No (n=151) | |||
| Valores medios±desviación estándar | ||||
| Valores gasométricos | ||||
| pH | 7,4±0,06 | 7,4±0,07 | 7,4±0,06 | NS |
| pO2 (mmHg) | 65,7±17,5 | 66,4±19,2 | 65,1±15,9 | NS |
| pCO2 (mmHg) | 37,6±10,1 | 39,5±11,2 | 36,1±9 | 0,006 |
| HCO3− (mmol/l) | 25,1±4,6 | 25,8±5,2 | 24,5±4,1 | 0,018 |
| Saturación de O2 (%) | 94,9±52,7 | 90,7±6,1 | 98,2±7,1 | NS |
| Hemoglobina (g/dl) | 13,1±2,1 | 13,2±2,2 | 13,1±2,1 | NS |
| Hematocrito (%) | 39,2±6,6 | 39,4±6,5 | 39,1±6,7 | NS |
| Plaquetas (células/ml) | 269.105±110.058 | 257.971±106.645 | 277.120±112.429 | NS |
| Leucocitos (células/ml) | 14.386±9.806 | 13.481±6.679 | 15.082±11.498 | NS |
| Neutrófilos (%) | 84,9±4,4 | 90,3±6,6 | 81,3±13,5 | NS |
| Linfocitos (%) | 10,4±9,6 | 9,5±6,6 | 10,1±11,1 | NS |
| Glucosa (mg/dl) | 137±60,9 | 140±61 | 135±61 | NS |
| Urea (mg/dl) | 53,2±26,1 | 56,5±27,3 | 51±25,1 | NS |
| Creatinina (mg/dl) | 1,1±0,5 | 1,1±0,6 | 1,1±0,5 | NS |
| Sodio (mmol/l) | 136±5,8 | 137±6,2 | 137±5,5 | NS |
| Potasio (mmol/l) | 4,2±0,6 | 4,3±0,6 | 4,1±0,7 | 0,018 |
| Proteínas (g/dl) | 6,9±0,7 | 6,7±0,5 | 6,9±0,8 | NS |
| PCR (mg/dl) | 15,9±13,2 | 16,1±15,2 | 15,6±11,6 | NS |
| Ácido láctico (mmol/l) | 2,6±1,3 | 2,9±1,7 | 2,2±0,7 | NS |
| INR | 1,1±0,2 | 1,1±0,2 | 1,2±0,2 | 0,001 |
INR: International Normatized Ratio; pCO2: presión arterial de carbónico; PCR: proteína C reactiva; pO2: presión arterial de oxígeno.
Distribución de los pacientes según la escala PSI
| PSI | Población total | Tratamiento con esteroides | Valor de p | |
| (n=257) (%) | Sí (n=106) (%) | No (n=151) (%) | ||
| I | 13 (5) | 3 (1) | 10 (5,1) | 0,282 |
| II | 31 (12) | 6 (2,3) | 25 (9,3) | 0,014 |
| III | 41 (16) | 17 (6,6) | 24 (9,3) | 0,887 |
| IV | 133 (52) | 60 (24,1) | 73 (27,6) | 0,239 |
| V | 39 (15) | 20 (7,8) | 19 (7) | 0,228 |
PSI: Pneumonia Severity Index.
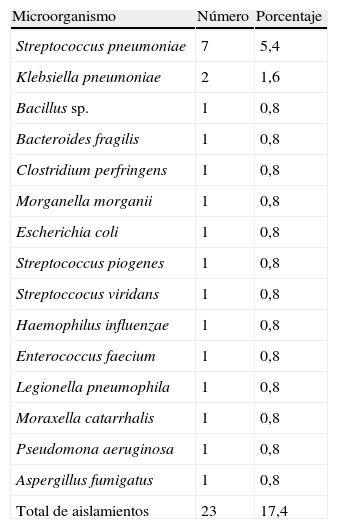
Se extrajeron hemocultivos en 129 pacientes (50,2%) aislándose microorganismos en 23 (17,4%) de ellos (tabla 3).
Aislamientos microbiológicos en los hemocultivos obtenidos en el servicio de Urgencias
| Microorganismo | Número | Porcentaje |
| Streptococcus pneumoniae | 7 | 5,4 |
| Klebsiella pneumoniae | 2 | 1,6 |
| Bacillus sp. | 1 | 0,8 |
| Bacteroides fragilis | 1 | 0,8 |
| Clostridium perfringens | 1 | 0,8 |
| Morganella morganii | 1 | 0,8 |
| Escherichia coli | 1 | 0,8 |
| Streptococcus piogenes | 1 | 0,8 |
| Streptoccocus viridans | 1 | 0,8 |
| Haemophilus influenzae | 1 | 0,8 |
| Enterococcus faecium | 1 | 0,8 |
| Legionella pneumophila | 1 | 0,8 |
| Moraxella catarrhalis | 1 | 0,8 |
| Pseudomona aeruginosa | 1 | 0,8 |
| Aspergillus fumigatus | 1 | 0,8 |
| Total de aislamientos | 23 | 17,4 |
El porcentaje se expresa en relación al total de hemocultivos extraídos, n=129.
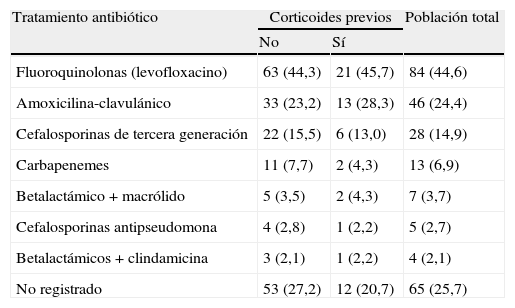
El tratamiento antibiótico empírico se describe en la tabla 4. El tiempo medio desde la entrada en urgencias hasta la administración de la primera dosis de antimicrobiano fue de 5,7h. La duración media del tratamiento fue de 14,5±5 días. En 17% de los casos fue necesario un cambio de régimen antibiótico durante la hospitalización. El cambio más frecuentemente realizado fue la adición de un macrólido al tratamiento previo, seguido del cambio o adición de una fluoroquinolona.
Tratamiento antibiótico empírico de los pacientes con neumonía adquirida en la comunidad incluidos en el estudio, desde el servicio de Urgencias
| Tratamiento antibiótico | Corticoides previos | Población total | |
| No | Sí | ||
| Fluoroquinolonas (levofloxacino) | 63 (44,3) | 21 (45,7) | 84 (44,6) |
| Amoxicilina-clavulánico | 33 (23,2) | 13 (28,3) | 46 (24,4) |
| Cefalosporinas de tercera generación | 22 (15,5) | 6 (13,0) | 28 (14,9) |
| Carbapenemes | 11 (7,7) | 2 (4,3) | 13 (6,9) |
| Betalactámico+macrólido | 5 (3,5) | 2 (4,3) | 7 (3,7) |
| Cefalosporinas antipseudomona | 4 (2,8) | 1 (2,2) | 5 (2,7) |
| Betalactámicos+clindamicina | 3 (2,1) | 1 (2,2) | 4 (2,1) |
| No registrado | 53 (27,2) | 12 (20,7) | 65 (25,7) |
Datos expresados como frecuencia (porcentaje).
Los corticoides sistémicos fueron utilizados frecuentemente como coadyuvantes en el tratamiento de la NAC, concretamente en 106 pacientes (41,4% del total). La principal indicación para su administración fue la existencia de broncoespasmo. La vía mayoritaria de administración inicial fue la intravenosa (99% de los casos). El corticoide utilizado en la mayor de los casos fue la metilprednisolona (se empleó en 105 de los 106 pacientes tratados con corticoides); solo se utilizó deflazacort en una ocasión.
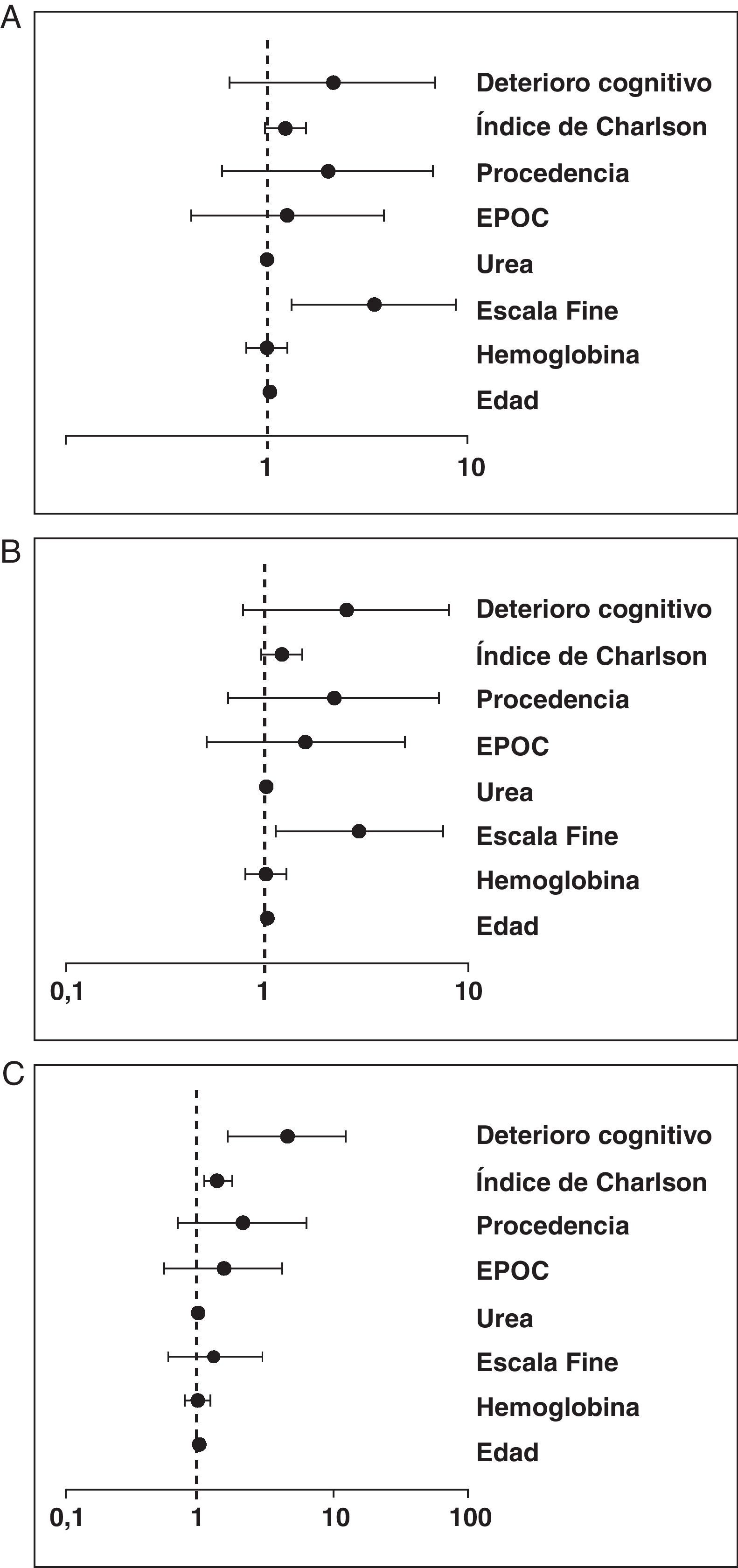
La mortalidad global durante el ingreso, así como a los 30 días del alta fue del 10,2% (26 pacientes). Se detectó una asociación estadísticamente significativa entre la mortalidad y la procedencia del paciente (7,6% de los pacientes procedía de su domicilio frente al 27,3% que había sido derivado de residencias y otras instituciones; p=0,002). También se detectó una mayor mortalidad en los pacientes que padecían deterioro cognitivo de algún grado (25,5 vs 5,9%; p<0,001). Esta mortalidad se concentró fundamentalmente en las categorías IV (9%) y V (34,2%) de la escala PSI.
Respecto a la mortalidad a los 90 días del alta, fue de 14,8% (38 pacientes). Al igual que en los casos anteriores se detectó una mayor mortalidad entre los pacientes que provenían de residencias (42,4 vs 10,8%; p<0,001) y en los que presentaban deterioro cognitivo (41,8 vs 7,4%; p<0,001). La mortalidad se concentró fundamentalmente en las categorías IV (15%) y V (39,5%) de la escala PSI.
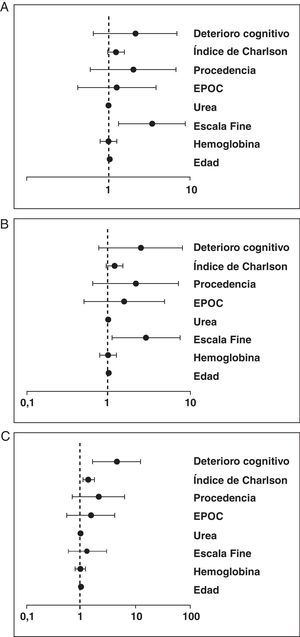
Tras el análisis de regresión logística multivariante, las variables asociadas de forma independiente a una mayor mortalidad fueron las puntuaciones elevadas en la escala PSI (mortalidad intrahospitalaria y a los 30 días), la existencia de deterioro cognitivo y las puntuaciones elevadas (>3 puntos) en el índice de Charlson (mortalidad a los 90 días del alta). En la figura 1 se detallan estos resultados.
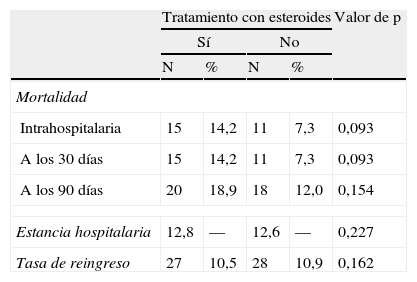
Los corticoides sistémicos fueron utilizados frecuentemente en el tratamiento de la NAC (41,4%; n=106). Su uso fue mayor en los varones (46,6 vs 29,5%; p=0,013) y en el subgrupo de pacientes con EPOC (65,9 vs 27,9%; p<0,001). Su principal indicación fue la existencia de broncoespasmo. La administración de corticoides sistémicos no tuvo un impacto significativo en la mortalidad en ninguno de los puntos de corte analizados, así como tampoco modificó de forma significativa los días de estancia hospitalaria ni la tasa de reingreso (tabla 5).
Relación entre el uso de corticoides sistémicos y la mortalidad
| Tratamiento con esteroides | Valor de p | ||||
| Sí | No | ||||
| N | % | N | % | ||
| Mortalidad | |||||
| Intrahospitalaria | 15 | 14,2 | 11 | 7,3 | 0,093 |
| A los 30 días | 15 | 14,2 | 11 | 7,3 | 0,093 |
| A los 90 días | 20 | 18,9 | 18 | 12,0 | 0,154 |
| Estancia hospitalaria | 12,8 | — | 12,6 | — | 0,227 |
| Tasa de reingreso | 27 | 10,5 | 28 | 10,9 | 0,162 |
El control de la respuesta inflamatoria está postulándose en los últimos años como un nuevo tratamiento para la infección respiratoria grave. Los principales fármacos implicados en dicho control son los glucocorticoides, cuyo uso ha sido objeto de un importante debate en los últimos tiempos. La discusión gira en torno a su eficacia como tratamiento coadyuvante para conseguir un aumento en la supervivencia de los pacientes con NAC grave, así como sus indicaciones, su dosificación y la duración óptima del tratamiento. Los últimos ensayos clínicos realizados a este respecto se han centrado en el empleo de dosis bajas y prolongadas en el tiempo, para evitar el efecto rebote en la inflamación al suprimir su administración:
- –
Annane et al.15 realizaron un ensayo multicéntrico, aleatorizado y doble ciego, en el que emplearon hidrocortisona (50mg por vía intravenosa cada 6h) y fludrocortisona (50μg al día durante 7 días). Dichos autores encontraron una menor mortalidad entre los pacientes que presentaban una insuficiencia suprarrenal relativa (53 vs 75%; p=0,006) y también, aunque menor, de forma global (58 vs 67%; p=0,043).
- –
Confalonieri et al.16 efectuaron otro estudio multicéntrico, prospectivo, aleatorizado y doble ciego, en el que administraron un bolo de 200mg de hidrocortisona, seguido de una perfusión continua de 10mg/h por vía intravenosa durante 7 días. Los pacientes que recibieron dicho tratamiento tuvieron una menor mortalidad (0 vs 38%; p=0,001) a los 60 días del alta. También detectaron una menor estancia hospitalaria y una menor necesidad de ventilación mecánica. Estos resultados fueron ampliamente criticados por el pequeño tamaño muestral (48 pacientes) y la existencia de diferencias en la comorbilidad entre los 2 grupos que favorecían al tratado con corticoides. En cualquier caso, estos datos parecen confirmar la hipótesis de que el control precoz de la inflamación, con dosis bajas y prolongadas en el tiempo, podría contribuir a una mejor evolución del proceso pulmonar.
- –
En nuestro país, García-Vidal et al.17 evaluaron el impacto del uso de corticoides sistémicos en 308 pacientes, y no observaron diferencias significativas en la mortalidad intrahospitalaria, aunque sí encontraron un cierto efecto protector de estos fármacos en el análisis de regresión logística. En este caso, los corticoides se emplearon fundamentalmente como tratamiento del broncoespasmo asociado a la infección respiratoria.
En los últimos años se han llevado a cabo varios metaanálisis para poner en conjunto los datos de los diferentes estudios realizados. Así, Gorman et al.18 concluyeron que el tratamiento con esteroides no está recomendado en el tratamiento de la NAC debido al pequeño tamaño muestral de los ensayos publicados y a la existencia de errores metodológicos. Sin embargo, Lamontagne et al.19 sugirieron que el tratamiento con dosis bajas administradas durante los 14 primeros días de la enfermedad, reducían la mortalidad de la neumonía grave, aunque admitieron que el nivel de recomendación era débil, debido a las limitaciones anteriormente comentadas por otros autores.
Recientemente se han publicado algunos trabajos que han aportado nuevos datos:
- –
Así, Snijders et al.20 realizaron un ensayo randomizado, en el que analizaron 213 pacientes (a 104 de ellos se les administró una media de 40mg de metilprednisolona diarios durante 7 días) y, concluyeron que el tratamiento con corticosteroides no mejoraba la evolución de la enfermedad. De hecho, estos autores encontraron una asociación entre el uso de estos fármacos y el fracaso tardío del tratamiento, lo que pusieron en relación con un posible efecto rebote de la respuesta inflamatoria tras la suspensión de los esteroides.
- –
Salluh et al.21 realizaron un estudio de cohortes en pacientes con NAC ingresados en Unidades de Cuidados Intensivos (UCI), y sometidos a ventilación mecánica invasiva. En el se analizaron un total de 111 pacientes, de los que el 55% recibieron corticoides sistémicos, equivalentes a 60mg de metilprednisolona diarios durante 7 días. Dicho tratamiento no se asoció a una menor mortalidad hospitalaria (29,5 vs 32% en los pacientes no tratados; p=0,837), pero sí a una mayor estancia, tanto en la UCI (15 vs 11 días; p=0,003), como hospitalaria global (20 vs 14 días; p=0,023).
- –
En nuestro entorno Fernández-Serrano et al.22 han publicado recientemente los resultados de un ensayo randomizado en el que se incluyeron 56 pacientes. El 50% de ellos fue tratado con un bolo de 200mg de metilprednisolona antes de iniciar el tratamiento antibiótico, y posteriormente con una pauta de 20mg cada 6h durante 3 días, seguida de 20mg cada 12h durante otros 3 días, y finalmente con 20mg al día durante 3 días más. Estos autores no detectaron diferencias significativas entre los grupos respecto a la necesidad de ventilación invasiva (objetivo primario del estudio), la mortalidad hospitalaria, ni los días de estancia.
- –
En uno de los trabajos más recientemente publicados, Meijvis et al.23 analizaron el efecto de la administración de dexametasona en la evolución de los pacientes ingresados con NAC grave (PSI IV y V). Se aleatorizaron 304 pacientes, de los cuales 151 recibieron un bolo de 5mg de dexametasona intravenosa, seguido de 5mg/día durante 3 días. Se detectó una reducción estadísticamente significativa de la duración del ingreso hospitalario en la cohorte tratada con corticoides (6,5 vs 7,5 días; p=0,048). Sin embargo, no hubo diferencias en la mortalidad hospitalaria (5% en ambos grupos; p=0,98) ni a los 30 días del alta (6% en el grupo tratado vs 7% en el grupo control; p=0,68).
En nuestro estudio, el tratamiento con corticoides no disminuyó la mortalidad de una forma significativa en ninguno de los 3 puntos de corte analizados. La principal indicación para su uso fue la existencia de broncoespasmo, y por ello se emplearon de forma significativamente mayor en los pacientes diagnosticados previamente de EPOC. Las diferencias encontradas en relación con los ensayos clínicos previos pueden deberse, al menos en parte, a que en estos, la administración de corticoides se hizo de forma aleatoria. Sin embargo, en nuestro estudio se administró dicho tratamiento a los pacientes que probablemente padecían infecciones más graves, lo que justificaría la similitud de nuestros resultados con los del estudio, también observacional, del grupo español de García-Vidal et al.17.
El principal factor asociado a la mortalidad temprana fue una puntuación alta en la escala PSI, que ponemos en relación con la gravedad del episodio infeccioso. Por otra parte, en los pacientes con una mayor puntuación (>3) en el índice de Charlson y en los que presentaban deterioro cognitivo, se detectó un aumento de la mortalidad tardía, en probable relación con su afección de base.
Entre las fortalezas de nuestro trabajo se encuentran el elevado tamaño muestral, y el hecho de que se ha realizado en condiciones de práctica clínica habitual en nuestro entorno. Entre sus limitaciones cabe destacar que es un estudio observacional en el que no se ha realizado ningún tipo de intervención. Tampoco se ha cuantificado la dosis acumulada ni la duración total del tratamiento con corticoides, ni se ha evaluado la función suprarrenal de los pacientes.
En conclusión, los resultados de este estudio no apoyan el uso de corticoides sistémicos de forma rutinaria en el tratamiento de la NAC.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.