Introducción
La enfermedad pulmonar obstructiva crónica (EPOC) es la principal causa neumológica de morbimortalidad en el mundo. En España la padece un 9% de los individuos mayores de 40 años y un 20% de los mayores de 65 años1. Supone la quinta causa de muerte entre los varones y la séptima entre las mujeres, con un aumento progresivo a lo largo de los últimos 10 años2. Esta enfermedad se ha situado entre las de máximo interés sanitario, tanto por los aspectos epidemiológicos anteriormente señalados como por los económicos, ya que la EPOC supone un importante gasto sanitario, directo e indirecto, así como un considerable empleo de recursos para cualquier sistema nacional de salud3.
La EPOC es un proceso que se caracteriza por una limitación permanente y progresiva del flujo aéreo, generalmente irreversible, causada por anormalidades de las vías aéreas (bronquitis crónica) y del parénquima pulmonar (enfisema pulmonar)4,5 que afecta seriamente la vida del paciente. La bronquitis crónica es el trastorno predominante en un 85% de estos enfermos. Clásicamente se define por la presencia de tos y expectoración durante más de tres meses al año y más de dos años consecutivos6. En la historia natural de la bronquitis crónica son frecuentes los episodios de agudización, con una media que oscila entre las dos y tres exacerbaciones anuales por paciente7. Estas agudizaciones pueden ser la consecuencia de infecciones víricas o bacterianas, de la polución ambiental (incluyendo el hábito tabáquico), de procesos alérgicos, de una irritación química de las vías aéreas o de otras diversas causas. Aunque se discute el papel de las infecciones bacterianas en estas agudizaciones los estudios broncoscópicos han demostrado que hasta un 50% de los pacientes presenta concentraciones elevadas de estos microorganismos en las vías respiratorias bajas8-10. La frecuencia de estos episodios de infección respiratoria se ha asociado con la progresión del deterioro de la función ventilatoria que caracteriza a la EPOC11, y por tanto, con la afectación, transitoria o permanente, de la calidad de vida de estos enfermos. De hecho, casi el 50% de los pacientes dados de alta tras una de estas agudizaciones requiere asistencia sanitaria en más de una ocasión durante los 6 meses siguientes de dicho alta12.
De lo anteriormente expuesto se deduce que la prevención y el tratamiento de los episodios de agudización infecciosa son el objetivo fundamental de la actuación médica en los pacientes que padecen una EPOC. La única medida terapéutica empleada actualmente con este fin durante las crisis de agudización es la antibioticoterapia, que en España se prescribe de forma empírica en más del 90% de estos casos13. Sin embargo, la antibioticoterapia no ha demostrado tener impacto alguno sobre la progresión de la enfermedad. Además, el uso frecuente e indiscriminado de los antibióticos favorece la selección de bacterias resistentes14. Ante esta situación se han planteado diversas alternativas terapéuticas, entre las que se encuentra la administración de los inmunomoduladores15,16. Recientemente se ha comprobado que la EPOC se asocia a diversas alteraciones en la inmunidad natural y adquirida que pueden relacionarse con el mantenimiento del estado inflamatorio y con la predisposición a contraer infecciones en el tracto respiratorio17,18. El intento de normalizar estas deficiencias en las funciones del sistema inmune en los pacientes con una EPOC justifica el empleo de los inmunomoduladores. El objetivo buscado es el de disminuir la alta predisposición de estos pacientes a las infecciones respiratorias, el de prevenir las agudizaciones y el de mejorar la calidad de vida de los enfermos.
AM3 (Inmunoferón®, Industrial Farmacéutica Cantabria, S. A.) es un inmunomodulador oral que ha demostrado capacidad para normalizar la función efectora de las células accesorias (sistema monocito-macrófago), de las células citotóxicas espontáneas (natural killer o NK) y de los linfocitos T. Simultáneamente, este fármaco inhibe la producción del factor de necrosis tumoral alfa (TNF-α), manteniendo o estimulando la de otras citocinas, como el interferón gamma o los receptores solubles del TNF-α 19. AM3 se ha empleado en enfermedades diversas, caracterizadas por un estado inflamatorio y/o infeccioso crónico, tales como la insuficiencia renal en hemodiálisis, la hepatitis crónica por virus B y la inflamación muscular. En la EPOC, AM3 ha demostrado que normaliza la función de las células fagocíticas, de las células NK16,19 y de los linfocitos T (observaciones no publicadas). En varios estudios clínicos se ha investigado el efecto de AM3 sobre las agudizaciones y el uso de antibióticos en los pacientes que padecen una EPOC. En este trabajo se realiza una revisión sistemática de estos estudios.
Métodos
Se ha efectuado una búsqueda sistemática de todos los informes de estudios clínicos controlados, publicados o sin publicar, en MEDLINE (desde 1966), CINAHL (desde 1974), HEALTHStar (desde 1975), EMBASE (desde 1980), Cochrane Library (desde marzo de 1998), así como de los aportados por la compañía titular de esta especialidad farmacéutica (Industrial Farmacéutica Cantabria, S. A.) hasta marzo de 1999. Los términos empleados para realizar la búsqueda han sido los siguientes: inmunoferón, immunoferon, AM3 y glycophosphopeptical.
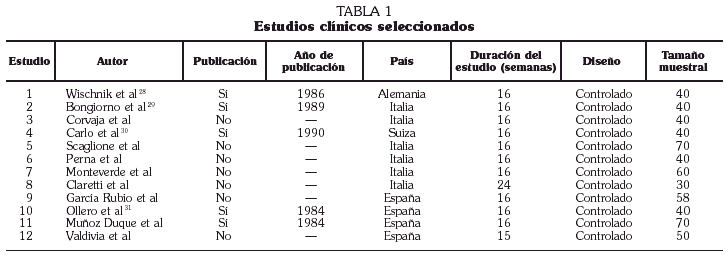
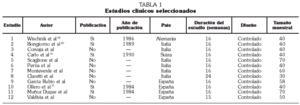
Los estudios clínicos se incluyeron en esta revisión si eran controlados, si se disponía de sus informes completos, publicados o no, si se empleaba AM3 en uno de los grupos de tratamiento y si contenían datos sobre los efectos de esta especialidad farmacéutica en pacientes con una EPOC. De igual forma se excluyeron los estudios de los que sólo se localizaron los resúmenes de sus informes, los que carecían de un grupo control de tratamiento y los que únicamente aportaban información sobre efectos adversos, datos farmacocinéticos o resultados inmunológicos. De acuerdo con estos criterios se localizó un total de 12 estudios (tabla 1).
Los protocolos de los estudios encontrados presentaban criterios de inclusión de pacientes y pautas de tratamiento que eran, en general, similares, es decir, enfermos de edad avanzada diagnosticados de EPOC que seguían tratamiento con AM3 o con un placebo a dosis de 500 mg cada 8 horas durante 4 meses. En atención a estos criterios el estudio 11 no se seleccionó ya que en él sólo se incluyó a pacientes mayores de 65 años de edad (criterio mucho más restrictivo que el del resto de los estudios) y porque, a partir del segundo mes de tratamiento, la dosis se redujo a 500 mg cada 12 horas.
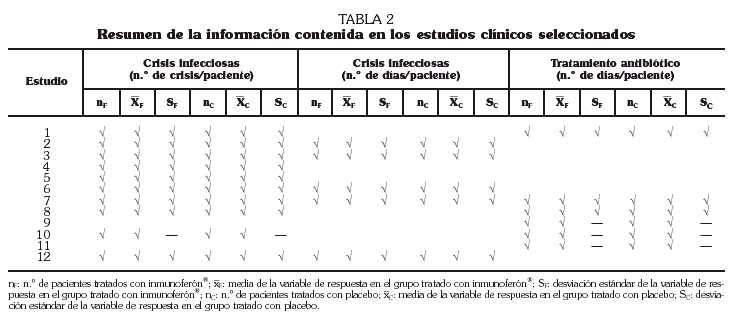
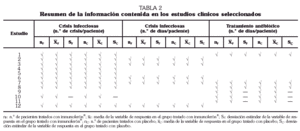
En los estudios revisados las variables seleccionadas para estimar la eficacia del tratamiento fueron el número de agudizaciones infecciosas, la duración de la exacerbación y la duración del tratamiento antibiótico empleado. En consideración a estos criterios se eliminaron los estudios 9 y 10 al no contener la información de referencia (tabla 2).
Los datos extraídos de los estudios aportaron información sobre las características generales de los ensayos, la población estudiada, los problemas clínicos de los pacientes, los tratamientos recibidos antes y durante los estudios, el desenlace del episodio, la calidad metodológica20,21 y la cantidad de información incluida en los informes22.
El análisis de los datos se ha realizado empleando una variante del método de las varianzas o método de Wolf. Con este análisis se han obtenido los estimadores del efecto a través de las diferencias entre las medias de los grupos (AM3 y placebo), ponderadas por el inverso de la varianza combinada de ambos grupos. Esta estimación sigue una ley normal, pudiéndose calcular el intervalo de confianza y comprobar la significación del estimador obtenido frente a la hipótesis nula de no efecto.
Asimismo se ha contrastado la homogeneidad entre los resultados de los estudios incluidos en esta revisión mediante la determinación de un estadístico calculado por la diferencia estimada en cada grupo, respecto al estimador global al cuadrado, ponderada por el inverso de la varianza definida previamente. Este estadístico sigue una distribución Chi cuadrado con k-1 grados de libertad, siendo k el número de estudios incluidos.
Resultados
Partiendo de las medias y desviaciones estándar de cada una de las variables seleccionadas para cada grupo de tratamiento (AM3 y placebo) e incluyendo en cada análisis los estudios que proporcionaron la información necesaria se calcularon los estimadores del efecto, obteniéndose los intervalos de confianza y su significación estadística. Asimismo se comprobó la homogeneidad entre los estudios para cada una de las variables elegidas.
Para evaluar la ganancia en la precisión, al considerar el estimador de efecto global, se han representado gráficamente los valores de la diferencia de medias, con su desviación estándar, en cada estudio, frente a las obtenidas en el metaanálisis para cada variable seleccionada.
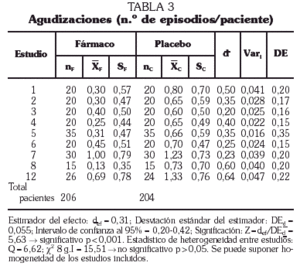
Agudizaciones
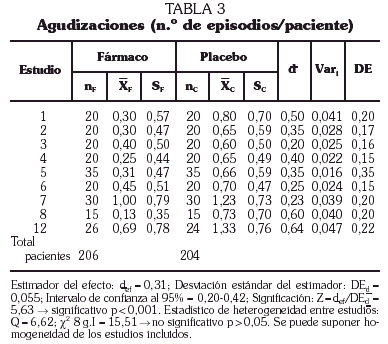
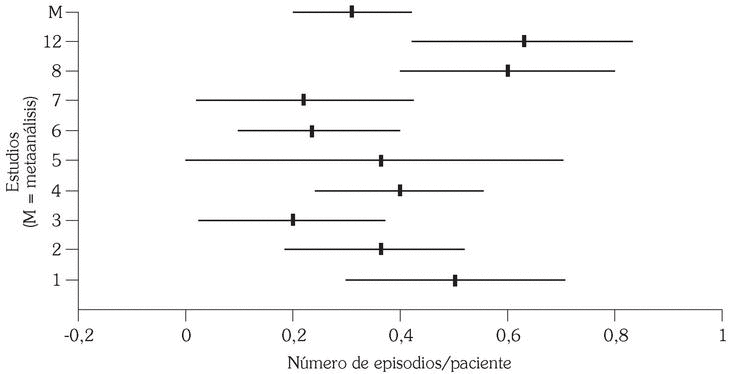
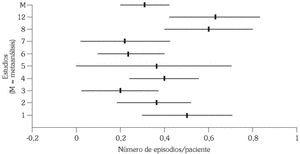
El número medio de agudizaciones sufridas por los pacientes incluidos en los estudios seleccionados disminuye, según el estimador del efecto, en 0,31 unidades (p < 0,001; intervalo de confianza al 95%: 0,20-0,42). Este valor se ha estimado para un total de 206 y 204 pacientes por grupo de tratamiento (AM3 y placebo, respectivamente) (tabla 3 y fig. 1).
Fig. 1. Disminución en el número de agudizaciones.
Al no encontrarse heterogeneidad entre los efectos de los diferentes estudios (Q = 6,62; p > 0,43) puede concluirse que, efectivamente, existe un efecto positivo en lo que se refiere al número de agudizaciones padecidas por cada paciente a favor del grupo tratado con AM3 frente al grupo placebo.
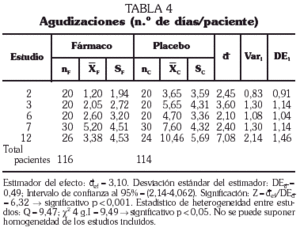
Duración de las agudizaciones
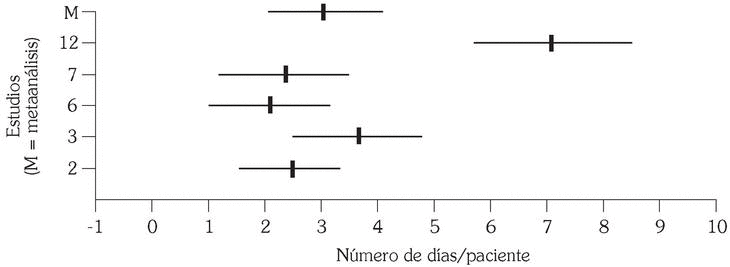
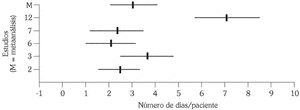
La duración media de las agudizaciones sufridas por los pacientes incluidos en los mencionados estudios disminuye, según el estimador del efecto, 3,10 días (p < 0,001; intervalo de confianza al 95%: 2,14-4,06). Este valor se ha estimado para un total de 116 y 114 pacientes por grupo de tratamiento (AM3 y placebo, respectivamente) (tabla 4 y fig. 2).
Fig. 2. Disminución en la duración en días de las agudizaciones.
Al contrastar la homogeneidad entre los efectos de los estudios incluidos en esta revisión se han obtenido resultados estadísticamente significativos (Q = 9,47; p < 0,05). Por tanto, aunque existen diferencias significativas en la duración de las agudizaciones a favor del grupo de pacientes tratados con AM3, no puede confirmarse este efecto positivo al tratarse de estudios cercanos a la heterogeneidad.
Tratamiento antibiótico
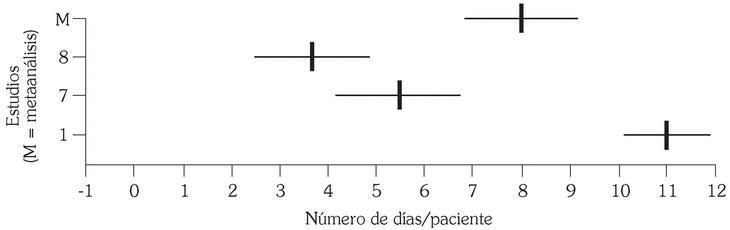
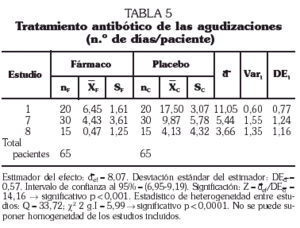
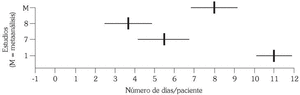
La duración media del tratamiento antibiótico pautado en estas agudizaciones se reduce, según el estimador del efecto, 8,07 días (p < 0,001; intervalo de confianza al 95%: 6,95-9,19) para los pacientes incluidos en el grupo de tratamiento con AM3 frente a los del grupo placebo. Esta estimación se ha realizado con un total de 65 pacientes por grupo de tratamiento (tabla 5 y fig. 3). A pesar de estos resultados, cuando se contrasta la homogeneidad de estos estudios se encuentran diferencias significativas (Q = 33,72; p < 0,0001) que invalidan la suposición de homogeneidad entre ellos y el efecto positivo hallado.
Fig. 3. Disminución en la duración en días del tratamiento antibiótico.
Discusión
Los resultados de esta revisión sistemática muestran que AM3 tiene un efecto clínico en la prevención de las agudizaciones que sufren los pacientes afectos de una EPOC, al reducir significativamente su número. Esta disminución en el número de agudizaciones anuales que experimentan estos pacientes podría relacionarse con un enlentecimiento de la progresión del deterioro de la función respiratoria11 y con un potencial impacto en la calidad de vida de los enfermos12.
La disminución en la frecuencia de agudizaciones de los pacientes con una EPOC tratados con AM3 también podría relacionarse con el uso de antibióticos. En las agudizaciones suele ser práctica clínica habitual la antibioticoterapia empírica, ya que no se dispone de métodos rápidos y eficientes para llegar a un diagnóstico etiológico13,23. Una reducción significativa en el número de agudizaciones supone un resultado terapéutico positivo y un posible menor desarrollo de resistencias bacterianas que se produce por el uso frecuente e indiscriminado de estos fármacos14.
La EPOC es un proceso de elevada prevalencia en la población general. Los pacientes que la padecen presentan, como media, entre dos y tres exacerbaciones anuales, lo que hace que esta enfermedad tenga una importante repercusión social y económica23. El fracaso del tratamiento de las agudizaciones incrementa aún más su coste debido esencialmente a que este hecho se asocia con un mayor número de ingresos hospitalarios y de consultas médicas ambulatorias, así como a la necesidad de emplear nuevos tratamientos antibióticos24,25.
Los resultados encontrados en esta revisión deben ponerse en relación con los obtenidos en los ensayos clínicos de AM3 realizados en pacientes con EPOC y en los que se analizan sus efectos biológicos16,19. La demostrada capacidad restauradora de la función efectora de las células fagocíticas y de las NK que tiene AM3 podría relacionarse con la mayor resistencia de estos pacientes al desarrollo de complicaciones infecciosas del tracto respiratorio. Además, los efectos inmunomoduladores de AM3 sobre los linfocitos T también pudieran inducir una mejor respuesta del paciente a las infecciones, fundamentalmente víricos. Asimismo debe señalarse que el efecto antiinflamatorio de AM3, mediado a través de la inhibición de la producción de TNF-α y la inducción de sus receptores solubles, pudiera estar implicado en una disminución de la reacción inflamatoria de la mucosa respiratoria que caracteriza a estos pacientes. Por tanto, parece posible relacionar el menor número de agudizaciones que padecen los pacientes con una EPOC tratados con AM3 con el efecto inmunomodulador de este fármaco.
Los resultados de futuros ensayos clínicos controlados deben servir para valorar la eficacia de AM3 en la prevención y el tratamiento de las agudizaciones de los pacientes que padecen una EPOC.
AGRADECIMIENTOS
A Francisca Ríus, del Departamento de Bioestadística de la Facultad de Medicina de la Universidad de Málaga.