Share
array:24 [
"pii" => "S0014256523001893"
"issn" => "00142565"
"doi" => "10.1016/j.rce.2023.11.001"
"estado" => "S300"
"fechaPublicacion" => "2023-12-01"
"aid" => "2145"
"copyright" => "Elsevier España, S.L.U. and Sociedad Española de Medicina Interna (SEMI)"
"copyrightAnyo" => "2023"
"documento" => "article"
"crossmark" => 1
"subdocumento" => "rev"
"cita" => "Rev Clin Esp. 2023;223:629-39"
"abierto" => array:3 [
"ES" => false
"ES2" => false
"LATM" => false
]
"gratuito" => false
"lecturas" => array:1 [
"total" => 0
]
"Traduccion" => array:1 [
"en" => array:19 [
"pii" => "S2254887423001236"
"issn" => "22548874"
"doi" => "10.1016/j.rceng.2023.11.001"
"estado" => "S300"
"fechaPublicacion" => "2023-12-01"
"aid" => "2145"
"copyright" => "Elsevier España, S.L.U. and Sociedad Española de Medicina Interna (SEMI)"
"documento" => "article"
"crossmark" => 1
"subdocumento" => "rev"
"cita" => "Rev Clin Esp. 2023;223:629-39"
"abierto" => array:3 [
"ES" => false
"ES2" => false
"LATM" => false
]
"gratuito" => false
"lecturas" => array:1 [
"total" => 0
]
"en" => array:13 [
"idiomaDefecto" => true
"cabecera" => "<span class="elsevierStyleTextfn">Review</span>"
"titulo" => "Treatment of systemic lupus erythematosus: new therapeutic options"
"tienePdf" => "en"
"tieneTextoCompleto" => "en"
"tieneResumen" => array:2 [
0 => "en"
1 => "es"
]
"paginas" => array:1 [
0 => array:2 [
"paginaInicial" => "629"
"paginaFinal" => "639"
]
]
"titulosAlternativos" => array:1 [
"es" => array:1 [
"titulo" => "Tratamiento del lupus eritematoso sistémico: nuevas opciones terapéuticas"
]
]
"contieneResumen" => array:2 [
"en" => true
"es" => true
]
"contieneTextoCompleto" => array:1 [
"en" => true
]
"contienePdf" => array:1 [
"en" => true
]
"resumenGrafico" => array:2 [
"original" => 0
"multimedia" => array:8 [
"identificador" => "fig0005"
"etiqueta" => "Figure 1"
"tipo" => "MULTIMEDIAFIGURA"
"mostrarFloat" => true
"mostrarDisplay" => false
"figura" => array:1 [
0 => array:4 [
"imagen" => "gr1.jpeg"
"Alto" => 1479
"Ancho" => 2925
"Tamanyo" => 373784
]
]
"detalles" => array:1 [
0 => array:3 [
"identificador" => "at0380"
"detalle" => "Figure "
"rol" => "short"
]
]
"descripcion" => array:1 [
"en" => "<p id="spar0005" class="elsevierStyleSimplePara elsevierViewall">Proposed treatment for lupus nephritis (III, IV+/−V).</p>"
]
]
]
"autores" => array:1 [
0 => array:2 [
"autoresLista" => "A. González-García, I. Cusácovich, G. Ruiz-Irastorza"
"autores" => array:3 [
0 => array:2 [
"nombre" => "A."
"apellidos" => "González-García"
]
1 => array:2 [
"nombre" => "I."
"apellidos" => "Cusácovich"
]
2 => array:2 [
"nombre" => "G."
"apellidos" => "Ruiz-Irastorza"
]
]
]
]
]
"idiomaDefecto" => "en"
"Traduccion" => array:1 [
"es" => array:9 [
"pii" => "S0014256523001893"
"doi" => "10.1016/j.rce.2023.11.001"
"estado" => "S300"
"subdocumento" => ""
"abierto" => array:3 [
"ES" => false
"ES2" => false
"LATM" => false
]
"gratuito" => false
"lecturas" => array:1 [
"total" => 0
]
"idiomaDefecto" => "es"
"EPUB" => "https://multimedia.elsevier.es/PublicationsMultimediaV1/item/epub/S0014256523001893?idApp=WRCEE"
]
]
"EPUB" => "https://multimedia.elsevier.es/PublicationsMultimediaV1/item/epub/S2254887423001236?idApp=WRCEE"
"url" => "/22548874/0000022300000010/v1_202312120705/S2254887423001236/v1_202312120705/en/main.assets"
]
]
"itemSiguiente" => array:19 [
"pii" => "S0014256523001649"
"issn" => "00142565"
"doi" => "10.1016/j.rce.2023.09.001"
"estado" => "S300"
"fechaPublicacion" => "2023-12-01"
"aid" => "2138"
"copyright" => "Elsevier España, S.L.U. and Sociedad Española de Medicina Interna (SEMI)"
"documento" => "simple-article"
"crossmark" => 1
"subdocumento" => "crp"
"cita" => "Rev Clin Esp. 2023;223:640-6"
"abierto" => array:3 [
"ES" => false
"ES2" => false
"LATM" => false
]
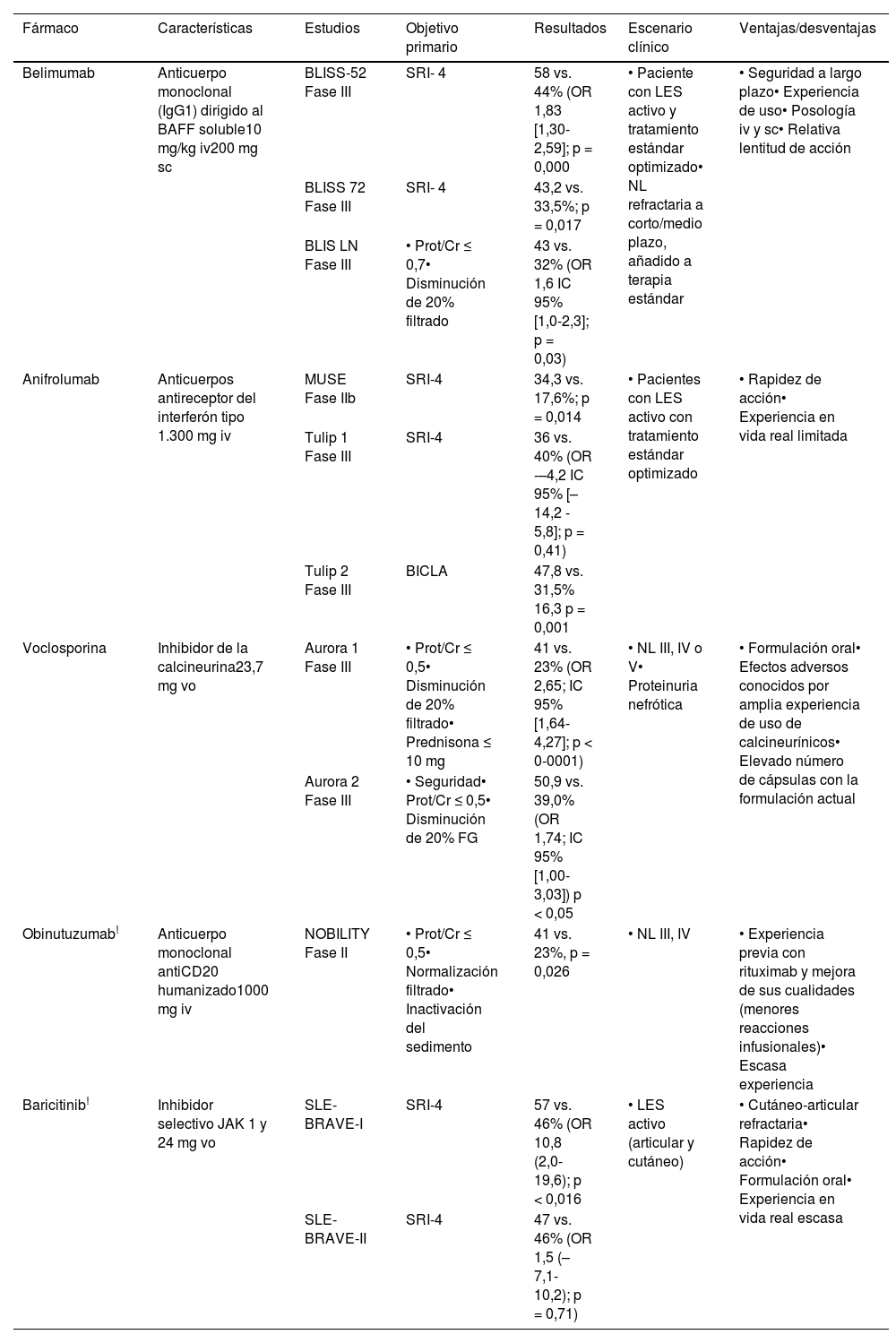
"gratuito" => false
"lecturas" => array:1 [
"total" => 0
]
"es" => array:12 [
"idiomaDefecto" => true
"cabecera" => "<span class="elsevierStyleTextfn">Original Breve</span>"
"titulo" => "Valoración nutricional por ecografía del recto femoral y el tejido adiposo preperitoneal como predictores del riesgo de complicaciones del paciente hospitalizado"
"tienePdf" => "es"
"tieneTextoCompleto" => "es"
"tieneResumen" => array:2 [
0 => "es"
1 => "en"
]
"paginas" => array:1 [
0 => array:2 [
"paginaInicial" => "640"
"paginaFinal" => "646"
]
]
"titulosAlternativos" => array:1 [
"en" => array:1 [
"titulo" => "Nutritional assessment by ultrasound of the rectus femoris and preperitoneal adipose tissue as predictors of hospitalized patient complications"
]
]
"contieneResumen" => array:2 [
"es" => true
"en" => true
]
"contieneTextoCompleto" => array:1 [
"es" => true
]
"contienePdf" => array:1 [
"es" => true
]
"autores" => array:1 [
0 => array:2 [
"autoresLista" => "R. Marín-Baselga, C. Sanz-Ortega, L. Platero-Dueñas, R. Sorriguieta-Torre, S. Palma-Milla, Y. Tung-Chen"
"autores" => array:6 [
0 => array:2 [
"nombre" => "R."
"apellidos" => "Marín-Baselga"
]
1 => array:2 [
"nombre" => "C."
"apellidos" => "Sanz-Ortega"
]
2 => array:2 [
"nombre" => "L."
"apellidos" => "Platero-Dueñas"
]
3 => array:2 [
"nombre" => "R."
"apellidos" => "Sorriguieta-Torre"
]
4 => array:2 [
"nombre" => "S."
"apellidos" => "Palma-Milla"
]
5 => array:2 [
"nombre" => "Y."
"apellidos" => "Tung-Chen"
]
]
]
]
]
"idiomaDefecto" => "es"
"Traduccion" => array:1 [
"en" => array:9 [
"pii" => "S2254887423001121"
"doi" => "10.1016/j.rceng.2023.10.002"
"estado" => "S300"
"subdocumento" => ""
"abierto" => array:3 [
"ES" => false
"ES2" => false
"LATM" => false
]
"gratuito" => false
"lecturas" => array:1 [
"total" => 0
]
"idiomaDefecto" => "en"
"EPUB" => "https://multimedia.elsevier.es/PublicationsMultimediaV1/item/epub/S2254887423001121?idApp=WRCEE"
]
]
"EPUB" => "https://multimedia.elsevier.es/PublicationsMultimediaV1/item/epub/S0014256523001649?idApp=WRCEE"
"url" => "/00142565/0000022300000010/v1_202312070441/S0014256523001649/v1_202312070441/es/main.assets"
]
"itemAnterior" => array:19 [
"pii" => "S0014256523001881"
"issn" => "00142565"
"doi" => "10.1016/j.rce.2023.10.002"
"estado" => "S300"
"fechaPublicacion" => "2023-12-01"
"aid" => "2144"
"copyright" => "Elsevier España, S.L.U. and Sociedad Española de Medicina Interna (SEMI)"
"documento" => "article"
"crossmark" => 1
"subdocumento" => "rev"
"cita" => "Rev Clin Esp. 2023;223:619-28"
"abierto" => array:3 [
"ES" => false
"ES2" => false
"LATM" => false
]
"gratuito" => false
"lecturas" => array:1 [
"total" => 0
]
"es" => array:13 [
"idiomaDefecto" => true
"cabecera" => "<span class="elsevierStyleTextfn">REVISIÓN</span>"
"titulo" => "Nueva era de la medicina basada en las células madre mesenquimales: bases, retos y perspectivas"
"tienePdf" => "es"
"tieneTextoCompleto" => "es"
"tieneResumen" => array:2 [
0 => "es"
1 => "en"
]
"paginas" => array:1 [
0 => array:2 [
"paginaInicial" => "619"
"paginaFinal" => "628"
]
]
"titulosAlternativos" => array:1 [
"en" => array:1 [
"titulo" => "New era of mesenchymal stem cell-based medicine: Basis, challenges and prospects"
]
]
"contieneResumen" => array:2 [
"es" => true
"en" => true
]
"contieneTextoCompleto" => array:1 [
"es" => true
]
"contienePdf" => array:1 [
"es" => true
]
"resumenGrafico" => array:2 [
"original" => 0
"multimedia" => array:7 [
"identificador" => "fig0020"
"etiqueta" => "Figura 4"
"tipo" => "MULTIMEDIAFIGURA"
"mostrarFloat" => true
"mostrarDisplay" => false
"figura" => array:1 [
0 => array:4 [
"imagen" => "gr4.jpeg"
"Alto" => 1111
"Ancho" => 2925
"Tamanyo" => 223711
]
]
"descripcion" => array:1 [
"es" => "<p id="spar0055" class="elsevierStyleSimplePara elsevierViewall">Representación gráfica de la obtención de medio condicionado y microvesículas de las CMM y expansión industrial mediante biorreactores.</p> <p id="spar0060" class="elsevierStyleSimplePara elsevierViewall">CMM: células madre mesenquimales.</p>"
]
]
]
"autores" => array:1 [
0 => array:2 [
"autoresLista" => "F.J. Vizoso, L.A. Costa, N. Eiro"
"autores" => array:3 [
0 => array:2 [
"nombre" => "F.J."
"apellidos" => "Vizoso"
]
1 => array:2 [
"nombre" => "L.A."
"apellidos" => "Costa"
]
2 => array:2 [
"nombre" => "N."
"apellidos" => "Eiro"
]
]
]
]
]
"idiomaDefecto" => "es"
"Traduccion" => array:1 [
"en" => array:9 [
"pii" => "S2254887423001248"
"doi" => "10.1016/j.rceng.2023.11.002"
"estado" => "S300"
"subdocumento" => ""
"abierto" => array:3 [
"ES" => false
"ES2" => false
"LATM" => false
]
"gratuito" => false
"lecturas" => array:1 [
"total" => 0
]
"idiomaDefecto" => "en"
"EPUB" => "https://multimedia.elsevier.es/PublicationsMultimediaV1/item/epub/S2254887423001248?idApp=WRCEE"
]
]
"EPUB" => "https://multimedia.elsevier.es/PublicationsMultimediaV1/item/epub/S0014256523001881?idApp=WRCEE"
"url" => "/00142565/0000022300000010/v1_202312070441/S0014256523001881/v1_202312070441/es/main.assets"
]
"es" => array:19 [
"idiomaDefecto" => true
"cabecera" => "<span class="elsevierStyleTextfn">REVISIÓN</span>"
"titulo" => "Tratamiento del lupus eritematoso sistémico: nuevas opciones terapéuticas"
"tieneTextoCompleto" => true
"paginas" => array:1 [
0 => array:2 [
"paginaInicial" => "629"
"paginaFinal" => "639"
]
]
"autores" => array:1 [
0 => array:4 [
"autoresLista" => "A. González-García, I. Cusácovich, G. Ruiz-Irastorza"
"autores" => array:3 [
0 => array:4 [
"nombre" => "A."
"apellidos" => "González-García"
"email" => array:1 [
0 => "andres.gonzalez@salud.madrid.org"
]
"referencia" => array:2 [
0 => array:2 [
"etiqueta" => "<span class="elsevierStyleSup">a</span>"
"identificador" => "aff0005"
]
1 => array:2 [
"etiqueta" => "<span class="elsevierStyleSup">*</span>"
"identificador" => "cor0005"
]
]
]
1 => array:3 [
"nombre" => "I."
"apellidos" => "Cusácovich"
"referencia" => array:1 [
0 => array:2 [
"etiqueta" => "<span class="elsevierStyleSup">b</span>"
"identificador" => "aff0010"
]
]
]
2 => array:3 [
"nombre" => "G."
"apellidos" => "Ruiz-Irastorza"
"referencia" => array:1 [
0 => array:2 [
"etiqueta" => "<span class="elsevierStyleSup">c</span>"
"identificador" => "aff0015"
]
]
]
]
"afiliaciones" => array:3 [
0 => array:3 [
"entidad" => "Unidad de Enfermedades Autoinmunes Sistémicas, Servicio de Medicina Interna, Hospital Universitario Ramón y Cajal, IRYCIS, Madrid, España"
"etiqueta" => "a"
"identificador" => "aff0005"
]
1 => array:3 [
"entidad" => "Servicio de Medicina Interna, Hospital Clínico Universitario de Valladolid, Valladolid, España"
"etiqueta" => "b"
"identificador" => "aff0010"
]
2 => array:3 [
"entidad" => "Unidad de Enfermedades Autoinmunes, Servicio de Medicina Interna, BioCruces Bizkaia Health Research Institute, Hospital Universitario Cruces, UPV/EHU, Barakaldo, Bizkaia, España"
"etiqueta" => "c"
"identificador" => "aff0015"
]
]
"correspondencia" => array:1 [
0 => array:3 [
"identificador" => "cor0005"
"etiqueta" => "⁎"
"correspondencia" => "Autor para correspondencia."
]
]
]
]
"titulosAlternativos" => array:1 [
"en" => array:1 [
"titulo" => "Treatment of systemic lupus erythematosus: New therapeutic options"
]
]
"resumenGrafico" => array:2 [
"original" => 0
"multimedia" => array:7 [
"identificador" => "fig0005"
"etiqueta" => "Figura 1"
"tipo" => "MULTIMEDIAFIGURA"
"mostrarFloat" => true
"mostrarDisplay" => false
"figura" => array:1 [
0 => array:4 [
"imagen" => "gr1.jpeg"
"Alto" => 1479
"Ancho" => 2925
"Tamanyo" => 316698
]
]
"descripcion" => array:1 [
"es" => "<p id="spar0015" class="elsevierStyleSimplePara elsevierViewall">Propuesta de tratamiento para la nefritis lúpica (III, IV+/-V).</p>"
]
]
]
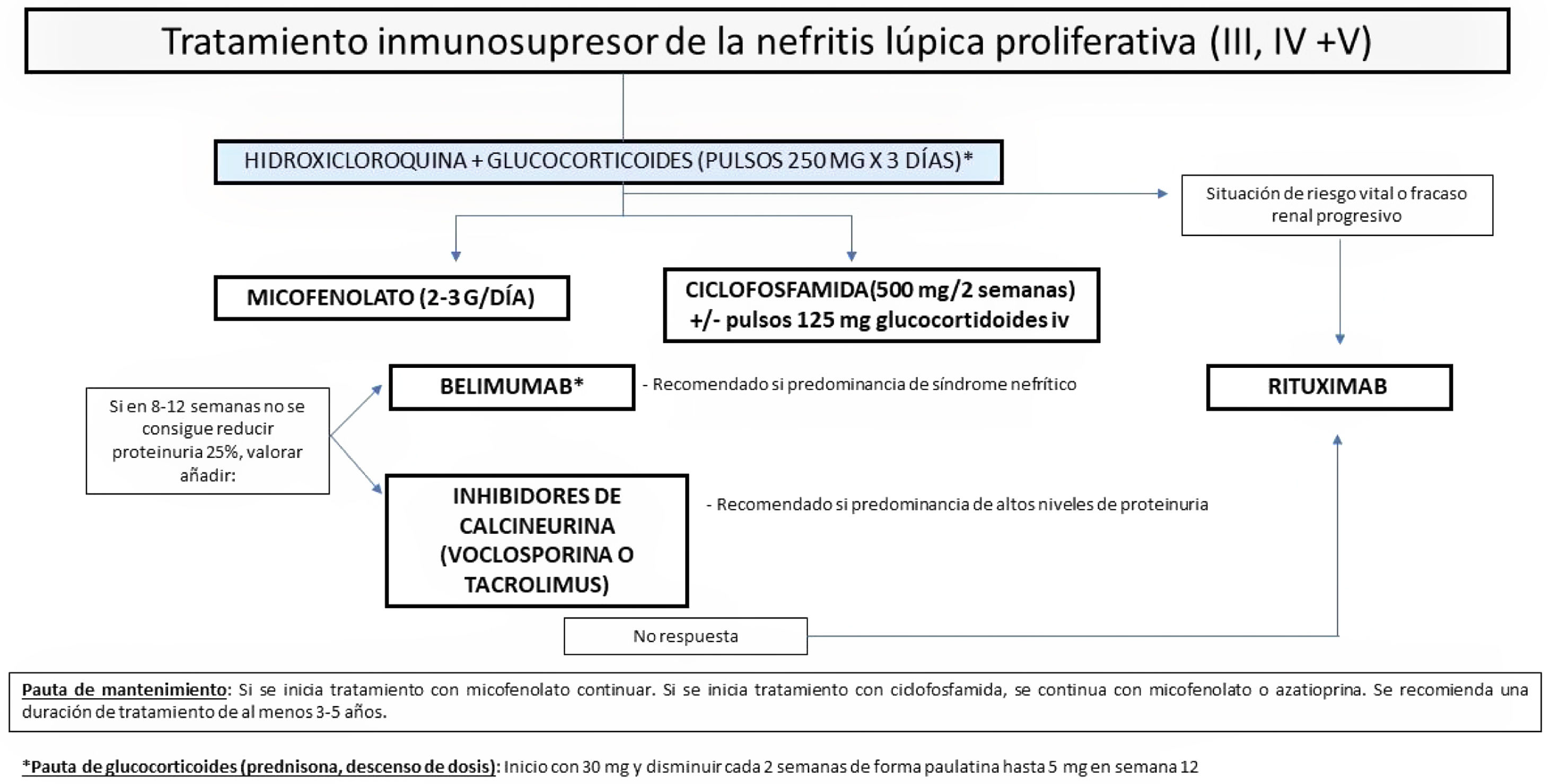
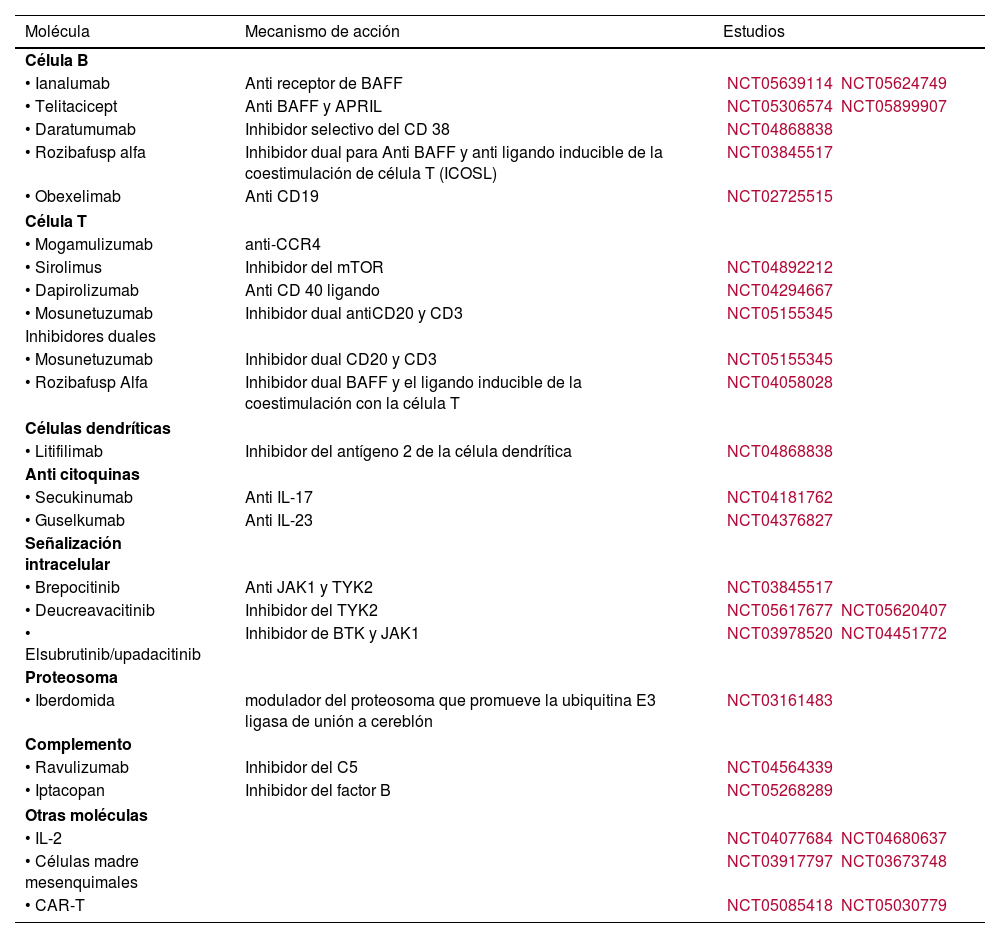
"textoCompleto" => "<span class="elsevierStyleSections"><span id="sec0005" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0025">Introducción</span><p id="par0005" class="elsevierStylePara elsevierViewall">El lupus eritematoso sistémico (LES) es una enfermedad inflamatoria autoinmune que se caracteriza por un amplio espectro de manifestaciones clínicas, analíticas e inmunológicas, y que se presenta con diversos fenotipos y en brotes<a class="elsevierStyleCrossRef" href="#bib0405"><span class="elsevierStyleSup">1</span></a>. El principal rasgo de la enfermedad es la presencia de autoanticuerpos derivados de la perpetuación de la pérdida de tolerancia con linfocitos autorreactivos<a class="elsevierStyleCrossRef" href="#bib0410"><span class="elsevierStyleSup">2</span></a>. La causa es desconocida, aunque la genética, sobre todo con la descripción reciente en una paciente con LES de una variante patogénica con ganancia de función en el gen TLR7<a class="elsevierStyleCrossRef" href="#bib0415"><span class="elsevierStyleSup">3</span></a>, los factores ambientales (radiación solar, tabaco, etc.) y los cambios hormonales juegan un papel importante. La prevalencia del LES en adultos se encuentra en torno al 30-210 casos por 100.000 habitantes<a class="elsevierStyleCrossRefs" href="#bib0420"><span class="elsevierStyleSup">4,5</span></a>, con diferencias marcadas a nivel de etnias.</p><p id="par0155" class="elsevierStylePara elsevierViewall">En los últimos años, las cifras de prevalencia se han incrementado, probablemente por la mayor concienciación y el diagnóstico temprano, así como la inclusión de formas indiferenciadas de la enfermedad en estadios de baja actividad. El LES presenta una predominancia en mujeres (9:1) y un pico de edad en torno a los 30 años<a class="elsevierStyleCrossRef" href="#bib0405"><span class="elsevierStyleSup">1</span></a>. Su marcada heterogeneidad confiere un reto para el clínico, si bien, un mayor conocimiento de su etiopatogenia, y un diagnóstico y tratamiento precoz, han conseguido que la supervivencia de esta enfermedad haya aumentado de 50% en los años 1950, a 90% en la actualidad<a class="elsevierStyleCrossRef" href="#bib0430"><span class="elsevierStyleSup">6</span></a>. La principal causa de muerte son las infecciones, con un incremento en las hospitalizaciones en España en la última década, seguida de la mortalidad cardiovascular, que en estos pacientes se encuentra incrementada respecto a la población sana<a class="elsevierStyleCrossRefs" href="#bib0435"><span class="elsevierStyleSup">7,8</span></a>.</p><p id="par0160" class="elsevierStylePara elsevierViewall">El objetivo principal de los expertos en la enfermedad en los últimos años ha sido la búsqueda de la remisión del LES y evitar el daño acumulado de la enfermedad, determinado en ocasiones por tratamientos, en especial glucocorticoides (GC)<a class="elsevierStyleCrossRef" href="#bib0445"><span class="elsevierStyleSup">9</span></a>. Dicho daño produce una morbilidad y una pérdida en la calidad de vida significativa<a class="elsevierStyleCrossRefs" href="#bib0450"><span class="elsevierStyleSup">10,11</span></a>. Por otro lado, se ha observado que la clave del tratamiento son los antimaláricos, por su efecto protector sobre la actividad y daño<a class="elsevierStyleCrossRefs" href="#bib0460"><span class="elsevierStyleSup">12–14</span></a>. La estrategia terapéutica actual del LES se basa en el principio de la implementación del tratamiento hasta llegar al objetivo (<span class="elsevierStyleItalic">treat to target</span> [T2T]<span class="elsevierStyleItalic">)</span><a class="elsevierStyleCrossRef" href="#bib0475"><span class="elsevierStyleSup">15</span></a> y se centra en alcanzar un estado definido de remisión<a class="elsevierStyleCrossRef" href="#bib0470"><span class="elsevierStyleSup">14</span></a> o de baja actividad de la enfermedad (LLDAS)<a class="elsevierStyleCrossRef" href="#bib0480"><span class="elsevierStyleSup">16</span></a>. Este enfoque implica el uso universal de antimaláricos, además de inmunosupresores clásicos o biológicos para lograr el LLDAS o preferiblemente la remisión, sin incrementar el uso de GC.</p><p id="par0165" class="elsevierStylePara elsevierViewall">El tratamiento de los pacientes con LES debe seguir las guías de práctica clínica<a class="elsevierStyleCrossRefs" href="#bib0465"><span class="elsevierStyleSup">13,17</span></a>, aunque la determinación final recaerá en una decisión compartida del clínico con el paciente basado en el balance riesgo-beneficio, así como la valoración global del enfermo. En esta revisión se presentan los nuevos fármacos aprobados para el tratamiento del LES, así como un pequeño avance de las moléculas que se encuentran en desarrollo clínico (<a class="elsevierStyleCrossRef" href="#tbl0005">tabla 1</a>).</p><elsevierMultimedia ident="tbl0005"></elsevierMultimedia></span><span id="sec0010" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0030">Fármacos dirigidos al linfocito B</span><span id="sec0015" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0035">Belimumab</span><p id="par0010" class="elsevierStylePara elsevierViewall">Dos miembros de la superfamilia TNF, BlyS y APRIL, pueden favorecer la supervivencia de las células B autorreactivas y la producción de autoanticuerpos en el LES<a class="elsevierStyleCrossRef" href="#bib0405"><span class="elsevierStyleSup">1</span></a>. Belimumab es un anticuerpo monoclonal humano de IgG1λ que se une específicamente a BLyS. Este bloqueo dificulta la supervivencia de las células B y, por tanto, reduce la diferenciación a células plasmáticas productoras de inmunoglobulinas. En dos estudios pivotales de fase 3 (BLISS 52<a class="elsevierStyleCrossRef" href="#bib0490"><span class="elsevierStyleSup">18</span></a> y BLISS-76<a class="elsevierStyleCrossRef" href="#bib0495"><span class="elsevierStyleSup">19</span></a>) se demostró la eficacia y seguridad de belimumab, y fue el primer biológico con indicación para el tratamiento del LES moderadamente grave. Desde el Grupo de trabajo de Enfermedades Autoinmunes Sistémicas (GEAS) de la Sociedad Española de Medicina Interna (SEMI), se crearon unas recomendaciones al respecto<a class="elsevierStyleCrossRef" href="#bib0500"><span class="elsevierStyleSup">20</span></a>. Desde entonces han surgido novedades en su posicionamiento debido a la mayor experiencia de los clínicos<a class="elsevierStyleCrossRef" href="#bib0505"><span class="elsevierStyleSup">21</span></a>, su seguridad a largo plazo<a class="elsevierStyleCrossRef" href="#bib0510"><span class="elsevierStyleSup">22</span></a>, y a la aparición de nuevas evidencias en nefritis lúpica (NL)<a class="elsevierStyleCrossRef" href="#bib0515"><span class="elsevierStyleSup">23</span></a>.</p><p id="par0015" class="elsevierStylePara elsevierViewall">Los ensayos BLISS 52 y BLISS 76 en adultos, PLUTO en población pediátrica y BLISS-LN en combinación con terapias inmunosupresoras de base para el tratamiento de pacientes adultos con NL han demostrado la eficacia y seguridad de belimumab<a class="elsevierStyleCrossRefs" href="#bib0490"><span class="elsevierStyleSup">18,19,23–25</span></a>. Con respecto a BLISS-LN, se utilizó belimumab intravenoso en pacientes con NL clase III, IV y V junto con tratamiento convencional (GC + micofenolato [MF] o ciclofosfamida [CF]). Un número significativamente mayor de pacientes en el grupo de belimumab (respecto del grupo de placebo) presentó una respuesta renal completa (RRC), de forma precoz, y ningún fracaso del tratamiento en la semana 104<a class="elsevierStyleCrossRef" href="#bib0515"><span class="elsevierStyleSup">23</span></a>. Sin embargo, el ensayo BLISS-LN cuenta con la importante limitación de la baja tasa de respuesta observada en el grupo tratado con terapias convencionales (CF o MF), por debajo de 30%, algo que no sucede en práctica clínica real y que se replica en otros ensayos clínicos de NL<a class="elsevierStyleCrossRef" href="#bib0530"><span class="elsevierStyleSup">26</span></a>. De hecho, en el grupo tratado con belimumab se observaron porcentajes de respuesta inferiores al 50%<a class="elsevierStyleCrossRefs" href="#bib0515"><span class="elsevierStyleSup">23,26</span></a>.</p><p id="par0020" class="elsevierStylePara elsevierViewall">Estudios observacionales sugieren la eficacia de la forma subcutánea en NL, al igual que en otras indicaciones, lo que confiere una mayor facilidad para el paciente<a class="elsevierStyleCrossRefs" href="#bib0535"><span class="elsevierStyleSup">27,28</span></a>. En práctica clínica convencional se ha observado una respuesta lenta debido a la gradual tasa de recambio de BlyS y al paulatino tiempo de desactivación de BlyS y su receptor, lo que limita la acción del fármaco. En un estudio observacional reciente de la cohorte RELES del GEAS, la indicación fundamental de belimumab entre los internistas españoles fue la clínica articular refractaria en el contexto de alta actividad medida por SLEDAI<a class="elsevierStyleCrossRef" href="#bib0545"><span class="elsevierStyleSup">29</span></a>.</p><p id="par0025" class="elsevierStylePara elsevierViewall">No obstante, tanto en estudios controlados como en registros observaciones se consigue reducir la frecuencia de los brotes, retardar la progresión del daño y, finalmente, un efecto ahorrador de corticosteroides<a class="elsevierStyleCrossRefs" href="#bib0505"><span class="elsevierStyleSup">21,30</span></a>. Además, se ha observado una respuesta serológica en términos de reducción del anti-DNA y normalización de los niveles de complemento<a class="elsevierStyleCrossRef" href="#bib0535"><span class="elsevierStyleSup">27</span></a>, y una mayor potencia terapéutica en cuando a nefroprotección cuando belimumab se usaba de forma concomitante con antimaláricos<a class="elsevierStyleCrossRef" href="#bib0555"><span class="elsevierStyleSup">31</span></a>. Por otro lado, se ha descrito en cohortes de pacientes que belimumab, utilizado de forma precoz con poco o escaso daño de la enfermedad, puede conllevar un estado de remisión o de LLDAS con más probabilidad<a class="elsevierStyleCrossRef" href="#bib0560"><span class="elsevierStyleSup">32</span></a>. Según las recomendaciones de la EULAR de 2019, el belimumab se debe considerar en aquellos pacientes con LES activo y respuesta inadecuada al tratamiento estándar (combinaciones de hidroxicloroquina y GC con o sin inmunosupresores), definida como actividad residual de la enfermedad que no permite reducir los GC y/o que presenten recaídas frecuentes<a class="elsevierStyleCrossRefs" href="#bib0465"><span class="elsevierStyleSup">13,77</span></a>. Similares recomendaciones se utilizan en otros grupos internacionales<a class="elsevierStyleCrossRef" href="#bib0565"><span class="elsevierStyleSup">33</span></a>. No hay experiencia en estudios controlados en manifestaciones del sistema nervioso central. En relación con NL, se ha propuesto el uso de belimumab en los siguientes escenarios,<ul class="elsevierStyleList" id="lis0005"><li class="elsevierStyleListItem" id="lsti0005"><span class="elsevierStyleLabel">•</span><p id="par0030" class="elsevierStylePara elsevierViewall">Añadido a la terapia convencional (CF o MF) en la inducción en pacientes con respuesta insuficiente en los primeros tres a seis meses<a class="elsevierStyleCrossRef" href="#bib0570"><span class="elsevierStyleSup">34</span></a>.</p></li><li class="elsevierStyleListItem" id="lsti0010"><span class="elsevierStyleLabel">•</span><p id="par0035" class="elsevierStylePara elsevierViewall">En pacientes refractarios<a class="elsevierStyleCrossRef" href="#bib0575"><span class="elsevierStyleSup">35</span></a>.</p></li><li class="elsevierStyleListItem" id="lsti0015"><span class="elsevierStyleLabel">•</span><p id="par0040" class="elsevierStylePara elsevierViewall">El Grupo de Estudio de Enfermedades Glomerulares (GLOSEN) propone la triple terapia de inicio con GC, MF y belimumab, en pacientes con:</p></li></ul></p><p id="par0045" class="elsevierStylePara elsevierViewall"><ul class="elsevierStyleList" id="lis0010"><li class="elsevierStyleListItem" id="lsti0020"><span class="elsevierStyleLabel">-</span><p id="par0050" class="elsevierStylePara elsevierViewall">Importante positividad inmunológica y manifestaciones extrarrenales<a class="elsevierStyleCrossRef" href="#bib0580"><span class="elsevierStyleSup">36</span></a>.</p></li><li class="elsevierStyleListItem" id="lsti0025"><span class="elsevierStyleLabel">-</span><p id="par0055" class="elsevierStylePara elsevierViewall">Antecedentes de brotes frecuentes y alto riesgo de evolución a enfermedad renal crónica<a class="elsevierStyleCrossRef" href="#bib0575"><span class="elsevierStyleSup">35</span></a>.</p></li></ul></p><p id="par0060" class="elsevierStylePara elsevierViewall">Sin embargo, hay que tener cuenta que las tasas de respuesta y los efectos beneficiosos a largo plazo sobre la función renal se producen sobre todo en pacientes con proteinuria basal < 3 g<a class="elsevierStyleCrossRef" href="#bib0585"><span class="elsevierStyleSup">37</span></a>, lo que unido al efecto relativamente lento de este biológico, nos hacen identificar como posibles candidatos a los pacientes en los que se ha producido un cierto grado de respuesta inicial a la terapia de inducción convencional con CF o MF, pero en los que no se prevé alcanzar la cifra «mágica» de proteinuria de 0,7 g al final del primer año. En cuanto al efecto ahorrador de GC de belimumab, hay que destacar que tanto el ensayo de voclosporina<a class="elsevierStyleCrossRef" href="#bib0590"><span class="elsevierStyleSup">38</span></a> como pautas que incluyen la combinación de CF junto con pulsos repetidos de metilprednisolona<a class="elsevierStyleCrossRef" href="#bib0595"><span class="elsevierStyleSup">39</span></a> han utilizado con éxito dosis reducidas de prednisona oral con muy rápido descenso a 5 mg/día.</p><p id="par0065" class="elsevierStylePara elsevierViewall">Con respecto a su retirada, no existe mucha evidencia al respecto, y se mantiene el criterio clínico de estabilidad para plantear la desescalada progresiva de dosis, y finalmente, la retirada definitiva del fármaco. Un estudio evaluó la consecuencia de suspender belimumab en pacientes estables, sin que se observara un mayor número de brotes o recurrencias de la enfermedad<a class="elsevierStyleCrossRef" href="#bib0600"><span class="elsevierStyleSup">40</span></a>. En cualquier caso, debe primar el sentido clínico e individualizar las decisiones en función del perfil concreto de gravedad y recurrencias de cada paciente.</p></span><span id="sec0020" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0040">Rituximab</span><p id="par0070" class="elsevierStylePara elsevierViewall">Rituximab es un anticuerpo monoclonal quimérico anti-CD20, con un uso ampliamente extendido en enfermedades linfoproliferativas e inmunomediadas variadas. En el caso del LES, a tenor de los primeros resultados en series de casos y estudios observacionales<a class="elsevierStyleCrossRefs" href="#bib0605"><span class="elsevierStyleSup">41–43</span></a>, se consideraba el tratamiento más prometedor para casos refractarios a la terapia convencional. Sin embargo, los dos ensayos clínicos pivotales no lograron demostrar la superioridad respecto al tratamiento estándar en NL y en enfermedad extrarrenal<a class="elsevierStyleCrossRefs" href="#bib0620"><span class="elsevierStyleSup">44,45</span></a>. El ensayo EXPLORER estudió la eficacia y seguridad de rituximab en pacientes con LES moderado-grave. Los resultados no mostraron diferencias en la proporción de pacientes que alcanzaron una respuesta completa o parcial entre el grupo de rituximab y el de placebo<a class="elsevierStyleCrossRef" href="#bib0620"><span class="elsevierStyleSup">44</span></a>. En cuanto a la NL proliferativa, el ensayo LUNAR no demostró superioridad sobre el MF para conseguir una RRC o parcial<a class="elsevierStyleCrossRef" href="#bib0625"><span class="elsevierStyleSup">45</span></a>.</p><p id="par0075" class="elsevierStylePara elsevierViewall">Se han estudiado detenidamente las posibles razones del fracaso de estos trabajos. Una hipótesis plantea que algunas características clínicas podrían haberse clasificado erróneamente como actividad, dando lugar a resultados sesgados al no mostrar mejoría, dado que las características se debían en realidad a daño. Otra crítica ha sido la metodología, donde pacientes con NL tenían biopsias realizadas mucho tiempo antes de la administración del fármaco, circunstancia que no se aplica en la práctica clínica habitual. Por otro lado, la gran heterogeneidad del LES entre los distintos grupos de pacientes podría estar implicada, así como la falta de una variable adecuada para analizar el efecto, como fue el índice de respuesta-4 del LES (<span class="elsevierStyleItalic">SRI-4</span>) del estudio de belimumab, o la evaluación compuesta del LES basada en el Grupo de Evaluación del Lupus de las Islas Británicas (BICLA). De hecho, un análisis secundario de la población incluida en el estudio LUNAR destacó que rituximab es eficaz en la inducción parcial y, en menor medida, en la remisión completa de la NL<a class="elsevierStyleCrossRef" href="#bib0630"><span class="elsevierStyleSup">46</span></a>. Por otro lado, se observó que la eficacia de este fármaco podía ser de utilidad en población hispana y afroamericana<a class="elsevierStyleCrossRef" href="#bib0620"><span class="elsevierStyleSup">44</span></a>.</p><p id="par0080" class="elsevierStylePara elsevierViewall">También se planteó la posibilidad de que el aumento del factor activador de linfocitos B perteneciente a la familia TNF (BAFF) acaecido en algunos pacientes tras la administración de rituximab estaba relacionado con el fracaso de los ensayos clínicos<a class="elsevierStyleCrossRef" href="#bib0635"><span class="elsevierStyleSup">47</span></a>. Esta observación ha dado lugar a la generación de nuevos ensayos con esquemas de tratamiento combinado de rituximab y belimumab. Dichos estudios (BEAT Lupus<a class="elsevierStyleCrossRef" href="#bib0640"><span class="elsevierStyleSup">48</span></a>, BLISS-BELIEVE<a class="elsevierStyleCrossRef" href="#bib0645"><span class="elsevierStyleSup">49</span></a>, CALIBRATE<a class="elsevierStyleCrossRef" href="#bib0650"><span class="elsevierStyleSup">50</span></a>, Synbiose 1<a class="elsevierStyleCrossRef" href="#bib0655"><span class="elsevierStyleSup">51</span></a> y 2) plantean el tratamiento inicial con rituximab seguido de belimumab para bloquear el posible BAAF incrementado tanto en LES como en NL. Los resultados del BEAT Lupus fueron favorables en cuanto a reducción de brotes en el grupo de tratamiento combinado, sin observarse datos de infección significativa<a class="elsevierStyleCrossRef" href="#bib0640"><span class="elsevierStyleSup">48</span></a>. Sin embargo, en el caso del BLISS-BELIEVE no se logró demostrar que el control de la enfermedad con la adición de un ciclo único de rituximab al tratamiento con belimumab fuera superior al logrado con el tratamiento con belimumab solo, y se observaron más infecciones graves en el grupo de la combinación<a class="elsevierStyleCrossRef" href="#bib0645"><span class="elsevierStyleSup">49</span></a>. Tampoco los resultados del estudio CALIBRATE en paciente con NL tratados con una combinación de CF y rituximab, donde además se añadía belimumab intravenoso, demostraron que la adición de este último ofreciera mayores ventajas, si bien es posible que existiera una falta de potencia para detectar diferencias<a class="elsevierStyleCrossRef" href="#bib0650"><span class="elsevierStyleSup">50</span></a>. Debemos esperar a los resultados del Synbiose 2 (<a href="ctgov:NCT03747159">NCT03747159</a>) para poder tener más datos sobre la combinación.</p><p id="par0085" class="elsevierStylePara elsevierViewall">A pesar de los decepcionantes resultados de los ensayos de rituximab, el fármaco ha sido ampliamente utilizado fuera de indicación durante años en pacientes con enfermedad grave y/o refractaria, con buenos resultados en práctica clínica real<a class="elsevierStyleCrossRefs" href="#bib0605"><span class="elsevierStyleSup">41–43</span></a>. Por ello, las guías EULAR lo posicionan como régimen de inducción para pacientes con enfermedad extrarrenal tras el fracaso de múltiples opciones terapéuticas, o en caso de contraindicación a los inmunosupresores convencionales<a class="elsevierStyleCrossRef" href="#bib0465"><span class="elsevierStyleSup">13</span></a>. En NL se sugiere rituximab solo o añadido a MF o CF en pacientes con mala respuesta o refractarios<a class="elsevierStyleCrossRef" href="#bib0575"><span class="elsevierStyleSup">35</span></a>.</p></span><span id="sec0025" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0045">Obinutuzumab</span><p id="par0090" class="elsevierStylePara elsevierViewall">Obinutuzumab es un anticuerpo monoclonal anti-CD20 humanizado (a diferencia de rituximab, que es quimérico) de tipo II que induce una potente y rápida depleción de células B. A diferencia con rituximab, obinutuzumab presenta menor citotoxicidad celular dependiente del complemento y mayor citotoxicidad celular dependiente de anticuerpos con una mayor actividad fagocítica<a class="elsevierStyleCrossRef" href="#bib0660"><span class="elsevierStyleSup">52</span></a>. En el ensayo NOBILITY en pacientes con NL se describió una depleción rápida y sostenida de las células B y se demostró que la adición de obinutuzumab al tratamiento estándar con GC y MF aumentaba la tasa de RRC en pacientes con NL proliferativa, además de mejorar la respuesta renal a las 104 semanas. En comparación con el placebo, obinutuzumab también produjo mejoras significativas en los títulos de anti-DNA, complemento, filtrado glomerular y la proteinuria, con un cierto margen de seguridad en relación con eventos adversos e infecciones<a class="elsevierStyleCrossRef" href="#bib0665"><span class="elsevierStyleSup">53</span></a>. Si los ensayos de fase III confirman el efecto beneficioso descrito, obinutuzumab podría sustituir a rituximab en el tratamiento de la NL refractaria.</p></span></span><span id="sec0030" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0050">Fármacos dirigidos a la vía del interferón</span><span id="sec0035" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0055">Anifrolumab</span><p id="par0095" class="elsevierStylePara elsevierViewall">La vía del interferón (IFN) también se ha estudiado ampliamente en el contexto de la patogénesis de la autoinmunidad, dado que múltiples polimorfismos genéticos se asocian con un incremento del riesgo de desarrollar LES<a class="elsevierStyleCrossRef" href="#bib0405"><span class="elsevierStyleSup">1</span></a>. El incremento en los niveles de IFN favorece la supervivencia y diferenciación de las células B mediante la inducción de BAFF<a class="elsevierStyleCrossRef" href="#bib0670"><span class="elsevierStyleSup">54</span></a>. La interacción de estos IFN con sus receptores induce la señalización a través de la vía Janus cinasa (JAK) –transductor de señales activador de la transcripción (STAT)– y la transcripción de cientos de genes sensibles a los IFN –la «<span class="elsevierStyleItalic">firma del interferón</span>»–, que codifican proteínas implicadas en la regulación de la función inmunitaria<a class="elsevierStyleCrossRef" href="#bib0675"><span class="elsevierStyleSup">55</span></a>.</p><p id="par0170" class="elsevierStylePara elsevierViewall">Mediante una cascada de retroalimentación positiva, el IFN de tipo 1 perpetúa la respuesta inmune innata y adaptativa favoreciendo la producción de citocinas proinflamatorias. Se ha descrito que hasta 80% de los pacientes con LES activo tiene una firma del interferón elevada, lo que significa que esta vía patogénica se encuentra hiperactivada<a class="elsevierStyleCrossRefs" href="#bib0680"><span class="elsevierStyleSup">56–58</span></a>. Debido a este papel central en fisiopatología del LES, se propuso estudiar anticuerpos monoclonales frente al IFN, con resultados pobres en relación a respuesta y a seguridad. Sin embargo, anifrolumab, un anticuerpo monoclonal contra el receptor del IFN de tipo I, ha conseguido finalmente con base en sus estudios pivotales la aprobación de la agencia americana y europea para el tratamiento de pacientes con LES de moderado a grave (se excluyen de momento los pacientes con NL activa grave o afectación neuropsiquiátrica) que reciben terapia estándar.</p><p id="par0175" class="elsevierStylePara elsevierViewall">Después de los resultados prometedores del ensayo fase 2 (MUSE)<a class="elsevierStyleCrossRef" href="#bib0680"><span class="elsevierStyleSup">56</span></a>, donde se alcanzó una proporción significativamente mayor de respuesta SRI-4 con reducción sostenida de GC en la semana 24, se realizaron dos ensayos fase 3 en pacientes con LES no renal activo (TULIP-1<a class="elsevierStyleCrossRef" href="#bib0685"><span class="elsevierStyleSup">57</span></a> y TULIP-2<a class="elsevierStyleCrossRef" href="#bib0690"><span class="elsevierStyleSup">58</span></a>). En el primero, TULIP-1, no se observaron diferencias en la variable principal (medida por SRI-4), aunque las respuestas medidas por BICLA fueron significativamente mayores en el grupo de anifrolumab<a class="elsevierStyleCrossRef" href="#bib0685"><span class="elsevierStyleSup">57</span></a>. Las razones de esa discordancia se deben a un diseño demasiado estricto para detectar cambios en la actividad, y que la variable SRI-4 no fue capaz de detectar mejorías parciales en distintos dominios. Se comprobó que hubo un subgrupo no respondedor a anifrolumab, que fueron aquellos incluidos en el grupo placebo que lograron una respuesta SRI-4, pero no BICLA. Estos pacientes presentaron previo a recibir el fármaco, bajos recuentos articulares y, por tanto, una puntuación SLEDAI-2K más baja, una dosis mayor de GC de base<a class="elsevierStyleCrossRef" href="#bib0695"><span class="elsevierStyleSup">59</span></a>. Se decidió realizar otro ensayo (TULIP-2) en el que el índice a utilizar como variable de resultado principal fue BICLA. En este trabajo, se obtuvieron mejores resultados, así como una mayor reducción del número de brotes y menor dosis de GC.</p><p id="par0100" class="elsevierStylePara elsevierViewall">Los análisis <span class="elsevierStyleItalic">post hoc</span> de los estudios MUSE, TULIP-1 y TULIP-2 corroboraron su eficacia en diferentes dominios orgánicos, y confirmaron una mayor eficacia en pacientes con una firma de IFN tipo I elevada, aunque pacientes con una firma baja también se beneficiaron de la adición de anifrolumab<a class="elsevierStyleCrossRef" href="#bib0700"><span class="elsevierStyleSup">60</span></a>. De igual manera, se observó que los pacientes tratados con anifrolumab alcanzaron de forma más precoz un estado de LLDAS, en el cual permanecieron más tiempo<a class="elsevierStyleCrossRef" href="#bib0705"><span class="elsevierStyleSup">61</span></a>. En relación con la utilidad de anifrolumab en NL, solamente se dispone de un ensayo fase 2 TULIP1- LN, donde el régimen intensificado (anifrolumab 900 mg/mes) se asoció a un porcentaje de mayor RRC, así como en otros parámetros como el cociente proteínas-creatinina en orina, el sedimento urinario inactivo y la reducción de la dosis de GC<a class="elsevierStyleCrossRef" href="#bib0710"><span class="elsevierStyleSup">62</span></a>. Un ensayo en fase III está actualmente en marcha (<a href="ctgov:NCT05138133">NCT05138133</a>).</p><p id="par0105" class="elsevierStylePara elsevierViewall">En relación con la seguridad del fármaco, se ha descrito mayor reactivación de herpes zóster e infección por COVID-19<a class="elsevierStyleCrossRef" href="#bib0690"><span class="elsevierStyleSup">58</span></a>, aunque en los estudios de extensión se vio que dicho riesgo de infección disminuía con el tiempo tras el primer año del fármaco y con la vacunación para SARS-CoV-2<a class="elsevierStyleCrossRef" href="#bib0715"><span class="elsevierStyleSup">63</span></a>. Se considera que las dosis altas de GC al inicio de los estudios pueden haber influido en el desarrollo de ambas infecciones. Razonablemente, se podría plantear un régimen de vacunación como estrategia preventiva previo al uso de este fármaco.</p></span></span><span id="sec0040" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0060">Nuevos fármacos inhibidores de la calcineurina</span><span id="sec0045" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0065">Voclosporina</span><p id="par0110" class="elsevierStylePara elsevierViewall">La voclosporina es un derivado del ciclosporina (CsA), con una cadena lateral funcional modificada, que induce cambios estructurales en la calcineurina, lo que multiplica por cuatro su potencia en comparación con CsA<a class="elsevierStyleCrossRef" href="#bib0720"><span class="elsevierStyleSup">64</span></a>. De igual manera que CsA y tacrolimus, su mecanismo de acción va dirigido contra el linfocito T, con el objetivo de disminuir su activación, así como la liberación de citocinas secundaria a la misma. Estos fármacos se emplean como segunda línea en combinación con MF, según las guías de práctica clínica<a class="elsevierStyleCrossRefs" href="#bib0570"><span class="elsevierStyleSup">34,35</span></a>, aunque en las últimas recomendaciones se podría plantear en pacientes con proteinuria nefrótica y función renal preservada. Es un fármaco que se ha empleado en ensayos clínicos de psoriasis y trasplante renal, donde se ha comprobado su poder inmunosupresor<a class="elsevierStyleCrossRef" href="#bib0720"><span class="elsevierStyleSup">64</span></a>. Actualmente ha conseguido la aprobación de la FDA y la agencia europea para el tratamiento de la NL activa de clase III, IV o V, sobre la base de varios ensayos clínicos (AURORA 1<a class="elsevierStyleCrossRef" href="#bib0590"><span class="elsevierStyleSup">38</span></a>, AURORA 2<a class="elsevierStyleCrossRef" href="#bib0725"><span class="elsevierStyleSup">65</span></a>). En estos estudios, voclosporina se utiliza en combinación con MF, y su característica diferencial en los diseños de estos ensayos, radica en la pauta rápida de descenso de GC en ambos grupos, placebo y voclosporina. Se ha comprobado que la tasa de RRC es mayor entre los pacientes tratados con voclosporina en comparación con placebo, de casi el doble (41 vs. 23%)<a class="elsevierStyleCrossRef" href="#bib0590"><span class="elsevierStyleSup">38</span></a>.</p><p id="par0180" class="elsevierStylePara elsevierViewall">Como ventajas frente a los clásicos inhibidores de la calcineurina, voclosporina tiene un perfil farmacocinético y farmacodinámico más predecible, lo que permite una dosificación fija y elimina la necesidad de monitorización del fármaco<a class="elsevierStyleCrossRef" href="#bib0720"><span class="elsevierStyleSup">64</span></a>. Sus eventos adversos son comparables a los de otros inhibidores de la calcineurina, y en lo que respecta a nefrotoxicidad, por el momento se ha comprobado cierta seguridad en los estudios realizados<a class="elsevierStyleCrossRefs" href="#bib0590"><span class="elsevierStyleSup">38,65</span></a>. En el ensayo de extensión del fármaco más allá del año de tratamiento, el AURORA 2, se comprobó mejoría progresiva de la proteinuria a lo largo de los tres años de seguimiento con mayores tasas de RRC (50.9 vs. 39%), con una seguridad similar a la observada en el AURORA 1<a class="elsevierStyleCrossRef" href="#bib0725"><span class="elsevierStyleSup">65</span></a>. Nuevamente, el principal problema de estos estudios es el mal comportamiento en el grupo placebo (es decir, con MF en monoterapia), lo que hace que la respuesta del grupo voclosporina que apenas superan 40% al año y 50% a los tres años, sean significativamente superiores. Actualmente se necesitan más datos a largo plazo para conocer la seguridad última en el fármaco en lo relativo a la nefrotoxicidad conocida de esta familia terapéutica y para identificar los subgrupos de pacientes que se pueden beneficiar de su uso.</p></span></span><span id="sec0050" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0070">Inhibidores JAK</span><p id="par0115" class="elsevierStylePara elsevierViewall">El receptor JAK-STAT se ha implicado en la patogénesis del LES debido a que es el mecanismo de entrada de múltiples citocinas proinflamatorias, como la vía del IFN. Una inhibición en esa vía podría controlar las manifestaciones del LES<a class="elsevierStyleCrossRef" href="#bib0730"><span class="elsevierStyleSup">66</span></a>. Además de ser moléculas que ya han sido utilizadas en otras enfermedades autoinmunes, tienen el atractivo de poder ofrecer formulación oral que facilitaría la adherencia.</p><span id="sec0055" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0075">Tofacitinib</span><p id="par0120" class="elsevierStylePara elsevierViewall">Tofacitinib, un inhibidor de JAK1/JAK3, se investigó en modelos animales donde se observó que prevenía la aparición de NL<a class="elsevierStyleCrossRef" href="#bib0735"><span class="elsevierStyleSup">67</span></a>. Por este motivo, se realizó un ensayo clínico donde se observó una disminución de la firma del IFN 1, y de otras moléculas proinflamatorias implicadas en el LES, con un perfil lipídico favorable<a class="elsevierStyleCrossRef" href="#bib0740"><span class="elsevierStyleSup">68</span></a>. Dicha circunstancia contrasta con los datos de seguridad observados en pacientes artritis reumatoide tratados con tofacitinib, con mayor riesgo cardiovascular, trombogénico y de neoplasia<a class="elsevierStyleCrossRef" href="#bib0745"><span class="elsevierStyleSup">69</span></a>. Por otro lado, en lo relativo a práctica clínica real, se han descritos series de casos con afectación cutánea y articular con muy buena respuesta a dicho tratamiento<a class="elsevierStyleCrossRef" href="#bib0750"><span class="elsevierStyleSup">70</span></a>.</p></span><span id="sec0060" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0080">Baricitinib</span><p id="par0125" class="elsevierStylePara elsevierViewall">Baricitinib es un inhibidor de JAK1/JAK2 que ha sido aprobado para el tratamiento de diversas enfermedades inmunomediadas<a class="elsevierStyleCrossRef" href="#bib0730"><span class="elsevierStyleSup">66</span></a>. Con esta molécula se han realizado tres ensayos clínicos. El primero, un fase 2 que quiso evaluar la respuesta cutáneo-articular, presentó muy buenos resultados en el brazo de baricitinib 4 mg<a class="elsevierStyleCrossRef" href="#bib0755"><span class="elsevierStyleSup">71</span></a>. Sin embargo, en los dos fase 3 posteriores (SLE-BRAVE 1<a class="elsevierStyleCrossRef" href="#bib0760"><span class="elsevierStyleSup">72</span></a> y SLE-BRAVE 2<a class="elsevierStyleCrossRef" href="#bib0765"><span class="elsevierStyleSup">73</span></a>) hubo resultados contradictorios. Existe un ensayo de extensión (SLE BRAVE- X) diseñado para evaluar la eficacia y seguridad a largo plazo, que quizá pueda aportar más información. En cualquier caso, es posible que pueda tener una cabida en formas agresivas articulares o cutáneas.</p></span><span id="sec0065" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0085">Deucravacitinib</span><p id="par0130" class="elsevierStylePara elsevierViewall">Deucravacitinib es un inhibidor alostérico selectivo y específico de la tirosina cinasa 2 (TYK2). En un ensayo de fase II en pacientes con LES, la tasa de respuesta al SRI-4 en la semana 32 fue significativamente mayor en los pacientes tratados con 3 mg dos veces al día (58%) que en los pacientes que recibieron placebo (34%)<a class="elsevierStyleCrossRef" href="#bib0770"><span class="elsevierStyleSup">74</span></a>. En el momento actual se está planteando un ensayo en fase 3 para confirmar estos resultados positivos (<a href="ctgov:NCT05620407">NCT05620407</a>).</p></span><span id="sec0070" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0090">Upadacitinib</span><p id="par0135" class="elsevierStylePara elsevierViewall">Upadacitinib es un inhibidor selectivo de JAK1, y con un uso creciente en enfermedades inmunomediadas. En LES, se ha realizado un ensayo fase II con resultados positivos, en monoterapia como en combinación con elsubrutinib (inhibidor de quinasa de Bruton) en cuanto reducción de brotes y tiempo hasta conseguir LLDAS<a class="elsevierStyleCrossRef" href="#bib0775"><span class="elsevierStyleSup">75</span></a>. Actualmente está en marcha un fase III para confirmar estos resultados positivos.</p></span></span><span id="sec0075" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0095">Conclusión</span><p id="par0140" class="elsevierStylePara elsevierViewall">Actualmente existe un importante arsenal de tratamientos para el LES. Es importante subrayar que con un adecuado uso de los medicamentos existentes, combinando drogas con perfil de toxicidad complementario, con una utilización juiciosa de los GC (pulsos para inducir remisión, dosis ≤ 5 mg/g de mantenimiento) y con la prescripción universal de hidroxicloroquina, se pueden obtener resultados favorables en cuanto a control de la actividad de la enfermedad y prevención de complicaciones a medio-largo plazo en una gran mayoría de pacientes<a class="elsevierStyleCrossRef" href="#bib0780"><span class="elsevierStyleSup">76</span></a>. Sin embargo, existen subgrupos en los que no se alcanzan los estados deseables de remisión o LLDAS. En los últimos años se han diseñado ensayos clínicos que han conseguido resultados favorables, y por ende la aprobación de nuevos fármacos para la enfermedad sistémica<a class="elsevierStyleCrossRef" href="#bib0690"><span class="elsevierStyleSup">58</span></a>, o para la nefritis lúpica<a class="elsevierStyleCrossRefs" href="#bib0515"><span class="elsevierStyleSup">23,38</span></a>. A este respecto, las recientes guías EULAR de tratamiento del LES dejan abierta la posibilidad de iniciar tratamiento biológico con belimumab o anifrolumab en fases muy precoces de la enfermedad, incluso sin que se requiera el fracaso de al menos un inmunosupresor convencional<a class="elsevierStyleCrossRef" href="#bib0785"><span class="elsevierStyleSup">77</span></a>. De igual modo, se contempla la posibilidad de asociar belimumab o calcineurínicos (incluyendo voclosporina, todavía no disponible en España) al tratamiento inicial de la nefritis lúpica con MF o CF, particularmente en pacientes con actividad extrarrenal (belimumab) o con proteinuria nefrótica (calcineurínicos)<a class="elsevierStyleCrossRefs" href="#bib0580"><span class="elsevierStyleSup">36,77</span></a>. Más allá de consideraciones económicas, muy importantes también en los tiempos que vivimos y más aún en el escenario de una sanidad pública universal como la española, el uso indiscriminado de los nuevos fármacos prácticamente desde el diagnóstico del LES puede suponer no solo el sobretratamiento de muchos pacientes, sino casi agotar el arsenal terapéutico desde fases muy precoces de la enfermedad. Nuestra postura al respecto sigue siendo la de reservar en cierta medida los medicamentos más recientemente autorizados, priorizando el uso de terapias convencionales asociadas al tratamiento de base con hidroxicloroquina y GC (tal y como se comenta al inicio de esta sección), eligiendo las diferentes alternativas en función del escenario clínico (mepacrina y/o metotrexate para manifestaciones cutáneas y articulares, MF y calcineurínicos en pacientes con nefritis, ciclofosfamida en afectación orgánica grave, azatioprina como inmunosupresor de mantenimiento, etc.)<a class="elsevierStyleCrossRef" href="#bib0780"><span class="elsevierStyleSup">76</span></a>. El tratamiento de inducción de la nefritis lúpica con CF o MF sigue resultando efectivo en estudios de práctica clínica real<a class="elsevierStyleCrossRefs" href="#bib0595"><span class="elsevierStyleSup">39,78,79</span></a>, con la posibilidad de que la administración repetida de pulsos de GC aumente las tasas de respuesta de forma significativa<a class="elsevierStyleCrossRef" href="#bib0595"><span class="elsevierStyleSup">39</span></a>. Se podría plantear añadir belimumab o inhibidores de la calcineurina (voclosporina o tacrolimus) en aquellas situaciones donde no se consiga una respuesta renal adecuada en los primeros meses (<a class="elsevierStyleCrossRef" href="#fig0005">fig. 1</a>). Rituximab, pese a su uso fuera de ficha técnica en LES sigue siendo una opción en cuadros multisistémicos de gran actividad y/o que ponen en peligro la vida<a class="elsevierStyleCrossRefs" href="#bib0545"><span class="elsevierStyleSup">29,34</span></a>. El rol de belimumab y anifrolumab se situaría en situaciones de actividad persistente a pesar de combinaciones de fármacos convencionales. La mayor experiencia clínica con el primero lo situaría como la opción inicial, aunque la afectación cutánea grave podría ser la excepción para el uso de anifrolumab como primer biológico<a class="elsevierStyleCrossRef" href="#bib0700"><span class="elsevierStyleSup">60</span></a>.</p><elsevierMultimedia ident="fig0005"></elsevierMultimedia><p id="par0145" class="elsevierStylePara elsevierViewall">Actualmente existen otras muchas moléculas en desarrollo (<a class="elsevierStyleCrossRef" href="#tbl0010">tabla 2</a>) con algunos resultados optimistas en fase 1 o 2. Es posible que, en los próximos años, podamos incorporar nuevos medicamentos, que junto con la experiencia ganada en las terapias clásicas y recientes, nos permitan un mejor control de la enfermedad con una disminución de las complicaciones directas de la misma e indirectas de los tratamientos en pacientes con enfermedad de difícil control con las terapias más convencionales. En el momento actual existe la controversia de optar por dos actitudes respecto al LES: seguir un tratamiento combinado (<span class="elsevierStyleItalic">multi-target</span>) siguiendo el esquema del T2T, o bien mantener una actitud clásica de inducción y mantenimiento, sobre todo en las formas de NL. La práctica clínica, los resultados de nuevos ensayos y la información de registros en vida real de cohortes de incepción, como el RELES<a class="elsevierStyleCrossRef" href="#bib0800"><span class="elsevierStyleSup">80</span></a>, podrán arrojar más luz en el debate actual.</p><elsevierMultimedia ident="tbl0010"></elsevierMultimedia></span><span id="sec0085" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0100">Financiación</span><p id="par0185" class="elsevierStylePara elsevierViewall">Este artículo no ha recibido financiación.</p></span><span id="sec0080" class="elsevierStyleSection elsevierViewall"><span class="elsevierStyleSectionTitle" id="sect0105">Conflicto de intereses</span><p id="par0150" class="elsevierStylePara elsevierViewall">AGG declara haber recibido honorarios por ponencias de Astra-Zeneca, Ortsuka y GSK. GRI e ICT declaran no tener ningún conflicto de intereres.</p></span></span>"
"textoCompletoSecciones" => array:1 [
"secciones" => array:13 [
0 => array:3 [
"identificador" => "xres2041412"
"titulo" => "Resumen"
"secciones" => array:1 [
0 => array:1 [
"identificador" => "abst0005"
]
]
]
1 => array:2 [
"identificador" => "xpalclavsec1745452"
"titulo" => "Palabras clave"
]
2 => array:3 [
"identificador" => "xres2041413"
"titulo" => "Abstract"
"secciones" => array:1 [
0 => array:1 [
"identificador" => "abst0010"
]
]
]
3 => array:2 [
"identificador" => "xpalclavsec1745453"
"titulo" => "Keywords"
]
4 => array:2 [
"identificador" => "sec0005"
"titulo" => "Introducción"
]
5 => array:3 [
"identificador" => "sec0010"
"titulo" => "Fármacos dirigidos al linfocito B"
"secciones" => array:3 [
0 => array:2 [
"identificador" => "sec0015"
"titulo" => "Belimumab"
]
1 => array:2 [
"identificador" => "sec0020"
"titulo" => "Rituximab"
]
2 => array:2 [
"identificador" => "sec0025"
"titulo" => "Obinutuzumab"
]
]
]
6 => array:3 [
"identificador" => "sec0030"
"titulo" => "Fármacos dirigidos a la vía del interferón"
"secciones" => array:1 [
0 => array:2 [
"identificador" => "sec0035"
"titulo" => "Anifrolumab"
]
]
]
7 => array:3 [
"identificador" => "sec0040"
"titulo" => "Nuevos fármacos inhibidores de la calcineurina"
"secciones" => array:1 [
0 => array:2 [
"identificador" => "sec0045"
"titulo" => "Voclosporina"
]
]
]
8 => array:3 [
"identificador" => "sec0050"
"titulo" => "Inhibidores JAK"
"secciones" => array:4 [
0 => array:2 [
"identificador" => "sec0055"
"titulo" => "Tofacitinib"
]
1 => array:2 [
"identificador" => "sec0060"
"titulo" => "Baricitinib"
]
2 => array:2 [
"identificador" => "sec0065"
"titulo" => "Deucravacitinib"
]
3 => array:2 [
"identificador" => "sec0070"
"titulo" => "Upadacitinib"
]
]
]
9 => array:2 [
"identificador" => "sec0075"
"titulo" => "Conclusión"
]
10 => array:2 [
"identificador" => "sec0085"
"titulo" => "Financiación"
]
11 => array:2 [
"identificador" => "sec0080"
"titulo" => "Conflicto de intereses"
]
12 => array:1 [
"titulo" => "Bibliografía"
]
]
]
"pdfFichero" => "main.pdf"
"tienePdf" => true
"fechaRecibido" => "2023-08-29"
"fechaAceptado" => "2023-11-01"
"PalabrasClave" => array:2 [
"es" => array:1 [
0 => array:4 [
"clase" => "keyword"
"titulo" => "Palabras clave"
"identificador" => "xpalclavsec1745452"
"palabras" => array:6 [
0 => "Lupus eritematoso sistémico"
1 => "Nefritis lúpica"
2 => "Rituximab"
3 => "Anifrolumab"
4 => "Belimumab"
5 => "Voclosporina"
]
]
]
"en" => array:1 [
0 => array:4 [
"clase" => "keyword"
"titulo" => "Keywords"
"identificador" => "xpalclavsec1745453"
"palabras" => array:6 [
0 => "Systemic lupus erythematosus"
1 => "Lupus nephritis"
2 => "Rituximab"
3 => "Anifrolumab"
4 => "Belimumab"
5 => "Voclosporin"
]
]
]
]
"tieneResumen" => true
"resumen" => array:2 [
"es" => array:2 [
"titulo" => "Resumen"
"resumen" => "<span id="abst0005" class="elsevierStyleSection elsevierViewall"><p id="spar0005" class="elsevierStyleSimplePara elsevierViewall">El lupus eritematoso sistémico (LES) es una enfermedad inflamatoria autoinmune sistémica de causa desconocida, con heterogeneidad en su presentación clínica, así como una variabilidad en su curso clínico y pronóstico. El objetivo actual del tratamiento es conseguir la remisión de la enfermedad o al menos un estado de baja actividad, y por consiguiente mejorar la calidad de vida del paciente. La terapia biológica en el lupus, a diferencia de otras entidades, si bien no ha conseguido instaurarse plenamente, ha irrumpido en los últimos años con novedades terapéuticas importantes. En esta revisión se pretende actualizar las herramientas terapéuticas del tratamiento del LES enfocado a las nuevas moléculas que han conseguido superar los objetivos de sus ensayos clínicos.</p></span>"
]
"en" => array:2 [
"titulo" => "Abstract"
"resumen" => "<span id="abst0010" class="elsevierStyleSection elsevierViewall"><p id="spar0010" class="elsevierStyleSimplePara elsevierViewall">Systemic lupus erythematosus (SLE) is a systemic autoimmune inflammatory disease of unknown cause, with heterogeneity in its clinical presentation, as well as variability in its clinical course and prognosis. The current goal of treatment is to achieve disease remission or a state of low activity, and thereby improve the patient's quality of life. Biological therapy in lupus, unlike other entities, although it has not been fully established, in recent years it has burst onto the scene with important therapeutic novelties. This review aims to update the therapeutic tools for the treatment of SLE focusing on the new molecules that have achieved the objectives of their clinical trials.</p></span>"
]
]
"multimedia" => array:3 [
0 => array:7 [
"identificador" => "fig0005"
"etiqueta" => "Figura 1"
"tipo" => "MULTIMEDIAFIGURA"
"mostrarFloat" => true
"mostrarDisplay" => false
"figura" => array:1 [
0 => array:4 [
"imagen" => "gr1.jpeg"
"Alto" => 1479
"Ancho" => 2925
"Tamanyo" => 316698
]
]
"descripcion" => array:1 [
"es" => "<p id="spar0015" class="elsevierStyleSimplePara elsevierViewall">Propuesta de tratamiento para la nefritis lúpica (III, IV+/-V).</p>"
]
]
1 => array:8 [
"identificador" => "tbl0005"
"etiqueta" => "Tabla 1"
"tipo" => "MULTIMEDIATABLA"
"mostrarFloat" => true
"mostrarDisplay" => false
"detalles" => array:1 [
0 => array:3 [
"identificador" => "at1"
"detalle" => "Tabla "
"rol" => "short"
]
]
"tabla" => array:3 [
"leyenda" => "<p id="spar0025" class="elsevierStyleSimplePara elsevierViewall">BICLA: evaluación compuesta del lupus basada en el Grupo de Evaluación del Lupus de las Islas Británicas; iv: intravenoso; FG: filtrado glomerular; LES: lupus eritematoso sistémico; mg: miligramos; NL: nefritis lúpica; vo: vía oral. Prt/cr: cociente proteína/creatinina; sc: subcutánea; SRI-4: índice de respuesta 4 del lupus eritematoso sistémico.</p>"
"tablatextoimagen" => array:1 [
0 => array:2 [
"tabla" => array:1 [
0 => """
<table border="0" frame="\n
\t\t\t\t\tvoid\n
\t\t\t\t" class=""><thead title="thead"><tr title="table-row"><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Fármaco \t\t\t\t\t\t\n
\t\t\t\t\t\t</th><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Características \t\t\t\t\t\t\n
\t\t\t\t\t\t</th><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Estudios \t\t\t\t\t\t\n
\t\t\t\t\t\t</th><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Objetivo primario \t\t\t\t\t\t\n
\t\t\t\t\t\t</th><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Resultados \t\t\t\t\t\t\n
\t\t\t\t\t\t</th><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Escenario clínico \t\t\t\t\t\t\n
\t\t\t\t\t\t</th><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Ventajas/desventajas \t\t\t\t\t\t\n
\t\t\t\t\t\t</th></tr></thead><tbody title="tbody"><tr title="table-row"><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Belimumab</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anticuerpo monoclonal (IgG1) dirigido al BAFF soluble10 mg/kg iv200 mg sc</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">BLISS-52 Fase III \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">SRI- 4 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">58 vs. 44% (OR 1,83 [1,30-2,59]; p = 0,000 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Paciente con LES activo y tratamiento estándar optimizado• NL refractaria a corto/medio plazo, añadido a terapia estándar</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Seguridad a largo plazo• Experiencia de uso• Posología iv y sc• Relativa lentitud de acción</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">BLISS 72 Fase III \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">SRI- 4 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">43,2 vs. 33,5%; p = 0,017 \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">BLIS LN Fase III \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Prot/Cr ≤ 0,7• Disminución de 20% filtrado \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">43 vs. 32% (OR 1,6 IC 95% [1,0-2,3]; p = 0,03) \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anifrolumab</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anticuerpos antireceptor del interferón tipo 1.300 mg iv</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">MUSE Fase IIb \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">SRI-4 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">34,3 vs. 17,6%; p = 0,014 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Pacientes con LES activo con tratamiento estándar optimizado</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Rapidez de acción• Experiencia en vida real limitada</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Tulip 1 Fase III \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">SRI-4 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">36 vs. 40% (OR -–4,2 IC 95% [–14,2 - 5,8]; p = 0,41) \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Tulip 2 Fase III \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">BICLA \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">47,8 vs. 31,5% 16,3 p = 0,001 \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="2" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Voclosporina</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="2" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor de la calcineurina23,7 mg vo</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Aurora 1 Fase III \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Prot/Cr ≤ 0,5• Disminución de 20% filtrado• Prednisona ≤ 10 mg \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">41 vs. 23% (OR 2,65; IC 95% [1,64-4,27]; p < 0-0001) \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="2" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• NL III, IV o V• Proteinuria nefrótica</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="2" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Formulación oral• Efectos adversos conocidos por amplia experiencia de uso de calcineurínicos• Elevado número de cápsulas con la formulación actual</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Aurora 2 Fase III \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Seguridad• Prot/Cr ≤ 0,5• Disminución de 20% FG \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">50,9 vs. 39,0% (OR 1,74; IC 95% [1,00- 3,03]) p < 0,05 \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Obinutuzumab<a class="elsevierStyleCrossRef" href="#tblfn0005"><span class="elsevierStyleSup">!</span></a> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anticuerpo monoclonal antiCD20 humanizado1000 mg iv \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">NOBILITY Fase II \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Prot/Cr ≤ 0,5• Normalización filtrado• Inactivación del sedimento \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">41 vs. 23%, p = 0,026 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• NL III, IV \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Experiencia previa con rituximab y mejora de sus cualidades (menores reacciones infusionales)• Escasa experiencia \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="2" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Baricitinib<a class="elsevierStyleCrossRef" href="#tblfn0005"><span class="elsevierStyleSup">!</span></a></td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="2" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor selectivo JAK 1 y 24 mg vo</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">SLE-BRAVE-I \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">SRI-4 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">57 vs. 46% (OR 10,8 (2,0-19,6); p < 0,016 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="2" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• LES activo (articular y cutáneo)</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " rowspan="2" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Cutáneo-articular refractaria• Rapidez de acción• Formulación oral• Experiencia en vida real escasa</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">SLE-BRAVE-II \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">SRI-4 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">47 vs. 46% (OR 1,5 (–7,1-10,2); p = 0,71) \t\t\t\t\t\t\n
\t\t\t\t</td></tr></tbody></table>
"""
]
"imagenFichero" => array:1 [
0 => "xTab3384968.png"
]
]
]
"notaPie" => array:1 [
0 => array:3 [
"identificador" => "tblfn0005"
"etiqueta" => "!"
"nota" => "<p class="elsevierStyleNotepara" id="npar0005">fármacos con indicación en otra enfermedad, y que en el momento actual no se encuentran en ficha técnica para el tratamiento del lupus eritematoso sistémico.</p>"
]
]
]
"descripcion" => array:1 [
"es" => "<p id="spar0020" class="elsevierStyleSimplePara elsevierViewall">Descripción de los principales tratamientos en el lupus eritematoso sistémico</p>"
]
]
2 => array:8 [
"identificador" => "tbl0010"
"etiqueta" => "Tabla 2"
"tipo" => "MULTIMEDIATABLA"
"mostrarFloat" => true
"mostrarDisplay" => false
"detalles" => array:1 [
0 => array:3 [
"identificador" => "at2"
"detalle" => "Tabla "
"rol" => "short"
]
]
"tabla" => array:2 [
"leyenda" => "<p id="spar0035" class="elsevierStyleSimplePara elsevierViewall">IL: interleucina; CAR-T: terapia de células T con receptores quiméricos de antígenos.</p>"
"tablatextoimagen" => array:1 [
0 => array:2 [
"tabla" => array:1 [
0 => """
<table border="0" frame="\n
\t\t\t\t\tvoid\n
\t\t\t\t" class=""><thead title="thead"><tr title="table-row"><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Molécula \t\t\t\t\t\t\n
\t\t\t\t\t\t</th><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Mecanismo de acción \t\t\t\t\t\t\n
\t\t\t\t\t\t</th><th class="td" title="\n
\t\t\t\t\ttable-head\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t" scope="col" style="border-bottom: 2px solid black">Estudios \t\t\t\t\t\t\n
\t\t\t\t\t\t</th></tr></thead><tbody title="tbody"><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleBold">Célula B</span> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Ianalumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anti receptor de BAFF \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0005" href="ctgov:NCT05639114">NCT05639114</span><span class="elsevierStyleInterRef" id="intr0010" href="ctgov:NCT05624749">NCT05624749</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Telitacicept \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anti BAFF y APRIL \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0015" href="ctgov:NCT05306574">NCT05306574</span><span class="elsevierStyleInterRef" id="intr0020" href="ctgov:NCT05899907">NCT05899907</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Daratumumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor selectivo del CD 38 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0025" href="ctgov:NCT04868838">NCT04868838</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Rozibafusp alfa \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor dual para Anti BAFF y anti ligando inducible de la coestimulación de célula T (ICOSL) \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0030" href="ctgov:NCT03845517">NCT03845517</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Obexelimab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anti CD19 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0035" href="ctgov:NCT02725515">NCT02725515</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " colspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleVsp" style="height:0.5px"></span></td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleBold">Célula T</span> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Mogamulizumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">anti-CCR4 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Sirolimus \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor del mTOR \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0040" href="ctgov:NCT04892212">NCT04892212</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Dapirolizumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anti CD 40 ligando \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0045" href="ctgov:NCT04294667">NCT04294667</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Mosunetuzumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor dual antiCD20 y CD3 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0050" href="ctgov:NCT05155345">NCT05155345</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidores duales \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Mosunetuzumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor dual CD20 y CD3 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0055" href="ctgov:NCT05155345">NCT05155345</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Rozibafusp Alfa \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor dual BAFF y el ligando inducible de la coestimulación con la célula T \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0060" href="ctgov:NCT04058028">NCT04058028</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " colspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleVsp" style="height:0.5px"></span></td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleBold">Células dendríticas</span> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Litifilimab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor del antígeno 2 de la célula dendrítica \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0065" href="ctgov:NCT04868838">NCT04868838</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleBold">Anti citoquinas</span> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Secukinumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anti IL-17 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0070" href="ctgov:NCT04181762">NCT04181762</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Guselkumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anti IL-23 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0075" href="ctgov:NCT04376827">NCT04376827</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleBold">Señalización intracelular</span> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Brepocitinib \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Anti JAK1 y TYK2 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0080" href="ctgov:NCT03845517">NCT03845517</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Deucreavacitinib \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor del TYK2 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0085" href="ctgov:NCT05617677">NCT05617677</span><span class="elsevierStyleInterRef" id="intr0090" href="ctgov:NCT05620407">NCT05620407</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Elsubrutinib/upadacitinib \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor de BTK y JAK1 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0095" href="ctgov:NCT03978520">NCT03978520</span><span class="elsevierStyleInterRef" id="intr0100" href="ctgov:NCT04451772">NCT04451772</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleBold">Proteosoma</span> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Iberdomida \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">modulador del proteosoma que promueve la ubiquitina E3 ligasa de unión a cereblón \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0105" href="ctgov:NCT03161483">NCT03161483</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleBold">Complemento</span> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Ravulizumab \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor del C5 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0110" href="ctgov:NCT04564339">NCT04564339</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Iptacopan \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">Inhibidor del factor B \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0115" href="ctgov:NCT05268289">NCT05268289</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " colspan="3" align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleVsp" style="height:0.5px"></span></td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleBold">Otras moléculas</span> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• IL-2 \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0120" href="ctgov:NCT04077684">NCT04077684</span><span class="elsevierStyleInterRef" id="intr0125" href="ctgov:NCT04680637">NCT04680637</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• Células madre mesenquimales \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0130" href="ctgov:NCT03917797">NCT03917797</span><span class="elsevierStyleInterRef" id="intr0135" href="ctgov:NCT03673748">NCT03673748</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr><tr title="table-row"><td class="td-with-role" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t ; entry_with_role_rowhead " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t">• CAR-T \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"> \t\t\t\t\t\t\n
\t\t\t\t</td><td class="td" title="\n
\t\t\t\t\ttable-entry\n
\t\t\t\t " align="left" valign="\n
\t\t\t\t\ttop\n
\t\t\t\t"><span class="elsevierStyleInterRef" id="intr0140" href="ctgov:NCT05085418">NCT05085418</span><span class="elsevierStyleInterRef" id="intr0145" href="ctgov:NCT05030779">NCT05030779</span> \t\t\t\t\t\t\n
\t\t\t\t</td></tr></tbody></table>
"""
]
"imagenFichero" => array:1 [
0 => "xTab3384967.png"
]
]
]
]
"descripcion" => array:1 [
"es" => "<p id="spar0030" class="elsevierStyleSimplePara elsevierViewall">Moléculas en investigación para el tratamiento del lupus eritematoso sistémico</p>"
]
]
]
"bibliografia" => array:2 [
"titulo" => "Bibliografía"
"seccion" => array:1 [
0 => array:2 [
"identificador" => "bibs0015"
"bibliografiaReferencia" => array:80 [
0 => array:3 [
"identificador" => "bib0405"
"etiqueta" => "1"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Novel paradigms in systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:2 [
0 => "T. Dorner"
1 => "R. Furie"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/s0140-6736(19)30546-x"
"Revista" => array:6 [
"tituloSerie" => "Lancet."
"fecha" => "2019"
"volumen" => "393"
"paginaInicial" => "2344"
"paginaFinal" => "2358"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/31180031"
"web" => "Medline"
]
]
]
]
]
]
]
]
1 => array:3 [
"identificador" => "bib0410"
"etiqueta" => "2"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "New insights into the immunopathogenesis of systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:4 [
0 => "G.C. Tsokos"
1 => "M.S. Lo"
2 => "P. Costa Reis"
3 => "K.E. Sullivan"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1038/nrrheum.2016.186"
"Revista" => array:6 [
"tituloSerie" => "Nat Rev Rheumatol."
"fecha" => "2016"
"volumen" => "12"
"paginaInicial" => "716"
"paginaFinal" => "730"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/27872476"
"web" => "Medline"
]
]
]
]
]
]
]
]
2 => array:3 [
"identificador" => "bib0415"
"etiqueta" => "3"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "TLR7 gain-of-function genetic variation causes human lupus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "G.J. Brown"
1 => "P.F. Cañete"
2 => "H. Wang"
3 => "A. Medhavy"
4 => "J. Bones"
5 => "J.A. Roco"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1038/s41586-022-04642-z"
"Revista" => array:6 [
"tituloSerie" => "Nature."
"fecha" => "2022"
"volumen" => "605"
"paginaInicial" => "349"
"paginaFinal" => "356"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/35477763"
"web" => "Medline"
]
]
]
]
]
]
]
]
3 => array:3 [
"identificador" => "bib0420"
"etiqueta" => "4"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Population-based lupus registries: advancing our epidemiologic understanding"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "S.S. Lim"
1 => "C. Drenkard"
2 => "W.J. McCune"
3 => "C.G. Helmick"
4 => "C. Gordon"
5 => "P. Deguire"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.24835"
"Revista" => array:6 [
"tituloSerie" => "Arthritis Rheum."
"fecha" => "2009"
"volumen" => "61"
"paginaInicial" => "1462"
"paginaFinal" => "1466"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/19790117"
"web" => "Medline"
]
]
]
]
]
]
]
]
4 => array:3 [
"identificador" => "bib0425"
"etiqueta" => "5"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Prevalence of systemic lupus erythematosus in Spain: higher than previously reported in other countries?"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "R. Cortes Verdu"
1 => "J.M. Pego-Reigosa"
2 => "D. Seoane-Mato"
3 => "M. Morcillo Valle"
4 => "D. Palma Sánchez"
5 => "M.J. Moreno Martínez"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1093/rheumatology/kez668"
"Revista" => array:5 [
"tituloSerie" => "Rheumatology (Oxford)."
"fecha" => "2020"
"volumen" => "59"
"paginaInicial" => "2556"
"paginaFinal" => "2562"
]
]
]
]
]
]
5 => array:3 [
"identificador" => "bib0430"
"etiqueta" => "6"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "46-Year Trends in Systemic Lupus Erythematosus Mortality in the United States, 1968 to 2013: A Nationwide Population-Based Study"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "E.Y. Yen"
1 => "M. Shaheen"
2 => "J.M.P. Woo"
3 => "N. Mercer"
4 => "N. Li"
5 => "D.K. McCurdy"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.7326/m17-0102"
"Revista" => array:6 [
"tituloSerie" => "Ann Intern Med."
"fecha" => "2017"
"volumen" => "167"
"paginaInicial" => "777"
"paginaFinal" => "785"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/29086801"
"web" => "Medline"
]
]
]
]
]
]
]
]
6 => array:3 [
"identificador" => "bib0435"
"etiqueta" => "7"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Trends in Hospital Admissions and Death Causes in Patients with Systemic Lupus Erythematosus: Spanish National Registry"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "V. Moreno-Torres"
1 => "C. Tarin"
2 => "G. Ruiz-Irastorza"
3 => "R. Castejón"
4 => "Á. Gutiérrez-Rojas"
5 => "A. Royuela"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.3390/jcm10245749"
"Revista" => array:5 [
"tituloSerie" => "J Clin Med."
"fecha" => "2021"
"volumen" => "10"
"paginaInicial" => "5749"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/34945045"
"web" => "Medline"
]
]
]
]
]
]
]
]
7 => array:3 [
"identificador" => "bib0440"
"etiqueta" => "8"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Infections in newly diagnosed Spanish patients with systemic lupus erythematosus: data from the RELES cohort"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "C. Gonzalez-Echavarri"
1 => "O. Capdevila"
2 => "G. Espinosa"
3 => "S. Suárez"
4 => "A. Marín-Ballvé"
5 => "R. González-León"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1177/0961203318811598"
"Revista" => array:6 [
"tituloSerie" => "Lupus."
"fecha" => "2018"
"volumen" => "27"
"paginaInicial" => "2253"
"paginaFinal" => "2261"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/30451641"
"web" => "Medline"
]
]
]
]
]
]
]
]
8 => array:3 [
"identificador" => "bib0445"
"etiqueta" => "9"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Glucocorticoids and irreversible damage in patients with systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:6 [
0 => "I. Ruiz-Arruza"
1 => "A. Ugarte"
2 => "I. Cabezas-Rodriguez"
3 => "J.A. Medina"
4 => "M.A. Moran"
5 => "G. Ruiz-Irastorza"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1093/rheumatology/keu148"
"Revista" => array:6 [
"tituloSerie" => "Rheumatology (Oxford)."
"fecha" => "2014"
"volumen" => "53"
"paginaInicial" => "1470"
"paginaFinal" => "1476"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/24681836"
"web" => "Medline"
]
]
]
]
]
]
]
]
9 => array:3 [
"identificador" => "bib0450"
"etiqueta" => "10"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Factors associated with damage accrual in patients with systemic lupus erythematosus: results from the Systemic Lupus International Collaborating Clinics (SLICC) Inception Cohort"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "I.N. Bruce"
1 => "A.G. O’Keeffe"
2 => "V. Farewell"
3 => "J.G. Hanly"
4 => "S. Manzi"
5 => "L. Su"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2013-205171"
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2015"
"volumen" => "74"
"paginaInicial" => "1706"
"paginaFinal" => "1713"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/24834926"
"web" => "Medline"
]
]
]
]
]
]
]
]
10 => array:3 [
"identificador" => "bib0455"
"etiqueta" => "11"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "The relationship between remission and health-related quality of life in a cohort of SLE patients"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:6 [
0 => "M.W.P. Tsang-A-Sjoe"
1 => "I.E.M. Bultink"
2 => "M. Heslinga"
3 => "L.H. van Tuyl"
4 => "R.F. van Vollenhoven"
5 => "A.E. Voskuyl"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1093/rheumatology/key349"
"Revista" => array:5 [
"tituloSerie" => "Rheumatology (Oxford)."
"fecha" => "2019"
"volumen" => "58"
"paginaInicial" => "628"
"paginaFinal" => "635"
]
]
]
]
]
]
11 => array:3 [
"identificador" => "bib0460"
"etiqueta" => "12"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Clinical characteristics during diagnosis of a prospective cohort of patients with systemic lupus erythematosus treated in Spanish Departments of Internal Medicine: The RELES study"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "J. Canora"
1 => "M. Garcia"
2 => "F. Mitjavila"
3 => "G. Espinosa"
4 => "S. Suárez"
5 => "R. González-León"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.rce.2016.09.006"
"Revista" => array:6 [
"tituloSerie" => "Rev Clin Esp (Barc)."
"fecha" => "2017"
"volumen" => "217"
"paginaInicial" => "7"
"paginaFinal" => "14"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/27793331"
"web" => "Medline"
]
]
]
]
]
]
]
]
12 => array:3 [
"identificador" => "bib0465"
"etiqueta" => "13"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "2019 update of the EULAR recommendations for the management of systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "A. Fanouriakis"
1 => "M. Kostopoulou"
2 => "A. Alunno"
3 => "M. Aringer"
4 => "I. Bajema"
5 => "J.N. Boletis"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2019-215089"
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2019"
"volumen" => "78"
"paginaInicial" => "736"
"paginaFinal" => "745"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/30926722"
"web" => "Medline"
]
]
]
]
]
]
]
]
13 => array:3 [
"identificador" => "bib0470"
"etiqueta" => "14"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "2021 DORIS definition of remission in SLE: final recommendations from an international task force"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "R.F. van Vollenhoven"
1 => "G. Bertsias"
2 => "A. Doria"
3 => "D. Isenberg"
4 => "E. Morand"
5 => "M.A. Petri"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/lupus-2021-000538"
"Revista" => array:5 [
"tituloSerie" => "Lupus Sci Med."
"fecha" => "2021"
"volumen" => "8"
"paginaInicial" => "e000538"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/34819388"
"web" => "Medline"
]
]
]
]
]
]
]
]
14 => array:3 [
"identificador" => "bib0475"
"etiqueta" => "15"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Treat-to-target in systemic lupus erythematosus: recommendations from an international task force"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "R.F. van Vollenhoven"
1 => "M. Mosca"
2 => "G. Bertsias"
3 => "D. Isenberg"
4 => "A. Kuhn"
5 => "K. Lerstrøm"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2013-205139"
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2014"
"volumen" => "73"
"paginaInicial" => "958"
"paginaFinal" => "967"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/24739325"
"web" => "Medline"
]
]
]
]
]
]
]
]
15 => array:3 [
"identificador" => "bib0480"
"etiqueta" => "16"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Definition and initial validation of a Lupus Low Disease Activity State (LLDAS)"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "K. Franklyn"
1 => "C.S. Lau"
2 => "S.V. Navarra"
3 => "W. Louthrenoo"
4 => "A. Lateef"
5 => "L. Hamijoyo"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2015-207726"
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2016"
"volumen" => "75"
"paginaInicial" => "1615"
"paginaFinal" => "1621"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/26458737"
"web" => "Medline"
]
]
]
]
]
]
]
]
16 => array:3 [
"identificador" => "bib0485"
"etiqueta" => "17"
"referencia" => array:1 [
0 => array:1 [
"referenciaCompleta" => "Grupo de trabajo de la Guía de Práctica Clínica sobre Lupus Eritematoso Sistémico. Guía de práctica clínica sobre lupus eritematoso sistémico. Ministerio de Sanidad, Servicios Sociales e Igualdad. Servicio de Evaluación del Servicio Canario de la Salud, 2014; [consultado 1 Ago 2023]. Disponible en: <a target="_blank" href="https://portal.guiasalud.es/gpc/lupus-eritematoso-sistemico/">https://portal.guiasalud.es/gpc/lupus-eritematoso-sistemico/</a>"
]
]
]
17 => array:3 [
"identificador" => "bib0490"
"etiqueta" => "18"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy and safety of belimumab in patients with active systemic lupus erythematosus: a randomised, placebo-controlled, phase 3 trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "S.V. Navarra"
1 => "R.M. Guzman"
2 => "A.E. Gallacher"
3 => "S. Hall"
4 => "R.A. Levy"
5 => "R.E. Jimenez"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/s0140-6736(10)61354-2"
"Revista" => array:6 [
"tituloSerie" => "Lancet."
"fecha" => "2011"
"volumen" => "377"
"paginaInicial" => "721"
"paginaFinal" => "731"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/21296403"
"web" => "Medline"
]
]
]
]
]
]
]
]
18 => array:3 [
"identificador" => "bib0495"
"etiqueta" => "19"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "A phase III, randomized, placebo-controlled study of belimumab, a monoclonal antibody that inhibits B lymphocyte stimulator, in patients with systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "R. Furie"
1 => "M. Petri"
2 => "O. Zamani"
3 => "R. Cervera"
4 => "D.J. Wallace"
5 => "D. Tegzová"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.30613"
"Revista" => array:6 [
"tituloSerie" => "Arthritis Rheum."
"fecha" => "2011"
"volumen" => "63"
"paginaInicial" => "3918"
"paginaFinal" => "3930"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/22127708"
"web" => "Medline"
]
]
]
]
]
]
]
]
19 => array:3 [
"identificador" => "bib0500"
"etiqueta" => "20"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Grupo de Trabajo de Enfermedades Autoinmunes Sistemicas de la Sociedad Espa nola de Medicina I. [Belimumab in systemic lupus erythematosus: a guide for its use in the daily practice]"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:4 [
0 => "M. Ramos-Casals"
1 => "G. Ruiz-Irastorza"
2 => "J. Jimenez-Alonso"
3 => "M.A. Khamashta"
]
]
]
]
]
"host" => array:1 [
0 => array:1 [
"Revista" => array:6 [
"tituloSerie" => "Rev Clin Esp (Barc)."
"fecha" => "2013"
"volumen" => "213"
"paginaInicial" => "66"
"paginaFinal" => "67"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/23565550"
"web" => "Medline"
]
]
]
]
]
]
]
]
20 => array:3 [
"identificador" => "bib0505"
"etiqueta" => "21"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Effectiveness, Tolerability, and Safety of Belimumab in Patients with Refractory SLE: a Review of Observational Clinical-Practice-Based Studies"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "F. Trentin"
1 => "M. Gatto"
2 => "M. Zen"
3 => "M. Larosa"
4 => "L. Maddalena"
5 => "L. Nalotto"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1007/s12016-018-8675-2"
"Revista" => array:5 [
"tituloSerie" => "Clin Rev Allergy Immunol."
"fecha" => "2018"
"volumen" => "54"
"paginaInicial" => "331"
"paginaFinal" => "343"
]
]
]
]
]
]
21 => array:3 [
"identificador" => "bib0510"
"etiqueta" => "22"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Long-term safety and limited organ damage in patients with systemic lupus erythematosus treated with belimumab: a Phase III study extension"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "R.F. van Vollenhoven"
1 => "S.V. Navarra"
2 => "R.A. Levy"
3 => "M. Thomas"
4 => "A. Heath"
5 => "T. Lustine"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1093/rheumatology/kez279"
"Revista" => array:6 [
"tituloSerie" => "Rheumatology (Oxford)."
"fecha" => "2020"
"volumen" => "59"
"paginaInicial" => "281"
"paginaFinal" => "291"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/31302695"
"web" => "Medline"
]
]
]
]
]
]
]
]
22 => array:3 [
"identificador" => "bib0515"
"etiqueta" => "23"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Two-Year, Randomized, Controlled Trial of Belimumab in Lupus Nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "R. Furie"
1 => "B.H. Rovin"
2 => "F. Houssiau"
3 => "A. Malvar"
4 => "Y.K.O. Teng"
5 => "G. Contreras"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1056/nejmoa2001180"
"Revista" => array:6 [
"tituloSerie" => "N Engl J Med."
"fecha" => "2020"
"volumen" => "383"
"paginaInicial" => "1117"
"paginaFinal" => "1128"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/32937045"
"web" => "Medline"
]
]
]
]
]
]
]
]
23 => array:3 [
"identificador" => "bib0520"
"etiqueta" => "24"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "A phase II, randomized, double-blind, placebo-controlled, dose-ranging study of belimumab in patients with active systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "D.J. Wallace"
1 => "W. Stohl"
2 => "R.A. Furie"
3 => "J.R. Lisse"
4 => "J.D. McKay"
5 => "J.T. Merrill"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.24699"
"Revista" => array:5 [
"tituloSerie" => "Arthritis Rheum."
"fecha" => "2009"
"volumen" => "61"
"paginaInicial" => "1168"
"paginaFinal" => "1178"
]
]
]
]
]
]
24 => array:3 [
"identificador" => "bib0525"
"etiqueta" => "25"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Safety and efficacy of intravenous belimumab in children with systemic lupus erythematosus: results from a randomised, placebo-controlled trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "H.I. Brunner"
1 => "C. Abud-Mendoza"
2 => "D.O. Viola"
3 => "I. Calvo Penades"
4 => "D. Levy"
5 => "J. Anton"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2020-217101"
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2020"
"volumen" => "79"
"paginaInicial" => "1340"
"paginaFinal" => "1348"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/32699034"
"web" => "Medline"
]
]
]
]
]
]
]
]
25 => array:3 [
"identificador" => "bib0530"
"etiqueta" => "26"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "KDOQI US Commentary on the 2021 KDIGO Clinical Practice Guideline for the Management of Glomerular Diseases"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "L.H. Beck Jr."
1 => "I. Ayoub"
2 => "D. Caster"
3 => "M.J. Choi"
4 => "J. Cobb"
5 => "D. Geetha"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1053/j.ajkd.2023.02.003"
"Revista" => array:6 [
"tituloSerie" => "Am J Kidney Dis."
"fecha" => "2023"
"volumen" => "82"
"paginaInicial" => "121"
"paginaFinal" => "175"
"link" => array:1 [
0 => array:2 [
"url" => "https://www.ncbi.nlm.nih.gov/pubmed/37341661"
"web" => "Medline"
]
]
]
]
]
]
]
]
26 => array:3 [
"identificador" => "bib0535"
"etiqueta" => "27"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy of belimumab on renal outcomes in patients with systemic lupus erythematosus: A systematic review"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "S. Sciascia"
1 => "M. Radin"
2 => "J. Yazdany"
3 => "R.A. Levy"
4 => "D. Roccatello"
5 => "M. Dall’Era"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.autrev.2017.01.010"
"Revista" => array:5 [
"tituloSerie" => "Autoimmun Rev."
"fecha" => "2017"
"volumen" => "16"
"paginaInicial" => "287"
"paginaFinal" => "293"
]
]
]
]
]
]
27 => array:3 [
"identificador" => "bib0540"
"etiqueta" => "28"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy and Safety of Subcutaneous Belimumab in Systemic Lupus Erythematosus: A Fifty-Two-Week Randomized, Double-Blind, Placebo-Controlled Study"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "W. Stohl"
1 => "A. Schwarting"
2 => "M. Okada"
3 => "M. Scheinberg"
4 => "A. Doria"
5 => "A.E. Hammer"
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.40049"
"Revista" => array:5 [
"tituloSerie" => "Arthritis Rheumatol."
"fecha" => "2017"
"volumen" => "69"
"paginaInicial" => "1016"
"paginaFinal" => "1027"
]
]
]
]
]
]
28 => array:3 [
"identificador" => "bib0545"
"etiqueta" => "29"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Predictive Factors of the Use of Rituximab and Belimumab in Spanish Lupus Patients"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [
0 => "O. Capdevila"
1 => "F. Mitjavila"
2 => "G. Espinosa"
3 => "L. Caminal-Montero"
…2
]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.3390/medicina59081362"
"Revista" => array:5 [
"tituloSerie" => "Medicina (Kaunas)."
"fecha" => "2023"
"volumen" => "59"
"paginaInicial" => "1362"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
29 => array:3 [
"identificador" => "bib0550"
"etiqueta" => "30"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Effects of Belimumab on Flare Rate and Expected Damage Progression in Patients With Active Systemic Lupus Erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/acr.22971"
"Revista" => array:6 [
"tituloSerie" => "Arthritis Care Res (Hoboken)."
"fecha" => "2017"
"volumen" => "69"
"paginaInicial" => "115"
"paginaFinal" => "123"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
30 => array:3 [
"identificador" => "bib0555"
"etiqueta" => "31"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Belimumab and antimalarials combined against renal flares in patients treated for extra-renal systemic lupus erythematosus: results from 4 phase III clinical trials"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:4 [ …4]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1093/rheumatology/kead253"
"Revista" => array:3 [
"tituloSerie" => "Rheumatology (Oxford)."
"fecha" => "2023"
"paginaInicial" => "kead253"
]
]
]
]
]
]
31 => array:3 [
"identificador" => "bib0560"
"etiqueta" => "32"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Early Disease and Low Baseline Damage as Predictors of Response to Belimumab in Patients With Systemic Lupus Erythematosus in a Real-Life Setting"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.41253"
"Revista" => array:5 [
"tituloSerie" => "Arthritis Rheumatol."
"fecha" => "2020"
"volumen" => "72"
"paginaInicial" => "1314"
"paginaFinal" => "1324"
]
]
]
]
]
]
32 => array:3 [
"identificador" => "bib0565"
"etiqueta" => "33"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Management of non-renal manifestations of systemic lupus erythematosus: A systematic literature review for the APLAR consensus statements"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1111/1756-185x.14413"
"Revista" => array:6 [
"tituloSerie" => "Int J Rheum Dis."
"fecha" => "2022"
"volumen" => "25"
"paginaInicial" => "1220"
"paginaFinal" => "1229"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
33 => array:3 [
"identificador" => "bib0570"
"etiqueta" => "34"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Executive summary of the KDIGO 2021 Guideline for the Management of Glomerular Diseases"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.kint.2021.05.015"
"Revista" => array:5 [
"tituloSerie" => "Kidney Int."
"fecha" => "2021"
"volumen" => "100"
"paginaInicial" => "753"
"paginaFinal" => "779"
]
]
]
]
]
]
34 => array:3 [
"identificador" => "bib0575"
"etiqueta" => "35"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "2019 Update of the Joint European League Against Rheumatism and European Renal Association-European Dialysis and Transplant Association (EULAR/ERA-EDTA) recommendations for the management of lupus nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2020-216924"
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2020"
"volumen" => "79"
"paginaInicial" => "713"
"paginaFinal" => "723"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
35 => array:3 [
"identificador" => "bib0580"
"etiqueta" => "36"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Consensus document of the Spanish Group for the Study of the Glomerular Diseases (GLOSEN) for the diagnosis and treatment of lupus nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.nefroe.2023.05.006"
"Revista" => array:6 [
"tituloSerie" => "Nefrologia (Engl Ed)."
"fecha" => "2023"
"volumen" => "43"
"paginaInicial" => "6"
"paginaFinal" => "47"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
36 => array:3 [
"identificador" => "bib0585"
"etiqueta" => "37"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "A secondary analysis of the Belimumab International Study in Lupus Nephritis trial examined effects of belimumab on kidney outcomes and preservation of kidney function in patients with lupus nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.kint.2021.08.027"
"Revista" => array:6 [
"tituloSerie" => "Kidney Int."
"fecha" => "2022"
"volumen" => "101"
"paginaInicial" => "403"
"paginaFinal" => "413"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
37 => array:3 [
"identificador" => "bib0590"
"etiqueta" => "38"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy and safety of voclosporin versus placebo for lupus nephritis (AURORA 1): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/s0140-6736(21)00578-x"
"Revista" => array:6 [
"tituloSerie" => "Lancet."
"fecha" => "2021"
"volumen" => "397"
"paginaInicial" => "2070"
"paginaFinal" => "2080"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
38 => array:3 [
"identificador" => "bib0595"
"etiqueta" => "39"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Eurolupus cyclophosphamide plus repeated pulses of methyl-prednisolone for the induction therapy of class III, IV and V lupus nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.autrev.2021.102898"
"Revista" => array:5 [
"tituloSerie" => "Autoimmun Rev."
"fecha" => "2021"
"volumen" => "20"
"paginaInicial" => "102898"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
39 => array:3 [
"identificador" => "bib0600"
"etiqueta" => "40"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "The effect of 24-week belimumab treatment withdrawal followed by treatment restart in patients with SLE: an open-label, non-randomised 52-week study"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1186/s13075-022-02723-y"
"Revista" => array:5 [
"tituloSerie" => "Arthritis Res Ther."
"fecha" => "2022"
"volumen" => "24"
"paginaInicial" => "46"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
40 => array:3 [
"identificador" => "bib0605"
"etiqueta" => "41"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy and safety of off-label use of rituximab in refractory lupus: data from the Italian Multicentre Registry"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:1 [
"Revista" => array:6 [
"tituloSerie" => "Clin Exp Rheumatol."
"fecha" => "2015"
"volumen" => "33"
"paginaInicial" => "449"
"paginaFinal" => "456"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
41 => array:3 [
"identificador" => "bib0610"
"etiqueta" => "42"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy and safety of rituximab in the treatment of non-renal systemic lupus erythematosus: a systematic review"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.semarthrit.2014.04.002"
"Revista" => array:6 [
"tituloSerie" => "Semin Arthritis Rheum."
"fecha" => "2014"
"volumen" => "44"
"paginaInicial" => "175"
"paginaFinal" => "185"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
42 => array:3 [
"identificador" => "bib0615"
"etiqueta" => "43"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy of rituximab in 164 patients with biopsy-proven lupus nephritis: pooled data from European cohorts"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.autrev.2011.10.009"
"Revista" => array:6 [
"tituloSerie" => "Autoimmun Rev."
"fecha" => "2012"
"volumen" => "11"
"paginaInicial" => "357"
"paginaFinal" => "364"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
43 => array:3 [
"identificador" => "bib0620"
"etiqueta" => "44"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy and safety of rituximab in moderately-to-severely active systemic lupus erythematosus: the randomized, double-blind, phase II/III systemic lupus erythematosus evaluation of rituximab trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.27233"
"Revista" => array:5 [
"tituloSerie" => "Arthritis Rheum."
"fecha" => "2010"
"volumen" => "62"
"paginaInicial" => "222"
"paginaFinal" => "233"
]
]
]
]
]
]
44 => array:3 [
"identificador" => "bib0625"
"etiqueta" => "45"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy and safety of rituximab in patients with active proliferative lupus nephritis: the Lupus Nephritis Assessment with Rituximab study"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.34359"
"Revista" => array:6 [
"tituloSerie" => "Arthritis Rheum."
"fecha" => "2012"
"volumen" => "64"
"paginaInicial" => "1215"
"paginaFinal" => "1226"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
45 => array:3 [
"identificador" => "bib0630"
"etiqueta" => "46"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Beyond the LUNAR trial. Efficacy of rituximab in refractory lupus nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:4 [ …4]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1093/ndt/gfs285"
"Revista" => array:6 [
"tituloSerie" => "Nephrol Dial Transplant."
"fecha" => "2013"
"volumen" => "28"
"paginaInicial" => "106"
"paginaFinal" => "111"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
46 => array:3 [
"identificador" => "bib0635"
"etiqueta" => "47"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Differential effects on BAFF and APRIL levels in rituximab-treated patients with systemic lupus erythematosus and rheumatoid arthritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1186/ar2076"
"Revista" => array:5 [
"tituloSerie" => "Arthritis Res Ther."
"fecha" => "2006"
"volumen" => "8"
"paginaInicial" => "R167"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
47 => array:3 [
"identificador" => "bib0640"
"etiqueta" => "48"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Effectiveness of Belimumab After Rituximab in Systemic Lupus Erythematosus: A Randomized Controlled Trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.7326/M21-2078"
"Revista" => array:6 [
"tituloSerie" => "Ann Intern Med."
"fecha" => "2021"
"volumen" => "174"
"paginaInicial" => "1647"
"paginaFinal" => "1657"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
48 => array:3 [
"identificador" => "bib0645"
"etiqueta" => "49"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Phase III, multicentre, randomised, double-blind, placebo-controlled, 104-week study of subcutaneous belimumab administered in combination with rituximab in adults with systemic lupus erythematosus (SLE): BLISS-BELIEVE study protocol"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/bmjopen-2018-025687"
"Revista" => array:5 [
"tituloSerie" => "BMJ Open."
"fecha" => "2019"
"volumen" => "9"
"paginaInicial" => "e025687"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
49 => array:3 [
"identificador" => "bib0650"
"etiqueta" => "50"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Phase II Randomized Trial of Rituximab Plus Cyclophosphamide Followed by Belimumab for the Treatment of Lupus Nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.41466"
"Revista" => array:6 [
"tituloSerie" => "Arthritis Rheumatol."
"fecha" => "2021"
"volumen" => "73"
"paginaInicial" => "121"
"paginaFinal" => "131"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
50 => array:3 [
"identificador" => "bib0655"
"etiqueta" => "51"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "The NET-effect of combining rituximab with belimumab in severe systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.jaut.2018.03.003"
"Revista" => array:6 [
"tituloSerie" => "J Autoimmun."
"fecha" => "2018"
"volumen" => "91"
"paginaInicial" => "45"
"paginaFinal" => "54"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
51 => array:3 [
"identificador" => "bib0660"
"etiqueta" => "52"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Binding mechanisms of therapeutic antibodies to human CD20"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:5 [ …5]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1126/science.abb8008"
"Revista" => array:6 [
"tituloSerie" => "Science."
"fecha" => "2020"
"volumen" => "369"
"paginaInicial" => "793"
"paginaFinal" => "799"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
52 => array:3 [
"identificador" => "bib0665"
"etiqueta" => "53"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "B-cell depletion with obinutuzumab for the treatment of proliferative lupus nephritis: a randomised, double-blind, placebo-controlled trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2021-220920"
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2022"
"volumen" => "81"
"paginaInicial" => "100"
"paginaFinal" => "107"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
53 => array:3 [
"identificador" => "bib0670"
"etiqueta" => "54"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "B cell-activating factor of the tumor necrosis factor family (BAFF) is expressed under stimulation by interferon in salivary gland epithelial cells in primary Sjogren's syndrome"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1186/ar1912"
"Revista" => array:5 [
"tituloSerie" => "Arthritis Res Ther."
"fecha" => "2006"
"volumen" => "8"
"paginaInicial" => "R51"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
54 => array:3 [
"identificador" => "bib0675"
"etiqueta" => "55"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Interferon-inducible gene expression signature in peripheral blood cells of patients with severe lupus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1073/pnas.0337679100"
"Revista" => array:6 [
"tituloSerie" => "Proc Natl Acad Sci U S A."
"fecha" => "2003"
"volumen" => "100"
"paginaInicial" => "2610"
"paginaFinal" => "2615"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
55 => array:3 [
"identificador" => "bib0680"
"etiqueta" => "56"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Anifrolumab, an Anti–Interferon-α Receptor Monoclonal Antibody, in Moderate-to-Severe Systemic Lupus Erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.39962"
"Revista" => array:6 [
"tituloSerie" => "Arthritis Rheumatol."
"fecha" => "2017"
"volumen" => "69"
"paginaInicial" => "376"
"paginaFinal" => "386"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
56 => array:3 [
"identificador" => "bib0685"
"etiqueta" => "57"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Type I interferon inhibitor anifrolumab in active systemic lupus erythematosus (TULIP-1): a randomised, controlled, phase 3 trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/S2665-9913(19)30076-1"
"Revista" => array:5 [
"tituloSerie" => "Lancet Rheumatology."
"fecha" => "2019"
"volumen" => "1"
"paginaInicial" => "e208"
"paginaFinal" => "e219"
]
]
]
]
]
]
57 => array:3 [
"identificador" => "bib0690"
"etiqueta" => "58"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Trial of Anifrolumab in Active Systemic Lupus Erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1056/nejmoa1912196"
"Revista" => array:6 [
"tituloSerie" => "N Engl J Med."
"fecha" => "2020"
"volumen" => "382"
"paginaInicial" => "211"
"paginaFinal" => "221"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
58 => array:3 [
"identificador" => "bib0695"
"etiqueta" => "59"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Concordance and discordance in SLE clinical trial outcome measures: analysis of three anifrolumab phase 2/3 trials"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2021-221847"
"Revista" => array:5 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2022"
"volumen" => "81"
"paginaInicial" => "962"
"paginaFinal" => "969"
]
]
]
]
]
]
59 => array:3 [
"identificador" => "bib0700"
"etiqueta" => "60"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Efficacy of anifrolumab across organ domains in patients with moderate-to-severe systemic lupus erythematosus: a post-hoc analysis of pooled data from the TULIP-1 and TULIP-2 trials"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/S2665-9913(21)00317-9"
"Revista" => array:5 [
"tituloSerie" => "Lancet Rheumatology."
"fecha" => "2022"
"volumen" => "4"
"paginaInicial" => "e282"
"paginaFinal" => "e292"
]
]
]
]
]
]
60 => array:3 [
"identificador" => "bib0705"
"etiqueta" => "61"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Lupus low disease activity state attainment in the phase 3 TULIP trials of anifrolumab in active systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:5 [ …5]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/ard-2022-222748"
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2023"
"volumen" => "82"
"paginaInicial" => "639"
"paginaFinal" => "645"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
61 => array:3 [
"identificador" => "bib0710"
"etiqueta" => "62"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Phase II randomised trial of type I interferon inhibitor anifrolumab in patients with active lupus nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1136/annrheumdis-2021-221478"
"Revista" => array:5 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2022"
"volumen" => "81"
"paginaInicial" => "496"
"paginaFinal" => "506"
]
]
]
]
]
]
62 => array:3 [
"identificador" => "bib0715"
"etiqueta" => "63"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Long-Term Safety and Efficacy of Anifrolumab in Adults With Systemic Lupus Erythematosus: Results of a Phase II Open-Label Extension Study"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.41598"
"Revista" => array:6 [
"tituloSerie" => "Arthritis Rheumatol."
"fecha" => "2021"
"volumen" => "73"
"paginaInicial" => "816"
"paginaFinal" => "825"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
63 => array:3 [
"identificador" => "bib0720"
"etiqueta" => "64"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "An evaluation of voclosporin for the treatment of lupus nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:2 [ …2]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1080/14656566.2018.1516751"
"Revista" => array:6 [
"tituloSerie" => "Expert Opin Pharmacother."
"fecha" => "2018"
"volumen" => "19"
"paginaInicial" => "1613"
"paginaFinal" => "1621"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
64 => array:3 [
"identificador" => "bib0725"
"etiqueta" => "65"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Safety and efficacy of long-term voclosporin treatment for lupus nephritis in the Phase 3 AURORA 2 clinical trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.42657"
"Revista" => array:2 [
"tituloSerie" => "Arthritis Rheumatol."
"fecha" => "2023"
]
]
]
]
]
]
65 => array:3 [
"identificador" => "bib0730"
"etiqueta" => "66"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Janus kinase-targeting therapies in rheumatology: a mechanisms-based approach"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:4 [ …4]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1038/s41584-021-00726-8"
"Revista" => array:6 [
"tituloSerie" => "Nat Rev Rheumatol."
"fecha" => "2022"
"volumen" => "18"
"paginaInicial" => "133"
"paginaFinal" => "145"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
66 => array:3 [
"identificador" => "bib0735"
"etiqueta" => "67"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "JAK/STAT signaling controls the fate of CD8(+)CD103(+) tissue-resident memory T cell in lupus nephritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/j.jaut.2020.102424"
"Revista" => array:5 [
"tituloSerie" => "J Autoimmun."
"fecha" => "2020"
"volumen" => "109"
"paginaInicial" => "102424"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
67 => array:3 [
"identificador" => "bib0740"
"etiqueta" => "68"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Phase 1 double-blind randomized safety trial of the Janus kinase inhibitor tofacitinib in systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1038/s41467-021-23361-z"
"Revista" => array:5 [
"tituloSerie" => "Nat Commun."
"fecha" => "2021"
"volumen" => "12"
"paginaInicial" => "3391"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
68 => array:3 [
"identificador" => "bib0745"
"etiqueta" => "69"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Cardiovascular and Cancer Risk with Tofacitinib in Rheumatoid Arthritis"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1056/NEJMoa2109927"
"Revista" => array:6 [
"tituloSerie" => "N Engl J Med."
"fecha" => "2022"
"volumen" => "386"
"paginaInicial" => "316"
"paginaFinal" => "326"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
69 => array:3 [
"identificador" => "bib0750"
"etiqueta" => "70"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Tofacitinib for refractory chilblain lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:3 [ …3]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1111/ijd.15625"
"Revista" => array:6 [
"tituloSerie" => "Int J Dermatol."
"fecha" => "2022"
"volumen" => "61"
"paginaInicial" => "e156"
"paginaFinal" => "e157"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
70 => array:3 [
"identificador" => "bib0755"
"etiqueta" => "71"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Baricitinib for systemic lupus erythematosus: a double-blind, randomised, placebo-controlled, phase 2 trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/s0140-6736(18)31363-1"
"Revista" => array:6 [
"tituloSerie" => "Lancet."
"fecha" => "2018"
"volumen" => "392"
"numero" => "10143"
"paginaInicial" => "222"
"paginaFinal" => "231"
]
]
]
]
]
]
71 => array:3 [
"identificador" => "bib0760"
"etiqueta" => "72"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Baricitinib for systemic lupus erythematosus: a double-blind, randomised, placebo-controlled, phase 3 trial (SLE-BRAVE-I)"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/s0140-6736(22)02607-1"
"Revista" => array:7 [
"tituloSerie" => "Lancet."
"fecha" => "2023"
"volumen" => "401"
"numero" => "10381"
"paginaInicial" => "1001"
"paginaFinal" => "1010"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
72 => array:3 [
"identificador" => "bib0765"
"etiqueta" => "73"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Baricitinib for systemic lupus erythematosus: a double-blind, randomised, placebo-controlled, phase 3 trial (SLE-BRAVE-II)"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1016/s0140-6736(22)02546-6"
"Revista" => array:7 [
"tituloSerie" => "Lancet."
"fecha" => "2023"
"volumen" => "401"
"numero" => "10381"
"paginaInicial" => "1011"
"paginaFinal" => "1019"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
73 => array:3 [
"identificador" => "bib0770"
"etiqueta" => "74"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Deucravacitinib, a Tyrosine Kinase 2 Inhibitor, in Systemic Lupus Erythematosus: A Phase II, Randomized, Double-Blind, Placebo-Controlled Trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1002/art.42391"
"Revista" => array:6 [
"tituloSerie" => "Arthritis Rheumatol."
"fecha" => "2023"
"volumen" => "75"
"paginaInicial" => "242"
"paginaFinal" => "252"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
74 => array:3 [
"identificador" => "bib0775"
"etiqueta" => "75"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "OP0139 Efficacy and safety of abbv-599 high dose (elsubrutinib 60 mg and upadacitinib 30 mg) and upadacitinib monotherapy for the treatment of systemic lupus erythematosus: a phase 2, double-blind, placebo-controlled trial"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:1 [
"Revista" => array:6 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2023"
"volumen" => "82"
"numero" => "Suppl 1"
"paginaInicial" => "91"
"paginaFinal" => "92"
]
]
]
]
]
]
75 => array:3 [
"identificador" => "bib0780"
"etiqueta" => "76"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Treating systemic lupus erythematosus in the 21st century: new drugs and new perspectives on old drugs"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:2 [ …2]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1093/rheumatology/keaa403"
"Revista" => array:7 [
"tituloSerie" => "Rheumatology (Oxford)."
"fecha" => "2020"
"volumen" => "59"
"numero" => "Suppl 5"
"paginaInicial" => "v69"
"paginaFinal" => "v81"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
76 => array:3 [
"identificador" => "bib0785"
"etiqueta" => "77"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "EULAR recommendations for the management of systemic lupus erythematosus: 2023 update"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:1 [
"Revista" => array:3 [
"tituloSerie" => "Ann Rheum Dis."
"fecha" => "2023"
"volumen" => "ard-2023-224762"
]
]
]
]
]
]
77 => array:3 [
"identificador" => "bib0790"
"etiqueta" => "78"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Early predictors of renal outcome in patients with proliferative lupus nephritis: a 36-month cohort study"
"autores" => array:1 [
0 => array:2 [
"etal" => false
"autores" => array:5 [ …5]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.1093/rheumatology/keab126"
"Revista" => array:6 [
"tituloSerie" => "Rheumatology."
"fecha" => "2021"
"volumen" => "60"
"paginaInicial" => "5134"
"paginaFinal" => "5141"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
78 => array:3 [
"identificador" => "bib0795"
"etiqueta" => "79"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Predictors of Early Response, Flares, and Long-Term Adverse Renal Outcomes in Proliferative Lupus Nephritis: A 100-Month Median Follow-Up of an Inception Cohort"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:2 [
"doi" => "10.3390/jcm11175017"
"Revista" => array:5 [
"tituloSerie" => "J Clin Med."
"fecha" => "2022"
"volumen" => "11"
"paginaInicial" => "5017"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
79 => array:3 [
"identificador" => "bib0800"
"etiqueta" => "80"
"referencia" => array:1 [
0 => array:2 [
"contribucion" => array:1 [
0 => array:2 [
"titulo" => "Comparative study between two European inception cohorts of patients with early systemic lupus erythematosus"
"autores" => array:1 [
0 => array:2 [
"etal" => true
"autores" => array:6 [ …6]
]
]
]
]
"host" => array:1 [
0 => array:1 [
"Revista" => array:6 [
"tituloSerie" => "Clin Exp Rheumatol."
"fecha" => "2020"
"volumen" => "38"
"paginaInicial" => "925"
"paginaFinal" => "932"
"link" => array:1 [
0 => array:2 [ …2]
]
]
]
]
]
]
]
]
]
]
]
]
"idiomaDefecto" => "es"
"url" => "/00142565/0000022300000010/v1_202312070441/S0014256523001893/v1_202312070441/es/main.assets"
"Apartado" => array:4 [
"identificador" => "71063"
"tipo" => "SECCION"
"en" => array:2 [
"titulo" => "Revisión"
"idiomaDefecto" => true
]
"idiomaDefecto" => "en"
]
"PDF" => "https://static.elsevier.es/multimedia/00142565/0000022300000010/v1_202312070441/S0014256523001893/v1_202312070441/es/main.pdf?idApp=WRCEE&text.app=https://www.revclinesp.es/"
"EPUB" => "https://multimedia.elsevier.es/PublicationsMultimediaV1/item/epub/S0014256523001893?idApp=WRCEE"
]