El Registro Informatizado de Enfermedad Tromboembólica (RIETE) es un registro prospectivo que incluye de forma consecutiva pacientes diagnosticados de enfermedad tromboembólica venosa. Hemos comparado la presentación clínica y la respuesta al tratamiento anticoagulante en pacientes con enfermedad tromboembólica venosa idiopática (ETEVI) versus secundaria (ETEVS, asociada a algún factor de riesgo).
Pacientes y métodosSe analizaron las diferencias en las características clínicas, comorbilidad, tratamiento y episodios durante los primeros 3meses tras el diagnóstico de ETEV en los pacientes con ETEVI o ETEVS y según su presentación clínica inicial.
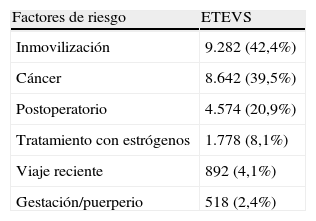
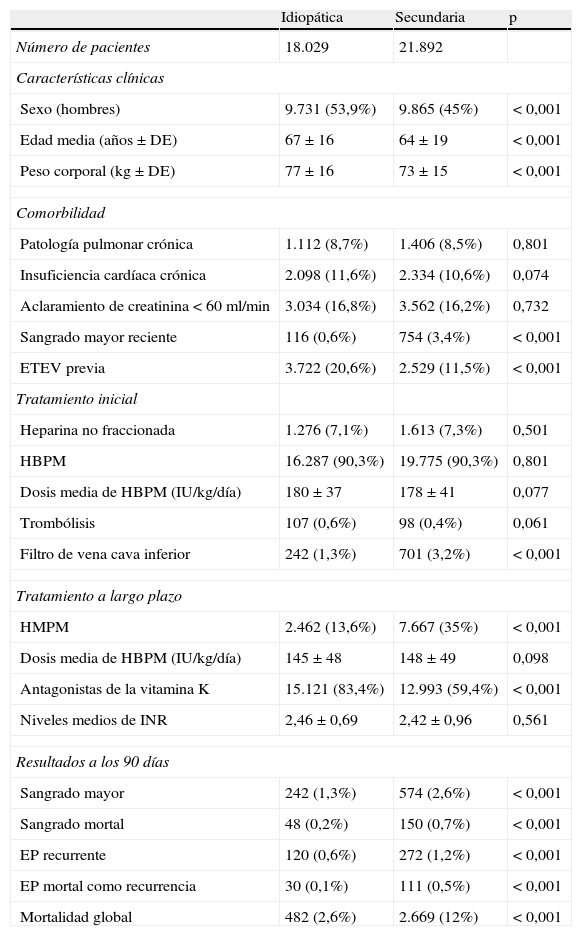
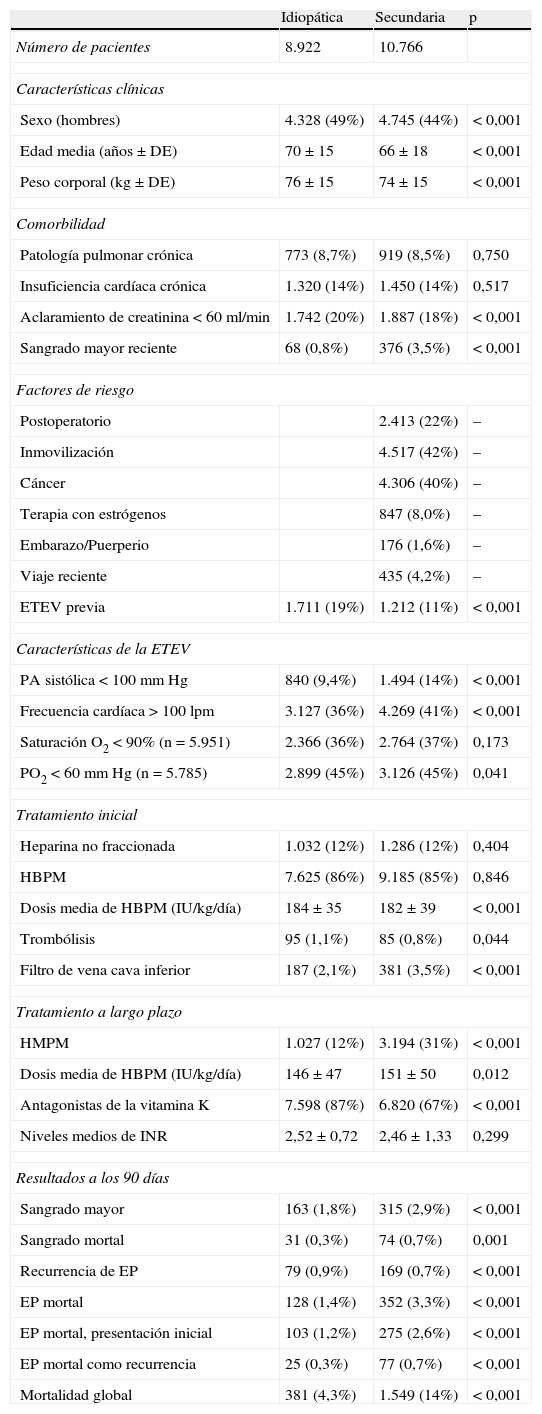
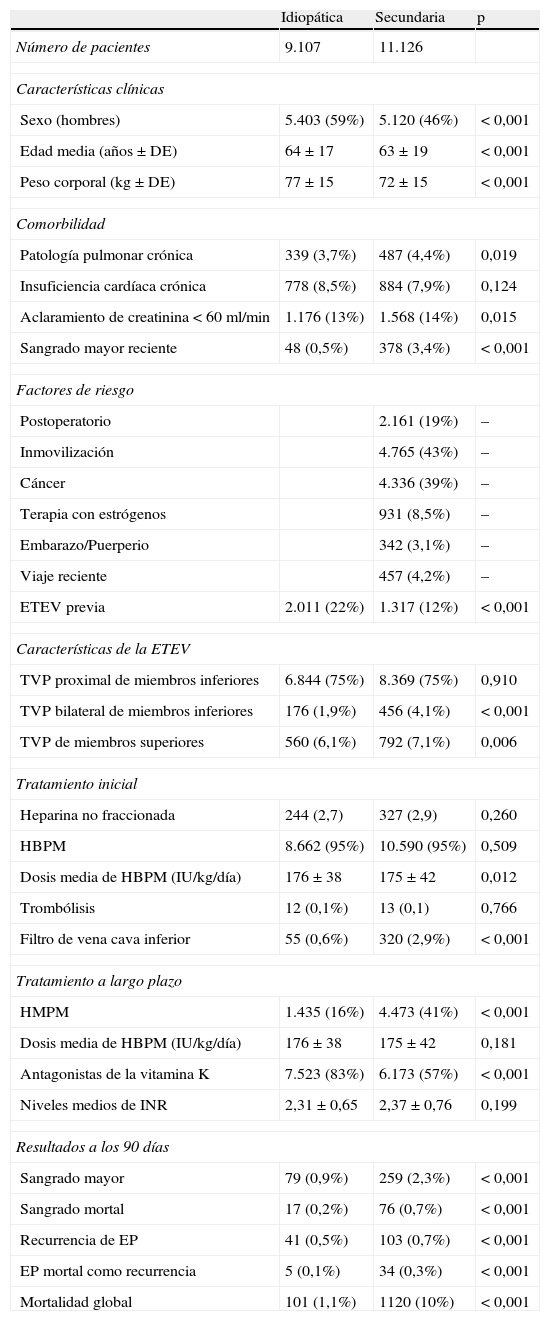
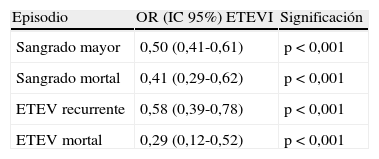
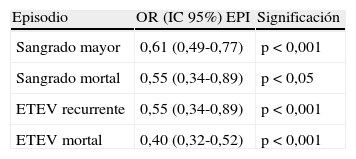
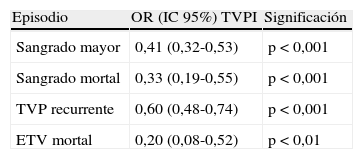
ResultadosSe incluyeron 39.921 pacientes, con ETEVI (n=18.029; 45,1%) o ETEVS (n=21.892; 54,9%). Los pacientes con ETEVI mostraron más antecedentes de ETEV que los diagnosticados de ETEVS (p<0,001). El tratamiento inicial fue similar en ambos grupos, pero se colocaron más filtros de vena cava inferior en el grupo de ETEVS (p<0,001). A largo plazo se utilizó con mayor frecuencia heparina de bajo peso molecular en el grupo de ETEVS que en el de ETEVI. A los 90días, la recidiva de ETEV, el sangrado y la muerte fueron significativamente más frecuentes en el grupo con ETEVS. El análisis multivariante confirmó que la ETEVI se asoció a un menor número de sangrados mayores (OR, 0,60; IC95%, 0,50-0,61; p<0,001) y mortales (OR, 0,41; IC95%, 0,29-0,62; p<0,001), menor número de recidivas (OR, 0,58; IC95%, 0,39-0,78; p<0,001) y de embolismo pulmonar mortal (OR, 0,29; IC95%, 0,12-0,52; p<0,001). Estas diferencias se mantuvieron en los pacientes cuya ETEV se inició con un embolismo pulmonar o con una trombosis venosa profunda.
ConclusionesLa ETEVI tiene mejor pronóstico que la ETEVS a los 90días del diagnóstico.
The Computerized Registry of Patients with Venous Thromboembolism (RIETE) is a prospective registry that consecutively includes patients diagnosed with venous thromboembolism. We compared the clinical presentation and response to anticoagulant treatment in patients with idiopathic venous thromboembolism (IVT) versus secondary venous thromboembolism (SVT, associated with a risk factor).
Patients and methodsWe analyzed the differences in clinical characteristics, comorbidity, treatment and events during the first 3months after the diagnosis of venous thromboembolism in patients with IVT or SVT and according to their initial clinical presentation.
ResultsA total of 39,921 patients with IVT (n=18,029; 45.1%) or SVT (n=21,892; 54.9%) were enrolled. The patients with IVT had a greater history of venous thromboembolism than those diagnosed with SVT (p<.001). The initial treatment was similar for the 2 groups, but more inferior vena cava filters were placed in the SVT group (p<.001). In the long term, low-molecular-weight heparin was used more often in the SVT group than in the IVT group. At 90days, bleeding, death and the recurrence of venous thromboembolism were significantly more frequent in the SVT group. The multivariate analysis confirmed that IVT was associated with fewer major (OR, 0.60; 95%CI, 0.50-0.61; p<.001) and fatal (OR, 0.41; 95%CI, 0.29-0.62; p<.001) bleedings, fewer relapses (OR, 0.58; 95%CI, 0.39-0.78; p<.001) and fewer fatal pulmonary embolisms (OR, 0.29; 95%CI, 0.12-0.52; p<.001). These differences were maintained in patients whose venous thromboembolism started with a pulmonary embolism or with deep vein thrombosis.
ConclusionsIVT has a better prognosis than SVT at 90days of the diagnosis.
Artículo
Diríjase desde aquí a la web de la >>>FESEMI<<< e inicie sesión mediante el formulario que se encuentra en la barra superior, pulsando sobre el candado.
Una vez autentificado, en la misma web de FESEMI, en el menú superior, elija la opción deseada.

>>>FESEMI<<<
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora