Como consecuencia inevitable de la inmigración latinoamericana, España y otros países europeos deben afrontar el abordaje de la infección/enfermedad chagásica de la que epidemiológicamente persisten más interrogantes que respuestas. El objetivo del estudio es describir la población diagnosticada de infección/enfermedad chagásica residente en la zona metropolitana norte de Barcelona (406.000 habitantes).
Pacientes y métodoEl estudio, prospectivo y multicéntrico en 3 hospitales y una unidad de salud internacional (2007-2011), incluyó a todos los pacientes con serología positiva a Trypanosoma cruzi solicitada por la razón que fuere.
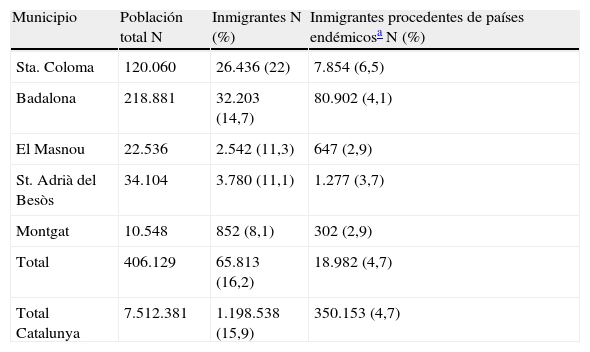
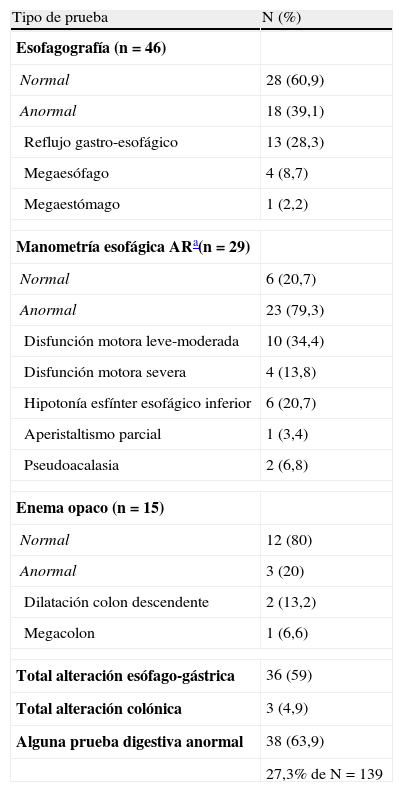
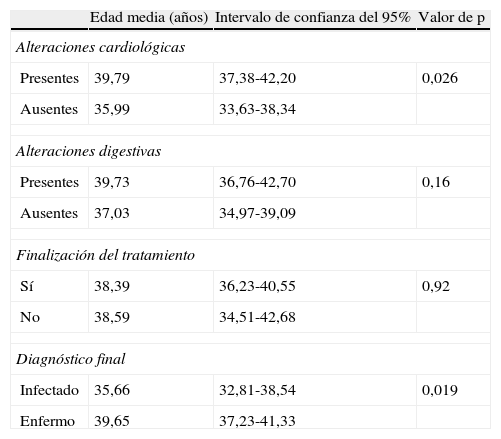
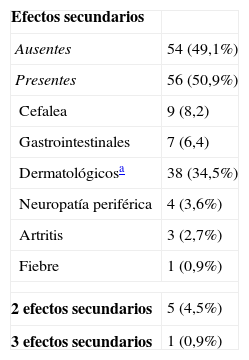
ResultadosLos 139 casos estudiados representan unas incidencias anuales de: a) 0,68/10.000 habitantes, y b) 73,2/10.000 inmigrantes procedentes de zonas endémicas. Estaban enfermos (presentaron alteraciones en alguna prueba complementaria) 80 (57,6%): cardiológicas 62 (44,6%), gastroenterológicas 38 (27,3%) y 20 (14,4%) ambas. Según el Consenso Brasileño de cardiopatía chagásica, se encontraban en estadio 0=84 (60,4%); a=40 (28,7%); b1=4 (2,9%), b2=10 (7,2%) y c/d=1 (0,7%) pacientes. Se indicó tratamiento (benznidazol 5mg/kg/24h durante 60 días) en 116 (83,4%) pacientes, y 89 (76,7%) lo completaron. Presentaron efectos secundarios 56 (50,9%), lo que obligó a retirarlo en 21 ocasiones (19,1%).
ConclusionesEn la zona metropolitana norte de Barcelona han sido diagnosticados menos casos de infección/enfermedad chagásica de los esperables. La serie contiene un elevado número de pacientes enfermos y posiblemente haya un número elevado de inmigrantes procedentes de zonas endémicas en la fase crónica asintomática de la infección que ignoran su estado.
As an inevitable consequence of Latin American immigration to Europe, Spain and other European countries, it is necessary to confront the approach to cases of Chagas infection/disease for which, epidemiologically, there are more questions than answers. This study has aimed to describe all the Chagas-infected population in the north metropolitan area of Barcelona (406,000 inhabitants).
Patients and methodsA prospective and multicentric study was performed in 3 hospitals and 1 International Health Unit. It included all patients with Trypanosoma cruzi positive serology, regardless of the requesting reason.Results The 139 diagnosed cases represent an annual incidence of: a) 0.68/10,000 inhabitants and, b) 73.2/10,000 immigrants coming from endemic zones. Of the patients, 80 (57.6%) had alterations in some complementary tests: cardiologic 62 (44.6%), digestive 38 (27.3%) and 20 (14.4%) both. According to the Brazilian Consensus of Chagas cardiomyopathy, they were classified as: 0=84 (60.4%); a=40 (28.7%); b1=4 (2.9%), b2=10 (7.2%) and c/d=1 (0.7%). Treatment with benznidazole (5mg/kg/24h for 60 days) was prescribed in 116 (83.4%) patients, 89 (76.7%) of whom completed it. Secondary effects were recorded in 56 (50.9%), which made it necessary to withdraw it in 21 (19.1%).
ConclusionsFewer cases of Chagas infection/disease than expected have been diagnosed in the North Metropolitan area of Barcelona. The series contains a high number of patients and there may be an elevated number of immigrants from endemic zones who have the asymptomatic chronic stages of the infection and who were unaware of their condition.
Article
Diríjase desde aquí a la web de la >>>FESEMI<<< e inicie sesión mediante el formulario que se encuentra en la barra superior, pulsando sobre el candado.
Una vez autentificado, en la misma web de FESEMI, en el menú superior, elija la opción deseada.

>>>FESEMI<<<